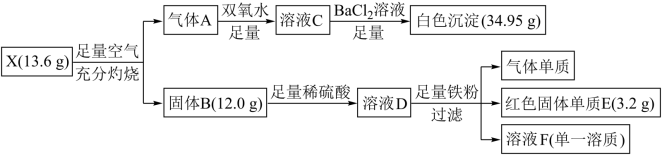
下列框图涉及的物质所含元素中,除一种元素外,其余均为1~18号元素。
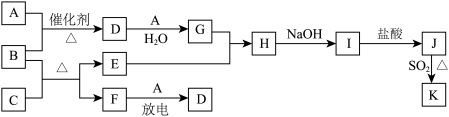
已知:A、F为无色气体单质,B为具有刺激性气味的气体,化学家哈伯因合成B获得1918年的诺贝尔化学奖。C为黑色氧化物,E为紫红色金属单质,I为蓝色沉淀(部分反应的产物未列出)。请回答下列问题:
(1)常温下铝遇到G的浓溶液后表面形成一层致密的保护膜,该现象称为___________ 。
(2)E与G的稀溶液反应的离子方程式为_________ 。
(3)在25 ℃和101 kPa的条件下,将VL的B气体溶于100 mL水中,得到密度为ρg·mL-1的溶液M,则M溶液的物质的量浓度为________ mol·L-1。(已知25 ℃、101 kPa条件下气体摩尔体积为24.5 L·mol-1,不必化简)
(4)分别蘸取B的浓溶液和G的浓溶液的玻璃棒,接近后的现象是_________ 。
(5)B和C反应的化学方程式为__________ 。
(6)J、K是同种金属的不同氯化物,K为白色沉淀。写出SO2还原J生成K的离子方程式:______ 。

已知:A、F为无色气体单质,B为具有刺激性气味的气体,化学家哈伯因合成B获得1918年的诺贝尔化学奖。C为黑色氧化物,E为紫红色金属单质,I为蓝色沉淀(部分反应的产物未列出)。请回答下列问题:
(1)常温下铝遇到G的浓溶液后表面形成一层致密的保护膜,该现象称为
(2)E与G的稀溶液反应的离子方程式为
(3)在25 ℃和101 kPa的条件下,将VL的B气体溶于100 mL水中,得到密度为ρg·mL-1的溶液M,则M溶液的物质的量浓度为
(4)分别蘸取B的浓溶液和G的浓溶液的玻璃棒,接近后的现象是
(5)B和C反应的化学方程式为
(6)J、K是同种金属的不同氯化物,K为白色沉淀。写出SO2还原J生成K的离子方程式:
17-18高一上·天津静海·期末 查看更多[13]
广西来宾市忻城县高级中学2019-2020学年高一上学期期末考试化学试题广西龙州县高级中学2019-2020学年高一上学期期末考试化学试题广西壮族自治区崇左市扶绥县第二中学2019-2020学年高一上学期期末考试化学试题广西壮族自治区崇左市大新县大新中学2019-2020学年高一上学期期末考试化学试题贵州省正安县第二中学2019-2020学年高一上学期期末考试化学试题云南省曲靖市陆良县第十中学2019-2020学年高一上学期期末考试化学试题贵州省安龙县第三中学2019-2020学年高一上学期期末考试化学试题贵州省三穗县三中2019-2020学年高一上学期期末考试化学试题贵州省岑巩县第四中学2019-2020学年高一上学期期末考试化学试题贵州省锦屏中学2019-2020学年高一上学期期末考试化学试题贵州省台江县第二中学2019-2020学年高一上学期期末考试化学试题贵州省独山县第四中学2019-2020学年高一上学期期末考试化学试题天津市六校(静海一中、杨村一中、宝坻一中等)2017-2018学年高一上学期期末联考化学试题
更新时间:2020-02-15 21:01:24
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A-J是中学化学常见的物质,它们之间的转化关系如图所示(部分产物已略去)。已知A是一种高熔点物质,D是一种红棕色固体。
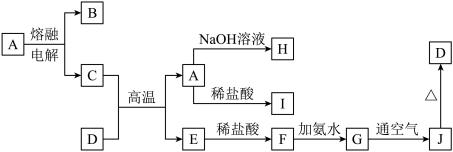
请回答下列问题:
(1)A物质的名称为_______ ;
(2)C与D在高温下的反应在冶金工业上称为_______ 反应,C与D反应的化学方程式:_______ 。
(3)写出G→J的化学方程式:_______ ;
写出J→D的化学方程式:_______ ;
(4)A→H的离子方程式为_______ ;
(5)用离子方程式表示I物质能用于净水的原理_______ 。

请回答下列问题:
(1)A物质的名称为
(2)C与D在高温下的反应在冶金工业上称为
(3)写出G→J的化学方程式:
写出J→D的化学方程式:
(4)A→H的离子方程式为
(5)用离子方程式表示I物质能用于净水的原理
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】短周期元素R、X、Y、Z的原子序数依次增大, a、b、c、d是这4种元素的单质(a、b、c、d顺序不与R、X、Y、Z对应),a为生活中常见的金属,厨房中常见a金属合金餐具和器具。在甲的溶液中通入丙气体,产生白色沉淀,它们之间转化关系如图所示。
回答下列问题:
(1)写出Z元素在元素周期表中的位置______________________ ;
(2)写出物质丙的电子式__________________ ;
(3)X、Y、Z元素简单离子的半径由大到小排列的顺序为(用离子符号表示)______________ ;
(4)写出Y元素的氢氧化物与NaOH溶液反应的离子方程式______________________________ ;
(5)As(砷)与X是同族元素,位于第四周期,请写出砷原子的原子结构示意图____________ 。

回答下列问题:
(1)写出Z元素在元素周期表中的位置
(2)写出物质丙的电子式
(3)X、Y、Z元素简单离子的半径由大到小排列的顺序为(用离子符号表示)
(4)写出Y元素的氢氧化物与NaOH溶液反应的离子方程式
(5)As(砷)与X是同族元素,位于第四周期,请写出砷原子的原子结构示意图
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】为探究氨气的还原性,某同学设计了下列实验装置( 其中夹持装置略去),在实验室中进行实验探究。回答下列问题:
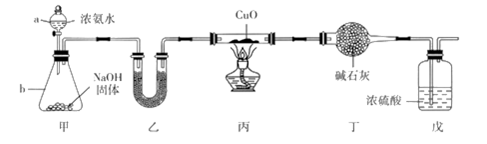
(1)仪器b的名称是_____________________ ,试解释该装置中产生NH3的原理:____________ 。
(2)装置乙中盛有的试剂名称是__________________ 。
(3)装置戊中浓硫酸的作用是_______________________________________________ 。
(4)+1价Cu 在酸性环境中不稳定,可发生反应:Cu2O+2H+==Cu2++Cu + H2O。某同学取上述反应后玻璃管内的物质于试管中,加入稀硫酸,振荡后发现溶液为蓝色,且试管底部有红色Cu,他得出结论:NH3还原CuO生成Cu2O。该同学的判断是否正确?________ (填“正确”或“不正确”),理由是__________________________________________________________________ 。
(5)已知装置丙的玻璃管内CuO粉末为mg,实验结束后测得玻璃管内固体粉末为n g,若CuO 完全被还原 为 Cu,则 m:n=______ ;写出玻璃管内发生反应的化学方程式:__________________ 。装置丁中的干燥管增重为_______ g(用含m 或n 的代数式表示)。

(1)仪器b的名称是
(2)装置乙中盛有的试剂名称是
(3)装置戊中浓硫酸的作用是
(4)+1价Cu 在酸性环境中不稳定,可发生反应:Cu2O+2H+==Cu2++Cu + H2O。某同学取上述反应后玻璃管内的物质于试管中,加入稀硫酸,振荡后发现溶液为蓝色,且试管底部有红色Cu,他得出结论:NH3还原CuO生成Cu2O。该同学的判断是否正确?
(5)已知装置丙的玻璃管内CuO粉末为mg,实验结束后测得玻璃管内固体粉末为n g,若CuO 完全被还原 为 Cu,则 m:n=
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】如图的各方框表示有关的一种反应物或生成物(某些物质已经略去),其中常温下A、C、D为无色气体,B为液体,C能使湿润的红色石蕊试纸变蓝,由X受热分解生成的A、B、C的物质的量之比为1:1:1.
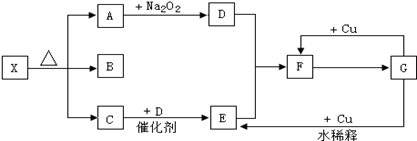
(1)写出下列各物质的化学式:D:______ ;F:_____ 。
(2)写出X分解为A、B、C的化学方程式___________________________________ 。
(3)写出G→E变化的离子方程式____________________________________________ 。

(1)写出下列各物质的化学式:D:
(2)写出X分解为A、B、C的化学方程式
(3)写出G→E变化的离子方程式
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某课外活动小组欲利用CuO与NH3反应,研究NH3的某种性质并测定其组成,设计了如图实验装置(夹持装置未画出)进行实验。请回答下列问题:
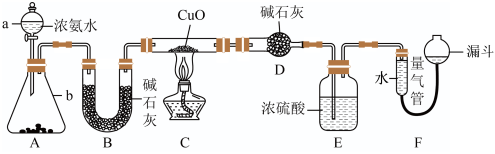
(1)实验室中,利用装置A,还可制取的有色 气体是___ (填字母)。
A.Cl2 B.O2 C.CO2 D.NO2
(2)仪器b中可选择的固体试剂为___ (填名称)。
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管有无色无味的气体生成,上述现象证明NH3具有___ 性,写出相应的化学方程式___ 。
(4)E装置中浓硫酸的两点作用是___ 。
(5)对装置F进行读取气体体积时,下列说法中正确的是___ 。
A.量气管内液面不再变化时抓紧时间读数
B.让量气管内气体冷却到室温后再读数
C.上下移动漏斗,使漏斗和量气管内液面在同一水平线上
D.对量气管进行读数时,眼睛、刻度、凹液面必须在同一水平线上。
(6)实验完毕,若测得仪器D增重mg,装置F测得气体的体积为nL(已折算成标准状况),则氨分子中氮、氢原子个数比为___ (用含m,n字母的代数式表示)。

(1)实验室中,利用装置A,还可制取的
A.Cl2 B.O2 C.CO2 D.NO2
(2)仪器b中可选择的固体试剂为
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管有无色无味的气体生成,上述现象证明NH3具有
(4)E装置中浓硫酸的两点作用是
(5)对装置F进行读取气体体积时,下列说法中正确的是
A.量气管内液面不再变化时抓紧时间读数
B.让量气管内气体冷却到室温后再读数
C.上下移动漏斗,使漏斗和量气管内液面在同一水平线上
D.对量气管进行读数时,眼睛、刻度、凹液面必须在同一水平线上。
(6)实验完毕,若测得仪器D增重mg,装置F测得气体的体积为nL(已折算成标准状况),则氨分子中氮、氢原子个数比为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】化学小组实验探究SO2和AgNO3溶液的反应。
(1)实验一:用如下装置(夹持、加热仪器略)制备SO2,将足量SO2通入AgNO3溶液中,迅速反应,得到无色溶液A和白色沉淀B。
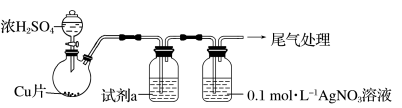
①装浓H2SO4的仪器名称是___________ ,与Cu反应的化学方程式为___________ 。
②试剂a是___________ ,尾气用___________ 溶液吸收,相关离子方程式为___________ 。
(2)对体系中有关物质性质分析得出:沉淀B可能为Ag2SO3、Ag2SO4或二者混合物。
(资料:Ag2SO4微溶于水;Ag2SO3难溶于水,Ag2SO3和NH3·H2O生成[Ag(NH3)2]+)
实验二:验证B的成分

①写出Ag2SO3溶于氨水的离子方程式:___________ 。
②加入盐酸后沉淀D大部分溶解,剩余少量沉淀F.推断D中主要是BaSO3,进而推断B中含有Ag2SO3。向滤液E中加入一种试剂,可进一步证实B中含有Ag2SO3。所用试剂及现象是___________ ,___________ 。
(3)根据沉淀F的存在,推测SO 的产生有两个途径:
的产生有两个途径:
途径1:实验一中,SO2在AgNO3溶液中被氧化生成Ag2SO4,随沉淀B进入D。
途径2:实验二中,SO 被氧化为SO
被氧化为SO 进入D。
进入D。
实验三:探究SO 的产生途径
的产生途径
①向溶液A中滴入过量盐酸,产生白色沉淀,证明溶液中含有___________ ;取上层清液继续滴加BaCl2溶液,未出现白色沉淀,且BaSO4比 Ag2SO4更难溶于水,可判断B中不含Ag2SO4。
②实验三的结论:___________ 。
(4)实验一中SO2与AgNO3溶液反应的离子方程式是___________ 。
①根据物质性质分析,SO2与AgNO3溶液应该可以发生氧化还原反应。将实验一所得混合物放置一段时间,有Ag和SO 生成。
生成。
②根据上述实验所得结论实验条件下:SO2与AgNO3溶液生成Ag2SO3的速率大于生成Ag和SO 的速率;碱性溶液中SO
的速率;碱性溶液中SO 更易被氧化为SO
更易被氧化为SO 。
。
(1)实验一:用如下装置(夹持、加热仪器略)制备SO2,将足量SO2通入AgNO3溶液中,迅速反应,得到无色溶液A和白色沉淀B。

①装浓H2SO4的仪器名称是
②试剂a是
(2)对体系中有关物质性质分析得出:沉淀B可能为Ag2SO3、Ag2SO4或二者混合物。
(资料:Ag2SO4微溶于水;Ag2SO3难溶于水,Ag2SO3和NH3·H2O生成[Ag(NH3)2]+)
实验二:验证B的成分

①写出Ag2SO3溶于氨水的离子方程式:
②加入盐酸后沉淀D大部分溶解,剩余少量沉淀F.推断D中主要是BaSO3,进而推断B中含有Ag2SO3。向滤液E中加入一种试剂,可进一步证实B中含有Ag2SO3。所用试剂及现象是
(3)根据沉淀F的存在,推测SO
 的产生有两个途径:
的产生有两个途径:途径1:实验一中,SO2在AgNO3溶液中被氧化生成Ag2SO4,随沉淀B进入D。
途径2:实验二中,SO
 被氧化为SO
被氧化为SO 进入D。
进入D。实验三:探究SO
 的产生途径
的产生途径①向溶液A中滴入过量盐酸,产生白色沉淀,证明溶液中含有
②实验三的结论:
(4)实验一中SO2与AgNO3溶液反应的离子方程式是
①根据物质性质分析,SO2与AgNO3溶液应该可以发生氧化还原反应。将实验一所得混合物放置一段时间,有Ag和SO
 生成。
生成。②根据上述实验所得结论实验条件下:SO2与AgNO3溶液生成Ag2SO3的速率大于生成Ag和SO
 的速率;碱性溶液中SO
的速率;碱性溶液中SO 更易被氧化为SO
更易被氧化为SO 。
。
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某化学探究小组拟用铜片制取Cu(NO3)2,并探究其化学性质。
I.他们先把铜粉放在空气中灼烧,再与稀HNO3反应制取硝酸铜。
(1)如果直接用铜屑与稀HNO3反应来制取硝酸铜,可能导致的两个不利因素是______ 。
(2)实验中铜粉应该放在_____ (选填“蒸发皿”、“坩埚”或“烧杯”)中灼烧。欲从反应后的溶液中得到硝酸铜晶体,实验操作步骤按顺序分别是___ 、____ 、过滤。
II.为了探究Cu(NO3)2的热稳定性,探究小组按下图中的装置进行实验。(图中铁架台、铁夹和加热设备均略去)
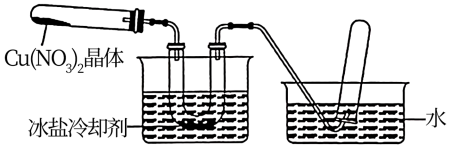
往左试管中放入研细的无水Cu(NO3)2晶体并加热,观察到左试管中有红棕色气体生成,最终残留黑色粉末;用U形管除去红棕色气体,在右试管中收集到无色气体。
(1)红棕色气体是____ 。
(2)当导管口不再有气泡冒出时,停止反应,这时在操作上应注意________ 。
(3)探究小组判断Cu(NO3)2的分解属于氧化还原反应,产物除了红棕色气体和黑色固体外,进一步分析、推断,分解产物中一定还含有_____ 。
III.为了探究Cu(NO3)2在酸性条件下跟铁单质的反应。他们取一支试管,加入Cu(NO3)2溶液,滴入适量稀硫酸酸化,再加入一定量铁粉,实验后没有固体残留物质。该探究小组对反应后溶液中铁元素的价态进行探究,他们设计了实验方案,并进行实验。请在下面表格中补充写出实验操作步骤、预期现象与结论___ 、___ 、___ 。
I.他们先把铜粉放在空气中灼烧,再与稀HNO3反应制取硝酸铜。
(1)如果直接用铜屑与稀HNO3反应来制取硝酸铜,可能导致的两个不利因素是
(2)实验中铜粉应该放在
II.为了探究Cu(NO3)2的热稳定性,探究小组按下图中的装置进行实验。(图中铁架台、铁夹和加热设备均略去)

往左试管中放入研细的无水Cu(NO3)2晶体并加热,观察到左试管中有红棕色气体生成,最终残留黑色粉末;用U形管除去红棕色气体,在右试管中收集到无色气体。
(1)红棕色气体是
(2)当导管口不再有气泡冒出时,停止反应,这时在操作上应注意
(3)探究小组判断Cu(NO3)2的分解属于氧化还原反应,产物除了红棕色气体和黑色固体外,进一步分析、推断,分解产物中一定还含有
III.为了探究Cu(NO3)2在酸性条件下跟铁单质的反应。他们取一支试管,加入Cu(NO3)2溶液,滴入适量稀硫酸酸化,再加入一定量铁粉,实验后没有固体残留物质。该探究小组对反应后溶液中铁元素的价态进行探究,他们设计了实验方案,并进行实验。请在下面表格中补充写出实验操作步骤、预期现象与结论
| 实验操作步骤 | 预期现象与结论 |
| 步骤1:观察样品 | 溶液呈蓝绿色, (填“能”或“不能”)确定 产物中铁元素的化合价 |
| 步骤2:取少量溶液,滴加酸性KMnO4溶液 | |
| 步骤3: | 若溶液变为红色,说明产物中含+3价的铁 元素;若溶液颜色无明显变化,则说明产物 中不含+3价的铁元素 |
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】甲、乙两同学为探究SO2与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验).
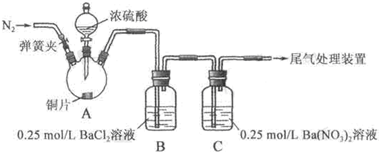
实验操作和现象:
(1)A中反应的化学方程式是___________ 。
(2)C中白色沉淀是___________ ,该沉淀的生成表明SO2具有___________ 性。
(3)C中液面上方生成浅棕色气体的化学方程式是___________ 。
(4)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应.
①为证实各自的观点,在原实验基础上:
甲在原有操作之前增加一步操作,该操作是___________ ;乙在A、B间增加洗气瓶D,D中盛放的试剂是___________ 。
②进行实验,B中现象:
(5)合并(4)中两同学的方案进行实验.B中无沉淀生成,而C中产生白色沉淀,由此得出的结论是___________ 。

实验操作和现象:
| 操作 | 现象 |
| 关闭弹簧夹,滴加一定量浓硫酸,加热 | A中有白雾生成,铜片表面产生气泡 B中有气泡冒出,产生大量白色沉淀 C中产生白色沉淀,液面上方略显浅棕色并逐渐消失 |
| 打开弹簧夹,通入N2,停止加热,一段时间后关闭 | |
| 从B、C中分别取少量白色沉淀,加稀盐酸 | 均未发现白色沉淀溶解 |
(2)C中白色沉淀是
(3)C中液面上方生成浅棕色气体的化学方程式是
(4)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应.
①为证实各自的观点,在原实验基础上:
甲在原有操作之前增加一步操作,该操作是
②进行实验,B中现象:
| 甲 | 大量白色沉淀 |
| 乙 | 少量白色沉淀 |
您最近半年使用:0次