 和
和 均为重要的化工原料,都满足8电子结构
均为重要的化工原料,都满足8电子结构已知:①
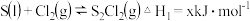
②
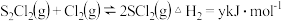
③相关化学键的键能如表所示:
| 化学键 | 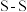 | 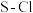 | 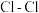 |
键能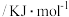 | a | b | c |

A.化学键的键能: |
B.以 的电子式为: 的电子式为: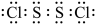 |
C.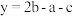 |
D.在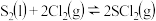 的反应中, 的反应中, |
更新时间:2020-02-17 12:39:05
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】 催化加氢制备
催化加氢制备 是
是 资源化利用的重要途径。已知下图所示的反应的能量变化。
资源化利用的重要途径。已知下图所示的反应的能量变化。

下列说法不正确 的是
 催化加氢制备
催化加氢制备 是
是 资源化利用的重要途径。已知下图所示的反应的能量变化。
资源化利用的重要途径。已知下图所示的反应的能量变化。
下列说法
| A.由图1推知反应物断键吸收的能量小于生成物成键释放的能量 |
B.图2中,若生成的 为液态,则能量变化曲线为① 为液态,则能量变化曲线为① |
C. |
D.制备 的反应使用催化剂时,其 的反应使用催化剂时,其 不变 不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】氨氮是造成水体富营养化的重要因素之一,用次氯酸钠水解生成的次氯酸将水中的氨氮(用NH3表示)转化为氮气除去,相关反应如下:
①NH3+HClO=NH2Cl+H2O
②NH2Cl+HClO=NHCl2+H2O
③2NHCl2+H2O=N2+HClO+3HCl
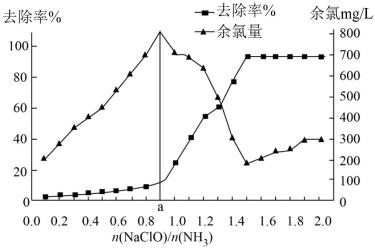
已知在水溶液中NH2Cl较稳定,NHCl2不稳定易转化为氮气。在其他条件一定的情况下,改变 (即NaClO溶液的投入量),溶液中次氯酸钠去除氨氮效果与余氯(溶液中+1价氯元素的含量)影响如图所示。则下列说法正确的是
(即NaClO溶液的投入量),溶液中次氯酸钠去除氨氮效果与余氯(溶液中+1价氯元素的含量)影响如图所示。则下列说法正确的是
①NH3+HClO=NH2Cl+H2O
②NH2Cl+HClO=NHCl2+H2O
③2NHCl2+H2O=N2+HClO+3HCl
已知在水溶液中NH2Cl较稳定,NHCl2不稳定易转化为氮气。在其他条件一定的情况下,改变
 (即NaClO溶液的投入量),溶液中次氯酸钠去除氨氮效果与余氯(溶液中+1价氯元素的含量)影响如图所示。则下列说法正确的是
(即NaClO溶液的投入量),溶液中次氯酸钠去除氨氮效果与余氯(溶液中+1价氯元素的含量)影响如图所示。则下列说法正确的是
| A.次氯酸与氨的总反应可表示为:2NH3+HClO=N2+3H2O+3HCl |
B.反应中氨氮去除效果最佳的 值约为1.5 值约为1.5 |
| C.a点之前溶液中发生的主要反应为:NH2Cl+HClO=NHCl2+H2O |
| D.次氯酸钠溶液pH较小时有O2生成,促使氨氮去除率提高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列说法不正确 的是
| A.增大NH4Cl溶液的浓度,其水的离子积常数和pH均减小 |
| B.盖斯定律表明,一个化学反应的焓变仅与始态和终态有关,与途径无关 |
| C.新能源一般应具有资源丰富、可再生、无污染或少污染等特点 |
| D.工业上在选择合成氨的条件时,不仅要寻找以较高的反应速率获得适当平衡转化率的反应条件,还要考虑原料的价格,氮气、氢气的循环使用,反应热的综合利用等问题 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知反应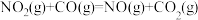 的能量变化如图所示,下列说法正确的是
的能量变化如图所示,下列说法正确的是

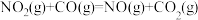 的能量变化如图所示,下列说法正确的是
的能量变化如图所示,下列说法正确的是
A.图中 的过程为放热过程 的过程为放热过程 |
| B.加入合适的催化剂可以降低该反应的活化能 |
C. 和1molCO的键能总和大于1molNO和 和1molCO的键能总和大于1molNO和 的键能总和 的键能总和 |
D.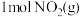 和 和 的总能量低于 的总能量低于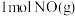 和 和 的总能量 的总能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
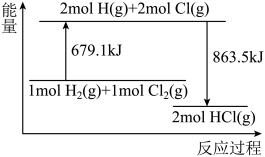
【推荐2】已知断开 中的化学键需要吸收
中的化学键需要吸收 的能量。根据反应
的能量。根据反应 的能量变化示意图,下列说法不正确的是
的能量变化示意图,下列说法不正确的是
 中的化学键需要吸收
中的化学键需要吸收 的能量。根据反应
的能量。根据反应 的能量变化示意图,下列说法不正确的是
的能量变化示意图,下列说法不正确的是
A.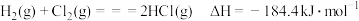 |
B.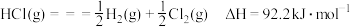 |
C.断开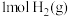 中的化学键需要吸收 中的化学键需要吸收 的能量 的能量 |
D.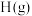 和 和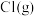 形成 形成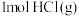 释放 释放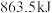 的能量 的能量 |
您最近一年使用:0次



