近年来,科技人员研究得到一种新型材料——泡沫铝。它是把发泡剂加到熔融或固体粉末的铝合金中而制成的,其优点是硬度高、密度小(约为0.16~0.5 g/cm3),比木材还轻,可浮于水面,又有很大刚性,且隔音、保温,是一种良好的建筑材料和轻质材料,可大批量投放市场。回答下列问题:
(1)铝制成铝箔用于食品包装,是利用它的__________ (填序号)。
A.金属光泽 B.延展性C.导电性 D.导热性
(2)铝在空气中会被氧化生成一层致密的氧化膜(氧化物)而对铝起保护作用,但这层氧化膜(氧化物)遇到强酸或强碱都会溶解,请写出其与盐酸反应的离子方程式:_________ 。与氢氧化钠溶液反应的化学方程式: _________ 。
(3)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,相同条件下所得H2的体积之比为______ 。
(4)足量的两份铝分别投入到等体积、一定物质的量浓度的HCl、NaOH溶液中,二者恰好完全反应且产生的H2相等,则HCl和NaOH的物质的量浓度之比是__________ 。
(1)铝制成铝箔用于食品包装,是利用它的
A.金属光泽 B.延展性C.导电性 D.导热性
(2)铝在空气中会被氧化生成一层致密的氧化膜(氧化物)而对铝起保护作用,但这层氧化膜(氧化物)遇到强酸或强碱都会溶解,请写出其与盐酸反应的离子方程式:
(3)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,相同条件下所得H2的体积之比为
(4)足量的两份铝分别投入到等体积、一定物质的量浓度的HCl、NaOH溶液中,二者恰好完全反应且产生的H2相等,则HCl和NaOH的物质的量浓度之比是
19-20高一上·贵州黔南·期末 查看更多[2]
(已下线)3.3 用途广泛的金属材料(基础练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版)贵州省黔南布依族苗族自治州龙里中学2019-2020学年高一上学期期末考试化学试题
更新时间:2020-02-14 21:23:30
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】钠和铝是两种重要的金属。请回答:
(1)钠元素的金属性比铝的_________ (填“强”或“弱”);常温下,可用_________ (填“钠”或“铝”)制成的容器盛装浓硫酸或浓硝酸。
(2)将一小块金属钠投入水中,发生反应的化学方程式为________________________ ;可观察到的实验现象是_________ (填序号)。
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(3)铝与氢氧化钠溶液反应的离子方程式为_________________________ 。
(1)钠元素的金属性比铝的
(2)将一小块金属钠投入水中,发生反应的化学方程式为
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(3)铝与氢氧化钠溶液反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】铁、铝在生产生活中有广泛的应用。完成下列填空:
(1)铝用作电线是利用了铝的________ 性;铁用作炊具是利用了铁的________ 性。
(2)常温下由于浓硫酸能使铁__________ ,因此浓硫酸可用铁槽车运输。
(3)氢氧化铝既能跟盐酸反应又能跟氢氧化钠溶液反应,由此可知氢氧化铝是_____ 物质。氢氧化铝和盐酸反应的离子方程式为_______ 。
(1)铝用作电线是利用了铝的
(2)常温下由于浓硫酸能使铁
(3)氢氧化铝既能跟盐酸反应又能跟氢氧化钠溶液反应,由此可知氢氧化铝是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】金属钠还可以用于钛、锆、铌、钽等金属的冶炼。如Na与 反应产生Ti。
反应产生Ti。
(1)把钠投入 溶液中,不能置换出Ti单质,原因是:
溶液中,不能置换出Ti单质,原因是:_____ 。
以下是Ti及其他2种金属的相关性质:
(2)钛是制造飞机的材料之一、根据表中数据,解释为何用钛来制造飞机_____ 。
(3)钢是主要含铁的合金。汽车车身可以用铝或钢制造。已知铁在潮湿的空气中会迅速腐蚀,而铝不会。
①请解释铝耐腐蚀的原因_____ 。(用方程式表示)
②根据表中数据,描述用铝来取代钢制造汽车车身的一项优点是_____ ,缺点是_____ 。
 反应产生Ti。
反应产生Ti。(1)把钠投入
 溶液中,不能置换出Ti单质,原因是:
溶液中,不能置换出Ti单质,原因是:以下是Ti及其他2种金属的相关性质:
| 金属 | 熔点(℃) | 密度( ) ) | 相对强度 | 相对硬度 | 每吨价格(元) |
| 铝 | 660 | 2.7 | 11 | 2.8 | 11400 |
| 铁 | 1538 | 7.9 | 20 | 4.5 | 4000 |
| 钛 | 1668 | 4.5 | 40 | 6.0 | 160000 |
(3)钢是主要含铁的合金。汽车车身可以用铝或钢制造。已知铁在潮湿的空气中会迅速腐蚀,而铝不会。
①请解释铝耐腐蚀的原因
②根据表中数据,描述用铝来取代钢制造汽车车身的一项优点是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】用C、Fe和Al组成的混合物进行如图所示实验。

填写下列空白.
(1)气体X为________ ,固体Z为________ 。
(2)滤液Y中除H+外,还含有的阳离子为_______ 和_________ 。
(3)滤液N中除Na2SO4和NaOH外,还含有的溶质为_____________ (填化学式)。

填写下列空白.
(1)气体X为
(2)滤液Y中除H+外,还含有的阳离子为
(3)滤液N中除Na2SO4和NaOH外,还含有的溶质为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】将在空气中久置的铝片投入足量稀硫酸中,该铝片与稀硫酸反应产生氢气的速率与反应时间可用下图来表示(已知该反应为放热反应),请回答下列问题。

(1)曲线由 段,用离子方程式表示不产生氢气的原因
段,用离子方程式表示不产生氢气的原因_______ 。
(2)曲线由 段,产生氢气的速率较慢的原因
段,产生氢气的速率较慢的原因_______ 。
(3)曲线由 段,产生氢气的速率增加较快的主要原因
段,产生氢气的速率增加较快的主要原因_______ 。
(4)曲线由c以后,产生氢气的速率逐渐下降的主要原因_______ 。
(5)下列措施能加快上述反应的化学反应速率的是_______。

(1)曲线由
 段,用离子方程式表示不产生氢气的原因
段,用离子方程式表示不产生氢气的原因(2)曲线由
 段,产生氢气的速率较慢的原因
段,产生氢气的速率较慢的原因(3)曲线由
 段,产生氢气的速率增加较快的主要原因
段,产生氢气的速率增加较快的主要原因(4)曲线由c以后,产生氢气的速率逐渐下降的主要原因
(5)下列措施能加快上述反应的化学反应速率的是_______。
| A.加入少量蒸馏水 | B.铝片改为铝粉 |
| C.加入少量饱和硫酸钠溶液 | D.加入少量硫酸铜溶液 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】硫、氮、氯其化合物在生产生活中应用广泛。请回答:
(1)将SO2通入品红溶液中,现象为品红溶液___________ ,加热后溶液颜色___________ 。将Cl2和SO2以1:1通入品红中,不能增强漂白性,用化学用语解释原因___________
(2)工业生产漂白粉有关反应的化学方程式:___________
(3)在汽车尾气排放管处安装一个催化转化器,可使尾气中有害气体CO和NO反应转化为两种无毒气体,该反应的化学方程式___________ 。
(4)0.3mol的钠镁铝分别投入100mL 1mol/L的硫酸中,相同条件下产生H2的体积比是___________
(5)用如图所示装置做实验:常温下将H2S和SO2以物质的量之比为1∶1充满烧瓶,不久烧瓶中能观察到的现象是___________ 。
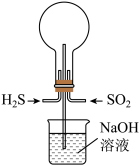
(1)将SO2通入品红溶液中,现象为品红溶液
(2)工业生产漂白粉有关反应的化学方程式:
(3)在汽车尾气排放管处安装一个催化转化器,可使尾气中有害气体CO和NO反应转化为两种无毒气体,该反应的化学方程式
(4)0.3mol的钠镁铝分别投入100mL 1mol/L的硫酸中,相同条件下产生H2的体积比是
(5)用如图所示装置做实验:常温下将H2S和SO2以物质的量之比为1∶1充满烧瓶,不久烧瓶中能观察到的现象是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】现有金属单质A、B、C和气体甲、丙以及物质D、E、F、G、H,它们之间的相互转化关系如下图所示(图中有些反应的生成物和反应的条件没有标出)。
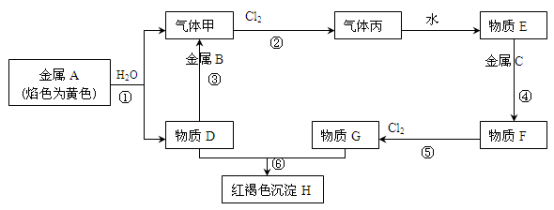
请回答下列问题:
(1)写出下列物质的化学式:B________ 、丙________
(2)写出下列反应的化学方程式:
反应①________________________________________________________________ ;
反应③________________________________________________________________ ;
反应⑥_______________________________________________________________ 。

请回答下列问题:
(1)写出下列物质的化学式:B
(2)写出下列反应的化学方程式:
反应①
反应③
反应⑥
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】铝的阳极氧化是一种重要的表面处理技术,其原理是用电化学方法处理铝件表面,优化氧化膜结构,增强铝件的抗腐蚀性,同时便于表面着色。取铝片模拟该实验,操作步骤如下:
(1)铝片预处理
铝片表面除去油垢后,用2 mol/L NaOH溶液在60~70 ℃ 下洗涤,除去铝表面薄氧化膜,离子方程式为:___________ ;再用10%(质量分数)的HNO3溶液对铝片表面进行化学抛光。若取一定体积68%(质量分数)的浓硝酸配制该化学抛光液,需要用到的玻璃仪有___________ 、___________ 、玻璃棒和胶头滴管。
(2)电解氧化
取预处理过的铝片和铅做电极,控制电流恒定为0.06 A,用直流电源在5~6 mol/L硫酸中电解。其中铝片接电源___________ 极,产生氧化膜(Al2O3)的电极反应式为___________ 。氧化膜的生长过程可大致分为A、B、C三个阶段(如图所示),C阶段多孔层产生孔隙的离子反应方程式为___________ 。

(1)铝片预处理
铝片表面除去油垢后,用2 mol/L NaOH溶液在60~70 ℃ 下洗涤,除去铝表面薄氧化膜,离子方程式为:
(2)电解氧化
取预处理过的铝片和铅做电极,控制电流恒定为0.06 A,用直流电源在5~6 mol/L硫酸中电解。其中铝片接电源

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】写出下列反应的离子方程式。
(1)可溶性多元弱酸或其酸酐与碱溶液反应。
如CO2通入NaOH溶液中
①CO2少量:___________ ;
②CO2足量:___________ 。
类似该反应的还有SO2、H2S、H2C2O4与碱溶液的反应。
(2)AlCl3溶液和NaOH溶液反应
①NaOH少量:___________ ;
②NaOH足量:___________ 。
类似该反应的还有Na2CO3溶液或NaAlO2溶液与稀盐酸的反应。
(3)Fe与稀硝酸反应
①Fe少量:___________ ;
②Fe足量:___________ 。
(1)可溶性多元弱酸或其酸酐与碱溶液反应。
如CO2通入NaOH溶液中
①CO2少量:
②CO2足量:
类似该反应的还有SO2、H2S、H2C2O4与碱溶液的反应。
(2)AlCl3溶液和NaOH溶液反应
①NaOH少量:
②NaOH足量:
类似该反应的还有Na2CO3溶液或NaAlO2溶液与稀盐酸的反应。
(3)Fe与稀硝酸反应
①Fe少量:
②Fe足量:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】英国皇家航空学会2019年度颁奖典礼于2019年11月25日晚在伦敦举行,嫦娥四号任务团队获得团队金奖,成为2019年度全球唯一获此殊荣的团队。这是英国皇家航空学会成立以来首次向中国项目颁发奖项。中国嫦娥四号探测器于2019年1月3日上午10点26分成功在月球背面软着陆,成为人类首次在月球背面软着陆的探测器。玉兔二号月球车实现了对月球背面的巡视。
(1)月球白天地面温度高达150度,而到了夜晚,温度又跌落到零下180度。嫦娥四号探测器、玉兔二号月球车均使用了大量合金材料,这些合金材料应具有哪些性质_________ ?
(2)形状记忆合金是一种在加热升温后能完全消除其在较低的温度下发生的变形,恢复其变形前原始形状的合金材料。中国嫦娥四号探测器,使用了记忆合金制作天线,试分析其好处________ 。
(1)月球白天地面温度高达150度,而到了夜晚,温度又跌落到零下180度。嫦娥四号探测器、玉兔二号月球车均使用了大量合金材料,这些合金材料应具有哪些性质
(2)形状记忆合金是一种在加热升温后能完全消除其在较低的温度下发生的变形,恢复其变形前原始形状的合金材料。中国嫦娥四号探测器,使用了记忆合金制作天线,试分析其好处
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)随着生活水平的提高,人们越来越关注自身的健康。
①平时我们到药店能买到的药如阿司匹林属于___ (选填“R”或“OTC”)类;人体铁元素摄入量不足可能会导致___ 。
②“是药三分毒”说明药物在人体内可能产生不良反应,下列药物可能引起的不良反应叙述错误的是____ (填字母代号)。
A.青霉素一一过敏反应 B.阿司匹林——胃肠道反应 C.复方氢氧化铝——肠胃穿孔
③低血糖病症发作时,喝葡萄糖水可快速见效。葡萄糖作为营养剂供给人体能量,在体内发生的主要反应是___ (填字母代号)。
A.加成反应 B.取代反应 C.氧化反应 D.聚合反应
(2)材料是人类赖以生存的重要物质基础,而化学是材料科学发展的基础。
①在原子反应堆中广泛应用的钠钾合金在常温下呈液态。说明合金的熔点比其各成分金属的熔点___ (选填“高”或“低”)。
②炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便会出现红褐色锈斑。我们将这种腐蚀方式称为___ 。
③人工合成的塑料有多种,其中聚丙烯是常见的食品级塑料,写出聚丙烯的结构简式___ 。
④世博会中国馆——“东方之冠”,它由钢筋混凝土、7000多块红色铝板和1200多块玻璃等建成。钢筋混凝土___ (选填“是”或“不是”)复合材料。
(3)可持续发展需要注意“环境保护”和“节约能源”。
①某污水处理厂处理含酸性物质、泥沙等的污水时,常先加入混凝剂,经曝气、沉砂后,再加入熟石灰处理,加入熟石灰的目的是___ 。
②汽车尾气的大量排放会引起环境污染,在机动车尾气系统中装置催化转化器,可将尾气中的NO、CO转化为无害的CO2和___ 。
(1)随着生活水平的提高,人们越来越关注自身的健康。
①平时我们到药店能买到的药如阿司匹林属于
②“是药三分毒”说明药物在人体内可能产生不良反应,下列药物可能引起的不良反应叙述错误的是_
A.青霉素一一过敏反应 B.阿司匹林——胃肠道反应 C.复方氢氧化铝——肠胃穿孔
③低血糖病症发作时,喝葡萄糖水可快速见效。葡萄糖作为营养剂供给人体能量,在体内发生的主要反应是
A.加成反应 B.取代反应 C.氧化反应 D.聚合反应
(2)材料是人类赖以生存的重要物质基础,而化学是材料科学发展的基础。
①在原子反应堆中广泛应用的钠钾合金在常温下呈液态。说明合金的熔点比其各成分金属的熔点
②炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便会出现红褐色锈斑。我们将这种腐蚀方式称为
③人工合成的塑料有多种,其中聚丙烯是常见的食品级塑料,写出聚丙烯的结构简式
④世博会中国馆——“东方之冠”,它由钢筋混凝土、7000多块红色铝板和1200多块玻璃等建成。钢筋混凝土
(3)可持续发展需要注意“环境保护”和“节约能源”。
①某污水处理厂处理含酸性物质、泥沙等的污水时,常先加入混凝剂,经曝气、沉砂后,再加入熟石灰处理,加入熟石灰的目的是
②汽车尾气的大量排放会引起环境污染,在机动车尾气系统中装置催化转化器,可将尾气中的NO、CO转化为无害的CO2和
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】考古出土的吴王夫差剑为春秋末期制造的青铜剑,历经2500余年,剑的表面虽有一层蓝色薄锈,但仍寒光逼人,剑刃锋利。回答下列问题。
(1)青铜是一种合金材料,该合金的主要成分是___________ (填元素符号)。合金材料有许多优良性能,比如①多数合金的熔点___________ 组成它的任何一种组分金属。②合金的导电性和导热性一般 ___________ 任何一种组分金属。(填“高于”或“低于”)。不锈钢中除了铁元素外,主要的合金元素是 ___________ (占12%-32%),采用该元素作合金是因为: ___________ 。
(2)从上述信息可以看出,青铜具有的性质有___________(填字母)
(3)青铜剑表面的蓝色薄锈,其主要成分为碱式碳酸铜[Cu2(OH)2CO3],这层蓝色薄锈形成的原理是 ___________ 。(用方程式表示)
(4)若要除去表面蓝色薄锈,一是用稀硫酸洗涤,该反应的离子方程式________________ ;此法弊端是 ___________ 。二是可以在炼铁高炉中锻造,其原理 ___________ 。
(1)青铜是一种合金材料,该合金的主要成分是
(2)从上述信息可以看出,青铜具有的性质有___________(填字母)
| A.强度高 | B.耐腐蚀 | C.可塑性好 | D.易加工 |
(4)若要除去表面蓝色薄锈,一是用稀硫酸洗涤,该反应的离子方程式
您最近一年使用:0次



