铁及其化合物之间的相互转化可用下式表示:Fe2+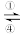 Fe3+
Fe3+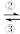 FeO42-(高铁酸根离子)。回答下列有关问题:
FeO42-(高铁酸根离子)。回答下列有关问题:
(1)Fe与过量盐酸反应可以制取FeCl2。若用反应所得的酸性溶液,实现上述①、④的转化,要求产物纯净,可选用__________ (填字母)。
a.Cl2 b.Fe c.Cu d.KMnO4
(2)如下化学方程式中:Fe2O3+3NaClO+4KOH=2K2FeO4(高铁酸钾)+3NaCl+2H2O,还原剂是______________ ,具有__________ 性。
(3)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成氢氧化铁胶体。高铁酸钾作为水处理剂发挥的作用是___________ 、__________ 。
(4)某同学为了检验家中的一瓶补铁药(成分为FeSO4)是否变质,查阅了有关资料,得知Fe2+能被酸性高锰酸钾溶液氧化而使高锰酸钾溶液褪色,并结合已学的知识设计了如下实验:将药片除去糖衣研细后,溶解过滤,取滤液分别加入两支试管中,在试管Ⅰ中滴入酸性高锰酸钾溶液,在试管Ⅱ中滴入KSCN溶液。
①请你填出该同学实验中出现以下现象时应得出的结论:
②能不能将KMnO4和KSCN滴入到同一试管中进行验证,为什么?试进行解释:________ 。
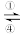 Fe3+
Fe3+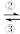 FeO42-(高铁酸根离子)。回答下列有关问题:
FeO42-(高铁酸根离子)。回答下列有关问题:(1)Fe与过量盐酸反应可以制取FeCl2。若用反应所得的酸性溶液,实现上述①、④的转化,要求产物纯净,可选用
a.Cl2 b.Fe c.Cu d.KMnO4
(2)如下化学方程式中:Fe2O3+3NaClO+4KOH=2K2FeO4(高铁酸钾)+3NaCl+2H2O,还原剂是
(3)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成氢氧化铁胶体。高铁酸钾作为水处理剂发挥的作用是
(4)某同学为了检验家中的一瓶补铁药(成分为FeSO4)是否变质,查阅了有关资料,得知Fe2+能被酸性高锰酸钾溶液氧化而使高锰酸钾溶液褪色,并结合已学的知识设计了如下实验:将药片除去糖衣研细后,溶解过滤,取滤液分别加入两支试管中,在试管Ⅰ中滴入酸性高锰酸钾溶液,在试管Ⅱ中滴入KSCN溶液。
①请你填出该同学实验中出现以下现象时应得出的结论:
| 实验现象 | 试管Ⅰ | 试管Ⅱ | 结论 |
| a | 褪色 | 不变红 | |
| b | 不褪色 | 变红 | |
| c | 褪色 | 变红 |
更新时间:2020-02-14 21:23:30
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】Ⅰ.地球上的金属矿物资源是有限的,应合理开发利用。
(1)金属冶炼的实质是金属离子被______ (填“氧化”或“还原”)生成金属单质。
(2)铜在自然界存在于多种矿石中,如:
请回答下列问题:
①上表所列铜化合物中,推断铜的质量百分含量最高的是______ 。
② 其中Cu为+2价、Fe为+2价,高温焙烧时发生的反应是
其中Cu为+2价、Fe为+2价,高温焙烧时发生的反应是 ,焙烧过程中被还原的元素有
,焙烧过程中被还原的元素有______ 。
③工业上以黄铜矿为原料,采用火法熔炼工艺生产铜,火法炼铜的反应为:,该反
应中氧化剂是______ 。
④ 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为__________________ 。
Ⅱ.某校化学兴趣小组通过查阅资料得知用海水获取氯化钠和金属镁的实验流程如图所示,请你根据题意回答下列问题。
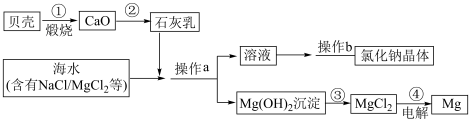
(3)①②③④四个反应中属于复分解反应的是____________ 。
(1)金属冶炼的实质是金属离子被
(2)铜在自然界存在于多种矿石中,如:
| 矿石名称 | 黄铜矿 | 辉铜矿 | 孔雀石 |
| 主要成分 |  |  |  |
①上表所列铜化合物中,推断铜的质量百分含量最高的是
②
 其中Cu为+2价、Fe为+2价,高温焙烧时发生的反应是
其中Cu为+2价、Fe为+2价,高温焙烧时发生的反应是 ,焙烧过程中被还原的元素有
,焙烧过程中被还原的元素有③工业上以黄铜矿为原料,采用火法熔炼工艺生产铜,火法炼铜的反应为:,该反

应中氧化剂是
④
 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为Ⅱ.某校化学兴趣小组通过查阅资料得知用海水获取氯化钠和金属镁的实验流程如图所示,请你根据题意回答下列问题。

(3)①②③④四个反应中属于复分解反应的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】已知高锰酸钾固体在室温下能将浓盐酸氧化,发生反应: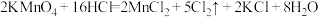
(1)标明上述化学方程式电子转移方向和数目___________ 。
(2)在该反应中,被还原的元素是_______ ,浓盐酸体现了_______ 性质(选填字母编号),氧化剂与还原剂的物质的量之比为______ 。
A.酸性B.碱性C.氧化性D.还原性
(3)产生0.1mol ,则转移的电子数目为
,则转移的电子数目为___________ 。
(4)下列装置中,可用作该反应的气体发生装置的是(选填字母编号)________ 。
A.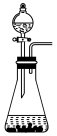 B.
B. C.
C.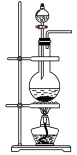
(5)用上述方法制得的氯气中含有杂质,可依次用如图洗气装置净化。装置D中应盛放_____ ,装置E中可盛放______ (均选填字母编号)

A.浓硫酸 B.NaOH溶液 C.饱和食盐水 D.固体 E.碱石灰
E.碱石灰
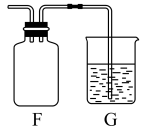
(6)氯气可用排空气法收集,在下图装置F中画出导管的正确位置______ 。装置G中盛放为NaOH溶液,作用是______ ,并写出反应的离子方程式________ 。
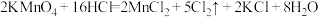
(1)标明上述化学方程式电子转移方向和数目
(2)在该反应中,被还原的元素是
A.酸性B.碱性C.氧化性D.还原性
(3)产生0.1mol
 ,则转移的电子数目为
,则转移的电子数目为(4)下列装置中,可用作该反应的气体发生装置的是(选填字母编号)
A.
 B.
B. C.
C.
(5)用上述方法制得的氯气中含有杂质,可依次用如图洗气装置净化。装置D中应盛放

A.浓硫酸 B.NaOH溶液 C.饱和食盐水 D.固体
 E.碱石灰
E.碱石灰(6)氯气可用排空气法收集,在下图装置F中画出导管的正确位置

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】按要求完成下列问题
(1)已知实验室制备NO的反应为: 。反应中氧化剂是
。反应中氧化剂是_______ ; 被氧化的元素是_______ ;氧化产物是_______ 。
(2)请配平下列方程式_______
_______Al +_______ + _______NaOH= _______
+ _______NaOH= _______ + _______
+ _______ ↑ + _______
↑ + _______
(3)用 溶液与Cu反应制作的印刷电路板,其制作原理可用
溶液与Cu反应制作的印刷电路板,其制作原理可用 表示。
表示。
①上式中X的化学式为_______ 。
②该反应的离子方程式为_______ 。
③请写出反应物氯化铁的电离方程式_______ 。
(1)已知实验室制备NO的反应为:
 。反应中氧化剂是
。反应中氧化剂是(2)请配平下列方程式
_______Al +_______
 + _______NaOH= _______
+ _______NaOH= _______ + _______
+ _______ ↑ + _______
↑ + _______
(3)用
 溶液与Cu反应制作的印刷电路板,其制作原理可用
溶液与Cu反应制作的印刷电路板,其制作原理可用 表示。
表示。①上式中X的化学式为
②该反应的离子方程式为
③请写出反应物氯化铁的电离方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】常见含硫物质A~D,在生活、生产中有着广泛应用,它们之间的转化关系如下图所示。其中反应①、②中所需物质B溶液的浓度不同。

请按要求回答下列问题:
(1)A的化学式为_______ 。
(2)反应①、②中Cu、Fe所起的作用相同,即都作_______ (填“氧化剂”或“还原剂”),你判断的依据是它们都是金属,在反应中都_______ 。
(3)反应②的离子方程式为_______ 。
(4)大气中因废气A引起酸雨的反应流程之一可用下图示意:

上图中由D→B的转化所需氧化剂为_______ 。
当将含D的雨水敞口放置一段时间后(忽略溶液体积、温度的变化),其c(H+)将_______ 。(填“增大”“减小”或“不变”)。废气A是一种重要的化工原料,常采用氨吸收法进行循环利用、变废为宝。某工厂若将4.48×106L(标准状况下)废气A进行环保处理,完全转化为 NH4HSO3时,需消耗10mol/L氨水溶液(溶质全部以NH3•H2O计)的体积为_______ L。

请按要求回答下列问题:
(1)A的化学式为
(2)反应①、②中Cu、Fe所起的作用相同,即都作
(3)反应②的离子方程式为
(4)大气中因废气A引起酸雨的反应流程之一可用下图示意:

上图中由D→B的转化所需氧化剂为
当将含D的雨水敞口放置一段时间后(忽略溶液体积、温度的变化),其c(H+)将
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知有以下物质相互转化。其中A为金属试回答:

(1)写出B的化学式________________ ,D的化学式________________ 。
(2)写出由D转变成H的化学方程式________________ 。
(3)写出向G溶液加入A的有关离子反应方程式________________ 。
(4)写出E转变为F的实验现象为:_________________________ 化学方程式:___________________ 。

(1)写出B的化学式
(2)写出由D转变成H的化学方程式
(3)写出向G溶液加入A的有关离子反应方程式
(4)写出E转变为F的实验现象为:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。回答下列问题:
(1)晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,以K3[Fe(CN)6]溶液为显色剂。其光解反应的化学方程式为:2K3[Fe(C2O4)3]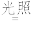 2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为
2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为___ 。
(2)某小组为探究三草酸合铁酸钾的热分解产物,按如图所示装置进行实验。

①通入氮气的目的是____ 。
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有____ 、___ 。
③为防止倒吸,停止实验时应进行的操作是___ 。
④样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是____ 。
(1)晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,以K3[Fe(CN)6]溶液为显色剂。其光解反应的化学方程式为:2K3[Fe(C2O4)3]
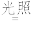 2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为
2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为(2)某小组为探究三草酸合铁酸钾的热分解产物,按如图所示装置进行实验。

①通入氮气的目的是
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有
③为防止倒吸,停止实验时应进行的操作是
④样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】为探究铁和铁的化合物的一些化学性质,某学生实验小组设计了以下实验。
(1)高温下,让铁粉与水蒸气反应,见题图。试管中发生的化学方程式是________________ ,该反应中氧化剂是________________ 。

(2)如图:

①往A溶液中滴入几滴KSCN溶液,溶液的颜色________________ 。
②写出上述过程中A→B的离子方程式________________ 。
③描述C暴露在空气中的颜色变化________________ 。写出相关的化学方程式________________ 。
④写出B加入氯水的离子方程式________________ 。
(1)高温下,让铁粉与水蒸气反应,见题图。试管中发生的化学方程式是

(2)如图:

①往A溶液中滴入几滴KSCN溶液,溶液的颜色
②写出上述过程中A→B的离子方程式
③描述C暴露在空气中的颜色变化
④写出B加入氯水的离子方程式
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】物质A~K存在下图转化关系,其中气体D为单质,E为氯气。试回答下列问题:

(1)写出下列物质的化学式:A是________ 。
(2)写出下列反应的离子方程式:
C→F____________________________________________
I→J_____________________________________________
(3)在溶液I中滴入NaOH溶液,可观察到的现象是___________________________ ,其反应的原理为____________________________________ (写化学方程式)。
(4)检验溶液J中的金属阳离子,所选用的试剂为__________ (填化学式),现象为___________________ 。

(1)写出下列物质的化学式:A是
(2)写出下列反应的离子方程式:
C→F
I→J
(3)在溶液I中滴入NaOH溶液,可观察到的现象是
(4)检验溶液J中的金属阳离子,所选用的试剂为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】纳米铁粉常用于废水处理,以草酸(H2C2O4)与FeSO4为原料可制取纳米铁粉。
I.制取草酸
用含有适量催化剂的混酸(65%HNO3与98%H2SO4的质量比为2:1.5)溶液氧化淀粉水解液制备草酸,其装置如下图所示。[已知:硝酸氧化淀粉水解液过程中主要反应: (未配平)]
(未配平)]

(1)仪器甲的名称为___________ 。
(2)装置B的作用___________ 。
(3)控制反应温度不超过60℃可以防止有机物脱水炭化和___________ 。
Ⅱ.制备纳米铁粉,其流程如下:

已知:H2C2O4为二元弱酸。
(4)检验酸溶后的溶液是否含Fe3+的试剂是___________ 。
(5)向酸溶后的溶液中滴加稍过量的H2C2O4,过滤得FeC2O4∙2H2O。
①沉淀反应的离子方程式为___________ 。
②过滤所得沉淀中FeC2O4∙2H2O含量的测定:准确称取5.800g沉淀,加入适量的蒸馏水和稀硫酸溶解、酸化,并转移入250mL容量瓶中定容,取25.00mL溶液,向其中滴加0.1000mol∙L-1 KMnO4溶液,完全反应时,消耗KMnO4溶液18.00mL。过程中发生的反应为: (未配平,假设杂质不参与反应)。计算沉淀中FeC2O4∙2H2O (相对分子质量为180)的质量分数
(未配平,假设杂质不参与反应)。计算沉淀中FeC2O4∙2H2O (相对分子质量为180)的质量分数___________ (写出计算过程)。
I.制取草酸
用含有适量催化剂的混酸(65%HNO3与98%H2SO4的质量比为2:1.5)溶液氧化淀粉水解液制备草酸,其装置如下图所示。[已知:硝酸氧化淀粉水解液过程中主要反应:
 (未配平)]
(未配平)]
(1)仪器甲的名称为
(2)装置B的作用
(3)控制反应温度不超过60℃可以防止有机物脱水炭化和
Ⅱ.制备纳米铁粉,其流程如下:

已知:H2C2O4为二元弱酸。
(4)检验酸溶后的溶液是否含Fe3+的试剂是
(5)向酸溶后的溶液中滴加稍过量的H2C2O4,过滤得FeC2O4∙2H2O。
①沉淀反应的离子方程式为
②过滤所得沉淀中FeC2O4∙2H2O含量的测定:准确称取5.800g沉淀,加入适量的蒸馏水和稀硫酸溶解、酸化,并转移入250mL容量瓶中定容,取25.00mL溶液,向其中滴加0.1000mol∙L-1 KMnO4溶液,完全反应时,消耗KMnO4溶液18.00mL。过程中发生的反应为:
 (未配平,假设杂质不参与反应)。计算沉淀中FeC2O4∙2H2O (相对分子质量为180)的质量分数
(未配平,假设杂质不参与反应)。计算沉淀中FeC2O4∙2H2O (相对分子质量为180)的质量分数
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】有关物质的转化关系如下图所示。A、C、E是常见的金属单质,E为紫红色,反应①可用于焊接铁轨,B是赤铁矿的主要成分,F的溶液中加入KSCN溶液变红。(部分反应物和生成物省略)
请回答下列问题:
(1)D的化学式是________ 。
(2)可选用________ (填“字母”)实现反应C→F的转化。
a.稀盐酸 b.氯气/点燃 c.CuSO4溶液
(3)反应①的化学方程式为____________ 。
(4)反应②的离子方程式为______________ 。

请回答下列问题:
(1)D的化学式是
(2)可选用
a.稀盐酸 b.氯气/点燃 c.CuSO4溶液
(3)反应①的化学方程式为
(4)反应②的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知有以下物质相互转化
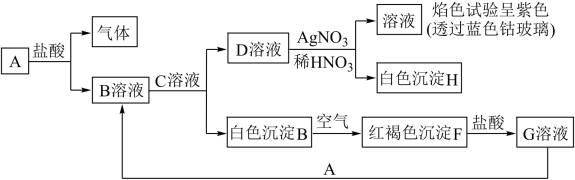
试回答:
(1)写出E的化学式___ ,H的化学式___ 。
(2)写出由E转变成F的化学方程式____ 。
(3)检验G溶液中的金属阳离子的方法是___ ;向G溶液加入A的有关离子反应方程式___ 。
(4)写出A在一定条件下与水反应的化学方程式___ 。

试回答:
(1)写出E的化学式
(2)写出由E转变成F的化学方程式
(3)检验G溶液中的金属阳离子的方法是
(4)写出A在一定条件下与水反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】铁及其化合物之间的相互转化可用下式表示:
Fe2+ Fe3+
Fe3+ FeO
FeO
(1)Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液实现上述①的转化,要求产物纯净,可选用的试剂是____ (填标号)。
a.Cl2 b.Fe c.HNO3 d.H2O2
(2)检验硫酸铁溶液中存在Fe2+的方法是____ 。
(3)配平下面的缺项方程式:____ 。
FeCl3+ Cl2+ = Na2FeO4+ NaCl+ H2O
= Na2FeO4+ NaCl+ H2O
(4)某同学用含有Fe2+、Fe3+的溶液A制备磁性Fe3O4胶体粒子,并测定产物中铁元素的含量,过程如图。已知:反应中K2Cr2O7被还原为Cr3+。

①写出由溶液A制备磁性Fe3O4胶体粒子的离子方程式:____ 。
②由溶液A制得Fe3O4胶体粒子的过程中,需持续通入N2,其原因是____ 。
③SnCl2溶液的作用是____ 。
④写出酸性条件下,乙→丙的离子方程式:____ 。
Fe2+
 Fe3+
Fe3+ FeO
FeO
(1)Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液实现上述①的转化,要求产物纯净,可选用的试剂是
a.Cl2 b.Fe c.HNO3 d.H2O2
(2)检验硫酸铁溶液中存在Fe2+的方法是
(3)配平下面的缺项方程式:
FeCl3+ Cl2+
 = Na2FeO4+ NaCl+ H2O
= Na2FeO4+ NaCl+ H2O(4)某同学用含有Fe2+、Fe3+的溶液A制备磁性Fe3O4胶体粒子,并测定产物中铁元素的含量,过程如图。已知:反应中K2Cr2O7被还原为Cr3+。

①写出由溶液A制备磁性Fe3O4胶体粒子的离子方程式:
②由溶液A制得Fe3O4胶体粒子的过程中,需持续通入N2,其原因是
③SnCl2溶液的作用是
④写出酸性条件下,乙→丙的离子方程式:
您最近一年使用:0次



