取等物质的量浓度的 溶液两份A和B,每份10mL,分别向A、B中通入不等量的
溶液两份A和B,每份10mL,分别向A、B中通入不等量的 ,再继续向两溶液中逐滴加入
,再继续向两溶液中逐滴加入 的盐酸,标准状况下产生的
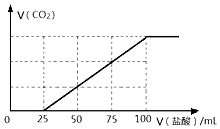
的盐酸,标准状况下产生的 气体体积与所加的盐酸溶液体积之的关系如下图所示,试回答下列问题:
气体体积与所加的盐酸溶液体积之的关系如下图所示,试回答下列问题:
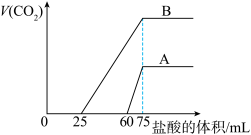
(1)原 溶液的物质的量浓度为
溶液的物质的量浓度为________ 
(2)曲线A表明,原 溶液中通入
溶液中通入 后,所得溶液中的溶质为(写化学式)
后,所得溶液中的溶质为(写化学式)________ ;其物质的量之比为________ ;
(3)曲线B表明,原 溶液中通入
溶液中通入 后,所得溶液加盐酸后产生
后,所得溶液加盐酸后产生 气体体积(标准状况)的最大值为
气体体积(标准状况)的最大值为________ mL。
 溶液两份A和B,每份10mL,分别向A、B中通入不等量的
溶液两份A和B,每份10mL,分别向A、B中通入不等量的 ,再继续向两溶液中逐滴加入
,再继续向两溶液中逐滴加入 的盐酸,标准状况下产生的
的盐酸,标准状况下产生的 气体体积与所加的盐酸溶液体积之的关系如下图所示,试回答下列问题:
气体体积与所加的盐酸溶液体积之的关系如下图所示,试回答下列问题:
(1)原
 溶液的物质的量浓度为
溶液的物质的量浓度为
(2)曲线A表明,原
 溶液中通入
溶液中通入 后,所得溶液中的溶质为(写化学式)
后,所得溶液中的溶质为(写化学式)(3)曲线B表明,原
 溶液中通入
溶液中通入 后,所得溶液加盐酸后产生
后,所得溶液加盐酸后产生 气体体积(标准状况)的最大值为
气体体积(标准状况)的最大值为
11-12高三上·湖北襄阳·期中 查看更多[10]
(已下线)2012届湖北省襄阳市四校高三上学期期中联考化学试卷2016届山东省乳山市第一中学高三上学期10月月考化学试卷2015-2016学年广东省汕头金山中学高一上期末化学试卷2016-2017学年江西省南昌二中高一上第二次考试化学卷黑龙江省齐齐哈尔市第八中学2019届高三9月月考化学试题湖北省武汉市汉阳一中2018-2019学年高一上学期12月月考化学试题江西省新余市分宜中学2020届高三上学期第一次段考化学试题(已下线)【新东方】2020-44(已下线)专题3.1 金属钠及其化合物 -巅峰冲刺山东省2020年高考化学一轮考点扫描《2020年新高考政策解读与配套资源》天津市耀华中学2021-2022学年高一上学期期中考试化学试题
更新时间:2020-02-27 17:55:27
|
相似题推荐
计算题
|
较难
(0.4)
解题方法
【推荐1】某工厂以精辉铜矿(主要成分为Cu2S)为原料冶炼铜,在炼铜炉内发生如下反应(在高温条件下进行):2Cu2S+3O22Cu2O+2SO2,2Cu2O+Cu2S6Cu+SO2
(1)若生成38.4吨金属铜,需要含杂质20%的精辉铜矿多少吨?___ (设杂质不参加反应)
(2)若(1)中产生的二氧化硫用于生产硫酸,可生产98%的硫酸多少吨___ (二氧化硫转化成三氧化硫的转化率为92%,三氧化硫的吸收率为98%)?(保留3位小数)
(3)今将amolCu2S与bmol空气(氧气约占空气体积的20%)在密闭容器中高温加热,设反应前容器内的压强为P1,反应结束后冷却到原来的温度,容器内的压强为P2,请完成下列表格:___
(1)若生成38.4吨金属铜,需要含杂质20%的精辉铜矿多少吨?
(2)若(1)中产生的二氧化硫用于生产硫酸,可生产98%的硫酸多少吨
(3)今将amolCu2S与bmol空气(氧气约占空气体积的20%)在密闭容器中高温加热,设反应前容器内的压强为P1,反应结束后冷却到原来的温度,容器内的压强为P2,请完成下列表格:
| 反应后固体的成分 | Cu | Cu2S、Cu | Cu2O、Cu |
| b的取值范围 | |||
| P1与P2的关系(填>、<、=) | P1 P2 | P1 P2 | P1 P2 |
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】工业以黄铁矿为原料生产硫酸,吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的SO2和铵盐。为测定该铵盐中氮元素的质量分数,将不同质量的铵盐分别加入到50.00mL相同浓度的NaOH溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。部分测定结果如下表:
计算:该铵盐中氮元素的质量分数_______ (计算结果保留两位小数)
| 铵盐的质量(g) | 10.00 | 20.00 | 30.00 | 50.00 |
| 浓硫酸增加的质量(g) | m | m | 1.29 | 0 |
计算:该铵盐中氮元素的质量分数
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】向某NaOH溶液分别通入不同量的CO2气体,得到A、B、C三种溶液。分别向这三种溶液中滴入1mol·L-1的盐酸,得到的气体变化如图。则:

(1)A溶液中的溶质为___________ 。
(2)C溶液中有两种溶质,除去其中碱性强的溶质的方法为:___________ 。

(1)A溶液中的溶质为
(2)C溶液中有两种溶质,除去其中碱性强的溶质的方法为:
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】某 样品露置在空气中部分变质生成
样品露置在空气中部分变质生成 ,为确定其中
,为确定其中 和
和 的含量,称取四份该样品溶于水后,分别逐滴加入相同浓度盐酸
的含量,称取四份该样品溶于水后,分别逐滴加入相同浓度盐酸 ,充分反应,产生气体的总体积(已折算成标准状况下的体积,不考虑气体在水中的溶解)如下表:
,充分反应,产生气体的总体积(已折算成标准状况下的体积,不考虑气体在水中的溶解)如下表:
(1)样品中物质的量之比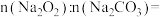
___________ 。
(2)盐酸的物质的量浓度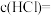
___________ 。
 样品露置在空气中部分变质生成
样品露置在空气中部分变质生成 ,为确定其中
,为确定其中 和
和 的含量,称取四份该样品溶于水后,分别逐滴加入相同浓度盐酸
的含量,称取四份该样品溶于水后,分别逐滴加入相同浓度盐酸 ,充分反应,产生气体的总体积(已折算成标准状况下的体积,不考虑气体在水中的溶解)如下表:
,充分反应,产生气体的总体积(已折算成标准状况下的体积,不考虑气体在水中的溶解)如下表:| 实验序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 盐酸体积/mL | 100.0 | 100.0 | 100.0 | 100.0 |
| 样品质量/g | 2.62 | 3.93 | 5.24 | 6.55 |
| 气体总体积/mL | 448 | 560 | 448 | 560 |
(1)样品中物质的量之比
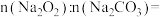
(2)盐酸的物质的量浓度
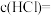
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐1】将5 g碳酸钠、碳酸氢钠和氢氧化钠固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入2mol/L的盐酸,当加入盐酸的体积为45mL时产生CO2的体积为896 mL(标准状况),之后再加入盐酸不再产生CO2。
(1)当加入40 mL盐酸时,产生二氧化碳的体积为_________ mL;(标准状况)
(2)计算原混合物中Na2CO3的质量分数为____________ ;
(3)请在右图中绘制出加入盐酸体积与产生CO2体积的关系曲线。(要在纵坐标上标明标准状况下CO2体积的数值)____________
(1)当加入40 mL盐酸时,产生二氧化碳的体积为
(2)计算原混合物中Na2CO3的质量分数为
(3)请在右图中绘制出加入盐酸体积与产生CO2体积的关系曲线。(要在纵坐标上标明标准状况下CO2体积的数值)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】取一定物质的量浓度的 NaOH 溶液 100 mL,向其中通入一定量的 CO2 气体,得到溶液 A,向A 中逐滴缓慢加入 2.00mol/L 的 HCl 溶液,产生的 CO2 气体体积 (标准状况)与所加 HCl 溶液的体积之间关系如图所示,请回答(结果留三位有效数字):
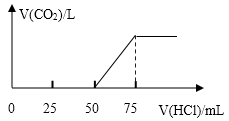
(1)A 溶液中的溶质_________ 。(用化学式表示)
(2)通入的 CO2 的体积(标准状况)为______ L。
(3)原 NaOH 溶液的物质的量浓度_____ mol/L。

(1)A 溶液中的溶质
(2)通入的 CO2 的体积(标准状况)为
(3)原 NaOH 溶液的物质的量浓度
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】取物质的量浓度相等的NaOH溶液两份甲和乙,每份50 mL,分别向甲、乙中通入不等量的CO2,再继续向两溶液中逐滴加入0.1mol/L的HCl溶液,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如下图所示,试回答下列问题:
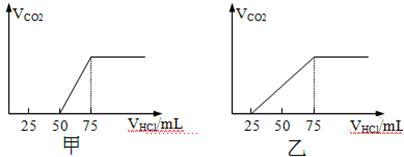
试分析NaOH在吸收CO2气体后,在甲所得溶液中存在的溶质是_________ ,其物质的量之比是_________ , 产生的CO2气体体积(标况)是___________ . 在乙所得溶液中存在的溶质是_________ ,其物质的量之比是___________ , 产生的CO2气体体积(标况)是_________ .

试分析NaOH在吸收CO2气体后,在甲所得溶液中存在的溶质是
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】将一定量的CO2气体通入500 mL某氢氧化钠溶液中,充分反应后将溶液在低温下蒸发,得到不含结晶水的白色固体A,取三份质量不相同的A试样分别与50mL相同浓度的盐酸溶液反应,得到标准状况下气体体积与固体A的质量关系如表所示:
(1)试判断:A的成分___ 。
(2)盐酸物质的量浓度为___ mol•L﹣1。
| 组别 | ① | ② | ③ |
| A的质量 | 3.80 | 5.70 | 7.60 |
| 气体体积(mL) | 896 | 1344 | 1120 |
(1)试判断:A的成分
(2)盐酸物质的量浓度为
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】将5 g碳酸钠、碳酸氢钠和氢氧化钠固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入2mol/L的盐酸,当加入盐酸的体积为45mL时产生CO2的体积为896 mL(标准状况),之后再加入盐酸不再产生CO2。
(1)当加入40 mL盐酸时,产生二氧化碳的体积为_________ mL;(标准状况)
(2)计算原混合物中Na2CO3的质量分数为____________ ;
(3)请在右图中绘制出加入盐酸体积与产生CO2体积的关系曲线。(要在纵坐标上标明标准状况下CO2体积的数值)____________
(1)当加入40 mL盐酸时,产生二氧化碳的体积为
(2)计算原混合物中Na2CO3的质量分数为
(3)请在右图中绘制出加入盐酸体积与产生CO2体积的关系曲线。(要在纵坐标上标明标准状况下CO2体积的数值)
您最近一年使用:0次