工业以黄铁矿为原料生产硫酸,吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的SO2和铵盐。为测定该铵盐中氮元素的质量分数,将不同质量的铵盐分别加入到50.00mL相同浓度的NaOH溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。部分测定结果如下表:
计算:该铵盐中氮元素的质量分数_______ (计算结果保留两位小数)
| 铵盐的质量(g) | 10.00 | 20.00 | 30.00 | 50.00 |
| 浓硫酸增加的质量(g) | m | m | 1.29 | 0 |
计算:该铵盐中氮元素的质量分数
更新时间:2021-08-05 13:46:11
|
相似题推荐
计算题
|
较难
(0.4)
解题方法
【推荐1】2.76 g CaO2·8H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线,140 ℃时完全脱水,杂质受热不分解)如图所示。

①试确定60 ℃时CaO2·xH2O中x=___________ 。
②该样品中CaO2的质量分数为___________ 。

①试确定60 ℃时CaO2·xH2O中x=
②该样品中CaO2的质量分数为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】氨气、氯气和化合物A是常见化合物,在工农业生产中有重要的应用。根据题意回答下列问题:
(1)化合物A的相对分子质量为60(含四种元素),A在一定条件下水解有氨气产生,A分子中碳元素、氧元素和氢元素的质量百分含量分别是20%、26.674%和6.7%。计算确定A的结构简式为_______ 。说出A在一种用途___________ 。
(2)NH3和Cl2在常温下可快速反应生成氮气和氯化铵:8NH3+3Cl2 →N2+6NH4Cl。该反应可用于检验化工生产中氯气是否泄漏。若要在实验室配制体积比为336:1的氨水1kg,计算此氨水的物质的量的浓度为多少________ ?(已知氨水密度为0.92g·cm-3、水的密度为0.899g·cm-3)
(3)常温常压下,取总物质的量为12mol的氯气和氨气的混合气体,完全反应后,气体总物质的量保持不变。求:
① 反应前氯气和氨气的物质的量之比为多少________ ?
② 反应后生成的氧化产物的质量为多少________ ?
(4)已知氨气和氯气混合可发生下列反应: 2NH3+3Cl2 → 6HCl+N2,NH3+HCl → NH4Cl 现有Cl2和NH3共aL,混合后充分反应,气体体积变为bL,问有多少升的NH3被氧化________ ?(气体前后气体体积均在同温同压下)。
(1)化合物A的相对分子质量为60(含四种元素),A在一定条件下水解有氨气产生,A分子中碳元素、氧元素和氢元素的质量百分含量分别是20%、26.674%和6.7%。计算确定A的结构简式为
(2)NH3和Cl2在常温下可快速反应生成氮气和氯化铵:8NH3+3Cl2 →N2+6NH4Cl。该反应可用于检验化工生产中氯气是否泄漏。若要在实验室配制体积比为336:1的氨水1kg,计算此氨水的物质的量的浓度为多少
(3)常温常压下,取总物质的量为12mol的氯气和氨气的混合气体,完全反应后,气体总物质的量保持不变。求:
① 反应前氯气和氨气的物质的量之比为多少
② 反应后生成的氧化产物的质量为多少
(4)已知氨气和氯气混合可发生下列反应: 2NH3+3Cl2 → 6HCl+N2,NH3+HCl → NH4Cl 现有Cl2和NH3共aL,混合后充分反应,气体体积变为bL,问有多少升的NH3被氧化
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】为测定某一混合铵盐的成分(主要含有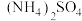 和
和 ),将不同质量的样品分别加入到
),将不同质量的样品分别加入到 浓度相同的
浓度相同的 溶液中,沸水浴加热至气体全部逸出(此温度下该铵盐不分解)。气体干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量如下表所示:
溶液中,沸水浴加热至气体全部逸出(此温度下该铵盐不分解)。气体干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量如下表所示:
(1)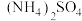 和
和 的物质的量之比
的物质的量之比______ ;
(2) 溶液的物质的量浓度为
溶液的物质的量浓度为______  ;
;
(3)第三次实验时浓硫酸增加的质量a的值为______ 。
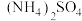 和
和 ),将不同质量的样品分别加入到
),将不同质量的样品分别加入到 浓度相同的
浓度相同的 溶液中,沸水浴加热至气体全部逸出(此温度下该铵盐不分解)。气体干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量如下表所示:
溶液中,沸水浴加热至气体全部逸出(此温度下该铵盐不分解)。气体干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量如下表所示:| 实验次数 | 1 | 2 | 3 | 4 |
铵盐质量/ | 9.05 | 18.10 | 27.15 | 36.2 |
浓硫酸增重/ | 1.7 | 1.7 |  | 0 |
(1)
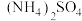 和
和 的物质的量之比
的物质的量之比(2)
 溶液的物质的量浓度为
溶液的物质的量浓度为 ;
;(3)第三次实验时浓硫酸增加的质量a的值为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】某同学取一定质量的铁铝合金与100 mLxmol/L稀硝酸充分反应,反应过程中没有气体放出。在反应结束后的溶液中,逐滴加入2 mol/L NaOH溶液,所加 NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)的关系如图所示:

(1)写出EF段发生反应的离子方程式____________
(2)C点对应的溶液中含有的阳离子除Na+外,还含有_______ 。
(3)x =________ 。
(4)铁铝合金中铝的物质的量分数为_________ 。

(1)写出EF段发生反应的离子方程式
(2)C点对应的溶液中含有的阳离子除Na+外,还含有
(3)x =
(4)铁铝合金中铝的物质的量分数为
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】在100mL NaOH溶液中加入NH4NO3和(NH4)2SO4的固体混合物,加热充分反应。下图表示加入的混合物的质量与产生的气体体积(标准状况)的关系。
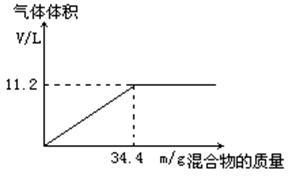
(1) NaOH溶液的物质的量浓度为________ 。
(2)当NaOH溶液的体积为80mL,固体混合物的质量为34.4g,充分反应后,生成气体的体积在标准状况下为_______ 升。
(3)当NaOH溶液的体积为120mL,固体混合物的质量仍为34.4g,充分反应后,生成气体的体积在标准状况下为_______ 升。

(1) NaOH溶液的物质的量浓度为
(2)当NaOH溶液的体积为80mL,固体混合物的质量为34.4g,充分反应后,生成气体的体积在标准状况下为
(3)当NaOH溶液的体积为120mL,固体混合物的质量仍为34.4g,充分反应后,生成气体的体积在标准状况下为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】完成下列问题:
(1)1.000g铝黄铜合金(设只含铜、锌、铝)与0.100mol·dm-3硫酸反应,在25℃和101.325kPa下测得放出的气体的体积为149.3cm3,将相同质量的该合金溶于足量热浓硫酸,在相同温度和压强下测得放出的气体的体积为411.1cm3,计算此铝黄铜合金中各组分的质量分数_____ 。
(2)向[Cu(NH3)4]SO4水溶液中通入SO2气体至溶液呈微酸性,析出白色沉淀CuNH4SO3,CuNH4SO3与足量的硫酸混合并微热,得到金属Cu等物质,本法制得的Cu呈超细粉末状,有重要用途。
①写出生成CuNH4SO3的反应方程式______ 。
②写出CuNH4SO3与H2SO4作用的反应方程式_____ ,若反应在敞开反应器中进行,计算反应物中的Cu元素变成超细粉末Cu的转化率______ 。
③若反应在密闭容器中进行,且酸量充足,计算反应物中的Cu元素变成超细粉末Cu的转化率_____ 。并对此做出解释______ 。
(1)1.000g铝黄铜合金(设只含铜、锌、铝)与0.100mol·dm-3硫酸反应,在25℃和101.325kPa下测得放出的气体的体积为149.3cm3,将相同质量的该合金溶于足量热浓硫酸,在相同温度和压强下测得放出的气体的体积为411.1cm3,计算此铝黄铜合金中各组分的质量分数
(2)向[Cu(NH3)4]SO4水溶液中通入SO2气体至溶液呈微酸性,析出白色沉淀CuNH4SO3,CuNH4SO3与足量的硫酸混合并微热,得到金属Cu等物质,本法制得的Cu呈超细粉末状,有重要用途。
①写出生成CuNH4SO3的反应方程式
②写出CuNH4SO3与H2SO4作用的反应方程式
③若反应在密闭容器中进行,且酸量充足,计算反应物中的Cu元素变成超细粉末Cu的转化率
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】人工合成的某固氮铁铂催化剂的组成分析方法如下:取一定量的样品加酸溶。解并调至pH为1.分成两份,第2份体积为第1份的两倍。第1份溶液以磺基水杨酸为指示剂,用EDTA标准溶液滴至终点,消耗24.40 mL。第2份先用沉淀法除去铁,用盐酸羟胺将Mo(VI)还原成Mo(V),然后加入25.00 mL EDTA标准溶液,充分反应后,加入一定体积pH 5.0的醋酸-醋酸钠缓冲溶液,以二甲酚橙为指示剂,用Zn2+标准溶液滴至终点,消耗22.12 mL。
(1)Zn2+标准溶液的配制:称取0.3289 g金属Zn,溶解后转移至250 mL的容量瓶,定容。EDTA溶液的标定:用移液管取25.00 mL上述Zn2+标准溶液,以二甲酚橙作指示剂,用EDTA标准溶液滴至终点,消耗20.24 mL。计算Zn2+标准溶液和EDTA标准溶液的浓度_____ 。
(2)实验误差用标准差表示。对n次测量结果作加减和乘除运算,运算结果(Q)的误差为ΔQ,其计算公式分别为ΔQ±=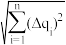 )和ΔQ×÷=|Q|
)和ΔQ×÷=|Q|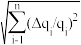 ,其中Δqi,为第i次测量值qi的误差。已知分析天平称量的标准差为0.1 mg,移液管、容量瓶和滴定管的标准差均为0.01 mL,忽略其他误差因素,计算
,其中Δqi,为第i次测量值qi的误差。已知分析天平称量的标准差为0.1 mg,移液管、容量瓶和滴定管的标准差均为0.01 mL,忽略其他误差因素,计算
①中EDTA标准溶液浓度的最小标准差____ 。
②请计算该催化剂中Fe和Mo的原子个数之比____ 。
③欲在室温下配制1.0 L pH 5.00的醋酸-醋酸钠缓冲溶液,现有11.8 g醋酸钠,请计算需要加入醋酸(ρ=1.05 g·mL-1)的体积_____ (醋酸在水溶液中的Ka=1.8× 10-5)。
(1)Zn2+标准溶液的配制:称取0.3289 g金属Zn,溶解后转移至250 mL的容量瓶,定容。EDTA溶液的标定:用移液管取25.00 mL上述Zn2+标准溶液,以二甲酚橙作指示剂,用EDTA标准溶液滴至终点,消耗20.24 mL。计算Zn2+标准溶液和EDTA标准溶液的浓度
(2)实验误差用标准差表示。对n次测量结果作加减和乘除运算,运算结果(Q)的误差为ΔQ,其计算公式分别为ΔQ±=
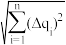 )和ΔQ×÷=|Q|
)和ΔQ×÷=|Q|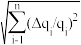 ,其中Δqi,为第i次测量值qi的误差。已知分析天平称量的标准差为0.1 mg,移液管、容量瓶和滴定管的标准差均为0.01 mL,忽略其他误差因素,计算
,其中Δqi,为第i次测量值qi的误差。已知分析天平称量的标准差为0.1 mg,移液管、容量瓶和滴定管的标准差均为0.01 mL,忽略其他误差因素,计算①中EDTA标准溶液浓度的最小标准差
②请计算该催化剂中Fe和Mo的原子个数之比
③欲在室温下配制1.0 L pH 5.00的醋酸-醋酸钠缓冲溶液,现有11.8 g醋酸钠,请计算需要加入醋酸(ρ=1.05 g·mL-1)的体积
您最近一年使用:0次




