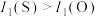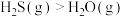根据相关化学原理,下列判断正确的是
| A.若X是原子晶体,Y是分子晶体,则熔点:X<Y |
| B.若A2+2D-→2A-+D2,则氧化性:D2>A2 |
| C.若R2-和M+的电子层结构相同,则原子序数:R>M |
| D.若弱酸HA的酸性强于弱酸HB,则同浓度钠盐溶液的碱性:NaA<NaB |
12-13高三上·浙江宁波·阶段练习 查看更多[2]
更新时间:2016-12-09 02:50:28
|
【知识点】 元素周期律的应用
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】四种短周期主族元素X、Y、Z、W原子序数依次增大,X、Y、Z在元素周期表中的位置如图所示,其中X和Y原子的最外层电子数之和为8,W的最高正价和最低负价的代数和为6,下列说法正确的是
| X | ||
| Y | Z |
A.简单离子的半径大小: |
B.最高价氧化物对应水化物的酸性: |
C.X形成的氢化物可能含有 或 或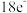 |
| D.工业上采用电解熔融的Y、W形成的化合物制备Y的单质 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,且四种元素的原子最外层电子数之和为24。下列说法错误的是
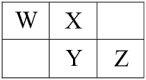
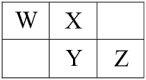
| A.原子半径大小顺序:W>X、Y>Z |
| B.X的最简单氢化物的稳定性强于Y的最简单氢化物 |
| C.W的气态氢化物与其最高价含氧酸反应生成盐 |
| D.在元素周期表中84号元素与Z位于同一主族 |
您最近半年使用:0次

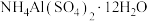 可用作净水剂.媒染剂等。下列说法正确的是
可用作净水剂.媒染剂等。下列说法正确的是