实验室制备叔丁基苯(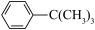 )的反应和有关数据如下:
)的反应和有关数据如下:
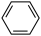 +ClC(CH3)3
+ClC(CH3)3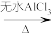
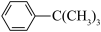 +HCl
+HCl
I.如图是实验室制备无水AlCl3可能需要的装置:
A.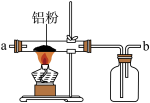 B.
B. 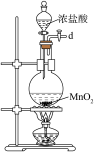 C.
C. 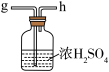 D.
D. 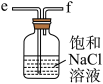 E.
E.  F.
F. 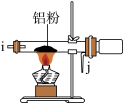
(1)检查B装置气密性的方法是__________ 。
(2)制备无水AlCl3的装置的合理的连接顺序为________ (填小写字母),其中E装置的作用是___________ 。
(3)实验时应先加热圆底烧瓶再加热硬质玻璃管,其原因是________ 。
II.如图是实验室制备叔丁基苯的装置(夹持装置略):
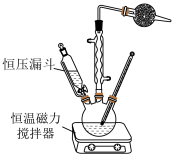
在三颈烧瓶中加入50mL的苯和适量的无水AlCl,由恒压漏斗滴加氯代叔丁烷10 mL,一定温度下反应一段时间后,将反应后的混合物洗涤分离,在所得产物中加入少量无水MgSO4固体,静置,过滤,蒸馏得叔丁基苯20 g。
使用恒压漏斗的优点是_________ ;加入无水MgSO4固体的作用是____________________________________ 。
(5)洗涤混合物时所用的试剂有如下三种,正确的使用顺序是__________ (填序号)
①5%的Na2CO3溶液 ②稀盐酸 ③H2O
(6)本实验中叔丁基苯的产率为______________ (保留3位有效数字)
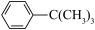 )的反应和有关数据如下:
)的反应和有关数据如下: +ClC(CH3)3
+ClC(CH3)3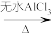
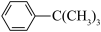 +HCl
+HCl| 物质 | 相对分子质量 | 密度/g∙cm-3 | 熔点/℃ | 沸点/℃ | 溶解性 |
| AlCl3 | —— | —— | 190 | 易升华 | 遇水极易潮解并产生白色烟雾,微溶于苯 |
| 苯 | 78 | 0.88 | —— | 80.1 | 难溶于水,易溶于乙醇 |
| 氯代叔丁烷 | 92.5 | 1.85 | —— | 51.6 | 难溶于水,可溶于苯 |
| 叔丁基苯 | 134 | 0.87 | —— | 169 | 难溶于水,易溶于苯 |
I.如图是实验室制备无水AlCl3可能需要的装置:
A.
 B.
B.  C.
C.  D.
D.  E.
E.  F.
F. 
(1)检查B装置气密性的方法是
(2)制备无水AlCl3的装置的合理的连接顺序为
(3)实验时应先加热圆底烧瓶再加热硬质玻璃管,其原因是
II.如图是实验室制备叔丁基苯的装置(夹持装置略):

在三颈烧瓶中加入50mL的苯和适量的无水AlCl,由恒压漏斗滴加氯代叔丁烷10 mL,一定温度下反应一段时间后,将反应后的混合物洗涤分离,在所得产物中加入少量无水MgSO4固体,静置,过滤,蒸馏得叔丁基苯20 g。
使用恒压漏斗的优点是
(5)洗涤混合物时所用的试剂有如下三种,正确的使用顺序是
①5%的Na2CO3溶液 ②稀盐酸 ③H2O
(6)本实验中叔丁基苯的产率为
更新时间:2020-03-06 09:08:24
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】有机化工中3,5-二甲氧基苯酚是重要的有机合成中间体,一种以间苯三酚为原料的合成反应如下:

甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见下表:
(1)1mol间苯三酚完全燃烧需要_____ molO2。
(2)反应结束后,先分离出甲醇,再加入乙醚进行萃取。
①分离出甲醇的操作是________ 。
②萃取用到的分液漏斗分液时有机层在分液漏斗的____ 填(“上”或“下”)层。
(3)分离得到的有机层依次用饱和NaHCO3溶液、少量蒸馏水进行洗涤。用饱和NaHCO3 溶液洗涤的目的是__________________________ ;
(4)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是_________ (填字母)。
a.蒸馏除去乙醚 b.冷却结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
(5)写出反应中可能出现的副产物结构简式______________ (只要写一种即可)。

甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见下表:
| 物质 | 沸点/℃ | 熔点/℃ | 密度(20℃) / g·cm-3 | 溶解性 |
| 甲醇 | 64. 7 |  | 0. 7915 | 易溶于水 |
| 乙醚 | 34. 5 |  | 0. 7138 | 微溶于水 |
| 3,5-二甲氧基苯酚 |  | 33 ~36 |  | 易溶于甲醇、乙醚,微溶于水 |
(2)反应结束后,先分离出甲醇,再加入乙醚进行萃取。
①分离出甲醇的操作是
②萃取用到的分液漏斗分液时有机层在分液漏斗的
(3)分离得到的有机层依次用饱和NaHCO3溶液、少量蒸馏水进行洗涤。用饱和NaHCO3 溶液洗涤的目的是
(4)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是
a.蒸馏除去乙醚 b.冷却结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
(5)写出反应中可能出现的副产物结构简式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】实验室用环己醇脱水的方法合成环己烯,该实验的装置如下图所示:
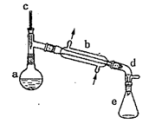
可能用到的有关数据如下:
按下列实验步骤回答问题:
Ⅰ.产物合成
在a中加入10.0g环己醇和2片碎瓷片,冷却搅拌下慢慢加入1mL浓硫酸,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度接近90℃。
(l)碎瓷片的作用是_______________________ ;b的名称是____________________ ;
(2)a中发生主要反应的化学方程式为_____________________________________ ;本实验最容易产生的有机副产物的结构简式为___________________ 。
Ⅱ.分离提纯
将反应粗产物倒入分液漏斗中,依次用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过操作X得到纯净的环己烯,称量,其质量为4.1g。
(3)用碳酸钠溶液洗涤的作用是________________ ,操作X的名称为_________________ 。
Ⅲ.产物分析及产率计算
(4)① 核磁共振氢谱可以帮助鉴定产物是否为环己烯,环己烯分子中有_______ 种不同化学环境的氢原子。
② 本实验所得环己烯的产率是______________ 。

可能用到的有关数据如下:
| 相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
按下列实验步骤回答问题:
Ⅰ.产物合成
在a中加入10.0g环己醇和2片碎瓷片,冷却搅拌下慢慢加入1mL浓硫酸,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度接近90℃。
(l)碎瓷片的作用是
(2)a中发生主要反应的化学方程式为
Ⅱ.分离提纯
将反应粗产物倒入分液漏斗中,依次用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过操作X得到纯净的环己烯,称量,其质量为4.1g。
(3)用碳酸钠溶液洗涤的作用是
Ⅲ.产物分析及产率计算
(4)① 核磁共振氢谱可以帮助鉴定产物是否为环己烯,环己烯分子中有
② 本实验所得环己烯的产率是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯。
已知:
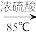
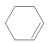 +H2O
+H2O

(1)制备粗品
将12.5 mL环己醇加入试管A中,再加入1 mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是___________ ,导管B除了导气外还具有的作用是___________ 。
②试管C置于冰水浴中的目的是___________ 。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在_____ 层(填“上”或“下”),分液后用______ (填编号)洗涤。
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按如图装置蒸馏,冷却水从g口进入。蒸馏时要加入生石灰,目的是___________ 。

(3)以下区分环己烯精品和粗品的方法,合理的是___________ 。
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点
已知:

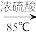
 +H2O
+H2O| 密度(g·cm-3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |

(1)制备粗品
将12.5 mL环己醇加入试管A中,再加入1 mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是
②试管C置于冰水浴中的目的是
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按如图装置蒸馏,冷却水从g口进入。蒸馏时要加入生石灰,目的是

(3)以下区分环己烯精品和粗品的方法,合理的是
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
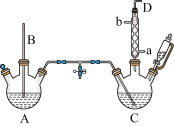
【推荐1】氯苯的合成工艺分为液相法和气相法两种,实验室模拟液相法的装置如下图(其中夹持仪器、加热装置及尾气处理装置已略去),有关物质的性质如表所示
(1)A反应器是利用实验室法制取氯气,装置中中空导管B的作用是_______________ 。
(2)把干燥的氯气通入装有50.0mL干燥苯、少量铁屑的三颈烧瓶C中制备氯苯,写出本方法制备氯苯的化学方程式。_______________ 。
(3)C的反应温度不宜过高,原因为①温度过高,反应得到二氯苯;②_______________ ,D出口的主要尾气成分有___________________ 。
(4)提纯粗产品过程如下:_____________ 。
(5)实验中最终得到产品22.5mL,产率为______________ 。
(6)气相法制氯苯是将空气、氯化氢气体混合物与苯在温度为210℃,迪肯型催化剂(CuCl2、FeCl3附在三氧化铝上)存在下进行氯化,发生反应生成氯苯。其反应方程式为:_______________ 。
| 名称 | 相对分子质量 | 沸点/(℃) | 密度/(g/mL) |
| 苯 | 78 | 78 | 0.88 |
| 氯苯 | 112.5 | 132.2 | 1.1 |
| 邻二氯苯 | 147 | 180.4 | 1.3 |
(1)A反应器是利用实验室法制取氯气,装置中中空导管B的作用是
(2)把干燥的氯气通入装有50.0mL干燥苯、少量铁屑的三颈烧瓶C中制备氯苯,写出本方法制备氯苯的化学方程式。
(3)C的反应温度不宜过高,原因为①温度过高,反应得到二氯苯;②
(4)提纯粗产品过程如下:

(5)实验中最终得到产品22.5mL,产率为
(6)气相法制氯苯是将空气、氯化氢气体混合物与苯在温度为210℃,迪肯型催化剂(CuCl2、FeCl3附在三氧化铝上)存在下进行氯化,发生反应生成氯苯。其反应方程式为:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】醇与氢卤酸反应是制备卤代烃的重要方法。实验室中制备溴乙烷(C2H5Br)通常采用以下方法:在烧瓶中加NaBr(约2-3g)、适量水和少量乙醇,再加两倍于乙醇体积的浓硫酸(1:1),塞上带有长导管的塞子,长导管的另一端插入装有冰水混合物的试管中,用酒精灯隔石棉网对反应物加热(如图所示)。用此装置也可制备一些其它的卤代烃,如:1-溴丁烷等。可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br-被浓硫酸氧化为Br2等。有关数据列表如下,请回答下列问题:

(1)写出该方法制备溴乙烷(C2H5Br)的化学方程式_____
(2)图中的试管放入冰水混合物的目的是_____ 。
(3)制备操作中,加入的浓硫酸必需进行稀释,目的是_____ 。
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂
(4)欲除去溴代烷中的少量杂质Br2,下列物质中最适合的是_____ (填字母)。
a.NaI b.NaOH c.NaHSO3 d.KCl
(5)在制备溴乙烷时,采用边反应边蒸出产物的方法,其有利于_____ ;但在制备1-溴丁烷时却不能边反应边蒸出产物,其原因是_____ 。

| 乙醇 | 溴乙烷 | 正丁醇 | 1-溴丁烷 | |
| 密度/g∙cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
| 沸点/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
(1)写出该方法制备溴乙烷(C2H5Br)的化学方程式
(2)图中的试管放入冰水混合物的目的是
(3)制备操作中,加入的浓硫酸必需进行稀释,目的是
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂
(4)欲除去溴代烷中的少量杂质Br2,下列物质中最适合的是
a.NaI b.NaOH c.NaHSO3 d.KCl
(5)在制备溴乙烷时,采用边反应边蒸出产物的方法,其有利于
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某实验小组用如图所示装置制取溴苯和溴乙烷。已知溴乙烷为无色液体,难溶于水,沸点为38.4℃,熔点为-119℃,密度为1.46g·cm-3。
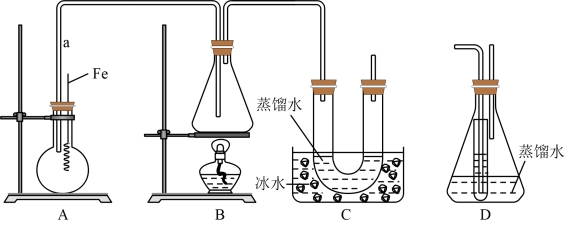
主要实验步骤如下:
①检查装置的气密性后,向烧瓶中加入一定量的苯和液溴。
②向B处锥形瓶中加入乙醇和浓H2SO4的混合液至浸没导管口。
③将A装置中的纯铁丝小心向下插入泥合液中。
④点燃B装置中的酒精灯,用小火缓缓对锥形瓶加热10 min。
请填写下列空白:
(1)A中导管的作用___________ 和导气。
(2)B装置中的主要化学方程式为___________ 。
(3)C装置中U形管内部用蒸馏水封住管底的作用是___________ 。
(4)步骤④中不能用大火加热,理由是___________ 。
(5)为证明溴和苯的上述反应是取代反应而不是加成反应,该同学用装置D代替装置B、C直接与A相连重新操作实验。
①D中小试管内CCl4作用___________ ;
②锥形瓶内装有水,反应后向锥形瓶内的水中滴加硝酸银溶液,若有___________ 产生,证明该反应属于取代反应。

主要实验步骤如下:
①检查装置的气密性后,向烧瓶中加入一定量的苯和液溴。
②向B处锥形瓶中加入乙醇和浓H2SO4的混合液至浸没导管口。
③将A装置中的纯铁丝小心向下插入泥合液中。
④点燃B装置中的酒精灯,用小火缓缓对锥形瓶加热10 min。
请填写下列空白:
(1)A中导管的作用
(2)B装置中的主要化学方程式为
(3)C装置中U形管内部用蒸馏水封住管底的作用是
(4)步骤④中不能用大火加热,理由是
(5)为证明溴和苯的上述反应是取代反应而不是加成反应,该同学用装置D代替装置B、C直接与A相连重新操作实验。
①D中小试管内CCl4作用
②锥形瓶内装有水,反应后向锥形瓶内的水中滴加硝酸银溶液,若有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】铁的化合物有广泛用途。
Ⅰ.用工业废渣(主要含有 、
、 、
、 及少量
及少量 )制备绿矾
)制备绿矾 晶体的流程如下:
晶体的流程如下:

(1)“浸泡”前将工业废渣粉碎的目的___________ 。
(2)已知: 属于两性氧化物,可以与
属于两性氧化物,可以与 等强碱反应生成
等强碱反应生成 。则上述浸泡过程中
。则上述浸泡过程中 与
与 溶液反应的离子方程式为
溶液反应的离子方程式为___________ 。
(3)“一系列操作”主要为___________ 、___________ 、过滤、洗涤、干燥。
Ⅱ.以 为原料生产氧化铁的步骤如下(部分操作和条件略):
为原料生产氧化铁的步骤如下(部分操作和条件略):
①将 配成溶液。
配成溶液。
② 溶液与稍过量的
溶液与稍过量的 溶液混合,得到含FeCO3的浊液。
溶液混合,得到含FeCO3的浊液。
③将浊液过滤,用 热水洗涤沉淀,干燥后得到固体。
热水洗涤沉淀,干燥后得到固体。
④煅烧,得到 固体。
固体。
(4)步骤②反应中,产物有 和
和 等,该反应的离子方程式为
等,该反应的离子方程式为___________ 。
(5)步骤③中,过滤、洗涤,通过检验 来判断沉淀是否洗涤干净。检验
来判断沉淀是否洗涤干净。检验 的操作是:取最后一次洗出液,先加入足量稀盐酸,再加入
的操作是:取最后一次洗出液,先加入足量稀盐酸,再加入___________ (填化学式)溶液,若无白色沉淀生成,证明已经洗涤干净。
(6)已知煅烧FeCO3的化学方程式是 ,现煅烧116.0kg的FeCO3,得到79.2kg产品。若产品中杂质只有
,现煅烧116.0kg的FeCO3,得到79.2kg产品。若产品中杂质只有 ,则该产品中
,则该产品中 的质量是
的质量是___________  。
。
Ⅰ.用工业废渣(主要含有
 、
、 、
、 及少量
及少量 )制备绿矾
)制备绿矾 晶体的流程如下:
晶体的流程如下:
(1)“浸泡”前将工业废渣粉碎的目的
(2)已知:
 属于两性氧化物,可以与
属于两性氧化物,可以与 等强碱反应生成
等强碱反应生成 。则上述浸泡过程中
。则上述浸泡过程中 与
与 溶液反应的离子方程式为
溶液反应的离子方程式为(3)“一系列操作”主要为
Ⅱ.以
 为原料生产氧化铁的步骤如下(部分操作和条件略):
为原料生产氧化铁的步骤如下(部分操作和条件略):①将
 配成溶液。
配成溶液。②
 溶液与稍过量的
溶液与稍过量的 溶液混合,得到含FeCO3的浊液。
溶液混合,得到含FeCO3的浊液。③将浊液过滤,用
 热水洗涤沉淀,干燥后得到固体。
热水洗涤沉淀,干燥后得到固体。④煅烧,得到
 固体。
固体。(4)步骤②反应中,产物有
 和
和 等,该反应的离子方程式为
等,该反应的离子方程式为(5)步骤③中,过滤、洗涤,通过检验
 来判断沉淀是否洗涤干净。检验
来判断沉淀是否洗涤干净。检验 的操作是:取最后一次洗出液,先加入足量稀盐酸,再加入
的操作是:取最后一次洗出液,先加入足量稀盐酸,再加入(6)已知煅烧FeCO3的化学方程式是
 ,现煅烧116.0kg的FeCO3,得到79.2kg产品。若产品中杂质只有
,现煅烧116.0kg的FeCO3,得到79.2kg产品。若产品中杂质只有 ,则该产品中
,则该产品中 的质量是
的质量是 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】硫代硫酸钠(Na2S2O3)在工业生产、医药制造业中被广泛应用,工业普遍使用Na2S2O3与硫黄(S)共煮得到,装置如图。(已知:Na2S2O3在酸性溶液中不能稳定存在,会发生歧化反应。)

(1)步骤1:打开K1、关闭K2,向圆底烧瓶中加入足量甲(浓硫酸)并加热,烧瓶中反应的化学方程式:Cu+2H2SO4(浓)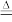 CuSO4+SO2↑+2H2O。生成物中,属于非电解质的是
CuSO4+SO2↑+2H2O。生成物中,属于非电解质的是___________ 。每生成0.5mol还原产物,消耗Cu的质量为___________ ,该过程中体现出浓硫酸___________ 的性质。
(2)步骤2:始终保持C中溶液呈碱性,反应一段时间后,硫粉的量逐渐减少,打开K2、关闭K1并停止加热。
①C中溶液须保持呈碱性,若呈酸性,则会发生___________ 和___________ (都用离子方程式表示)。
②装置B、D的试剂相同,均为___________ 。
步骤3:将C中所得混合物分离提纯后得产品。
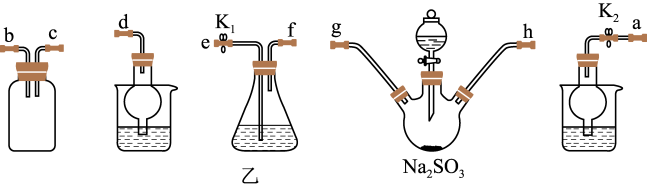
(3)利用反应2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2也能制备Na2S2O3。所需仪器见下图,按气流方向连接各仪器,接口顺序为a→g,h→___________ ,___________ →___________ ,___________ →d。
(4)Na2S2O3还原性强,工业上常用来除去溶液中残留的Cl2,往溶液中加入适量的Na2S2O3溶液,使其恰好与残留的Cl2完全反应,离子方程式为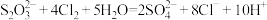 ,请设计实验方案,证明溶液中有Cl-
,请设计实验方案,证明溶液中有Cl-___________ 。

(1)步骤1:打开K1、关闭K2,向圆底烧瓶中加入足量甲(浓硫酸)并加热,烧瓶中反应的化学方程式:Cu+2H2SO4(浓)
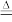 CuSO4+SO2↑+2H2O。生成物中,属于非电解质的是
CuSO4+SO2↑+2H2O。生成物中,属于非电解质的是(2)步骤2:始终保持C中溶液呈碱性,反应一段时间后,硫粉的量逐渐减少,打开K2、关闭K1并停止加热。
①C中溶液须保持呈碱性,若呈酸性,则会发生
②装置B、D的试剂相同,均为
步骤3:将C中所得混合物分离提纯后得产品。
(3)利用反应2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2也能制备Na2S2O3。所需仪器见下图,按气流方向连接各仪器,接口顺序为a→g,h→

(4)Na2S2O3还原性强,工业上常用来除去溶液中残留的Cl2,往溶液中加入适量的Na2S2O3溶液,使其恰好与残留的Cl2完全反应,离子方程式为
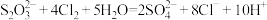 ,请设计实验方案,证明溶液中有Cl-
,请设计实验方案,证明溶液中有Cl-
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】冰晶石又名六氟铝酸钠(Na3AlF6),白色固体,微溶于水,常用作电解铝工业的助熔剂。工业上用萤石(主要成分是 CaF2)、浓硫酸、氢氧化铝和碳酸钠溶液通过湿法制备冰晶石,某化学实验小组模拟工业上制取 Na3AlF6 的装置图如图(该装置均由聚四氟乙烯仪器组装而成)。已知: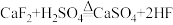 。
。

回答下列问题:
(1)实验仪器不能使用玻璃仪器的原因是________ (用化学方程式表示)。
(2)装置Ⅲ的作用为_________ 。
(3)在实验过程中,装置Ⅱ中有 CO2 气体逸出,同时观察到有白色固体析出,请写出该反应的离子方程式:________ 。
(4)在电解制铝的工业生产中,阳极的电极反应式为_________ 。
(5)萤石中含有少量的Fe2O3杂质,可用装置Ⅰ反应后的溶液来测定氟化钙的含量。具体操作如下:取8.0g萤石加入装置Ⅰ中,完全反应后,将混合液加水稀释,然后加入足量的KI 固体,再以淀粉为指示剂,用
 标准溶液滴定,达到滴定终点时,消耗
标准溶液滴定,达到滴定终点时,消耗 标准溶液40.00mL,则萤石中氟化钙的百分含量为
标准溶液40.00mL,则萤石中氟化钙的百分含量为_________ 。(已知: )
)
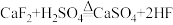 。
。
回答下列问题:
(1)实验仪器不能使用玻璃仪器的原因是
(2)装置Ⅲ的作用为
(3)在实验过程中,装置Ⅱ中有 CO2 气体逸出,同时观察到有白色固体析出,请写出该反应的离子方程式:
(4)在电解制铝的工业生产中,阳极的电极反应式为
(5)萤石中含有少量的Fe2O3杂质,可用装置Ⅰ反应后的溶液来测定氟化钙的含量。具体操作如下:取8.0g萤石加入装置Ⅰ中,完全反应后,将混合液加水稀释,然后加入足量的KI 固体,再以淀粉为指示剂,用

 标准溶液滴定,达到滴定终点时,消耗
标准溶液滴定,达到滴定终点时,消耗 标准溶液40.00mL,则萤石中氟化钙的百分含量为
标准溶液40.00mL,则萤石中氟化钙的百分含量为 )
)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】磺酰氯( )是一种重要的有机合成试剂,实验室可利用
)是一种重要的有机合成试剂,实验室可利用 与
与 在活性炭作用下反应制取少量的
在活性炭作用下反应制取少量的 ,装置如图所示(部分夹持装置省略),已知
,装置如图所示(部分夹持装置省略),已知 的熔点为-54.1℃,沸点为69.1℃,遇水能发生剧烈的水解反应,并产生白雾。
的熔点为-54.1℃,沸点为69.1℃,遇水能发生剧烈的水解反应,并产生白雾。

回答下列问题:
(1)装置乙和丁中可以使用同一种试剂,该试剂为_______ 。
(2)控制反应过程中装置丙中进气速率的方法是_______ ,实验结束时,关闭分液漏斗活塞和止水夹k,此时装置戊的作用是_______ 。
(3)氯磺酸(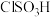 )加热分解,也能制得磺酰氯与另外一种物质,该反应的化学方程式为
)加热分解,也能制得磺酰氯与另外一种物质,该反应的化学方程式为___ 。
 )是一种重要的有机合成试剂,实验室可利用
)是一种重要的有机合成试剂,实验室可利用 与
与 在活性炭作用下反应制取少量的
在活性炭作用下反应制取少量的 ,装置如图所示(部分夹持装置省略),已知
,装置如图所示(部分夹持装置省略),已知 的熔点为-54.1℃,沸点为69.1℃,遇水能发生剧烈的水解反应,并产生白雾。
的熔点为-54.1℃,沸点为69.1℃,遇水能发生剧烈的水解反应,并产生白雾。
回答下列问题:
(1)装置乙和丁中可以使用同一种试剂,该试剂为
(2)控制反应过程中装置丙中进气速率的方法是
(3)氯磺酸(
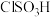 )加热分解,也能制得磺酰氯与另外一种物质,该反应的化学方程式为
)加热分解,也能制得磺酰氯与另外一种物质,该反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】二氧化氯气体常用于自来水消毒和果蔬保鲜等.目前较为广泛的制备 的原理是在酸性条件下,
的原理是在酸性条件下, 与
与 反应生成
反应生成 和
和 用下图装置(夹持装置略)对其制备、吸收、释放并对其氧化性依次进行研究。
用下图装置(夹持装置略)对其制备、吸收、释放并对其氧化性依次进行研究。 易溶于水但不与水反应,气体浓度较大时易分解(爆炸),实验室用稳定剂吸收
易溶于水但不与水反应,气体浓度较大时易分解(爆炸),实验室用稳定剂吸收 ,生成
,生成 ,使用时加酸只释放出
,使用时加酸只释放出 一种气体。
一种气体。
(1)仪器Ⅰ的名称为___________ ;
(2)对比仪器Ⅲ和Ⅳ,实验中Ⅲ的优点是___________ ;
(3)请写出甲中制备 的化学方程式
的化学方程式___________ ;
(4)根据实验原理和目的,上述装置的连接顺序为:ea__________ (填接口字母);
(5)不能用排空气法来收集得到纯净的 的原因是
的原因是___________ ;
(6)下列有关说法正确的是___________ ;
A.装置乙主要用于检验是否有 生成
生成
B.仪器e中 溶液主要用于停止反应,并吸收多余的
溶液主要用于停止反应,并吸收多余的
C. 和
和 都为强氧化剂,在相同条件下,等质量时,
都为强氧化剂,在相同条件下,等质量时, 的氧化能力是
的氧化能力是 的2.5倍
的2.5倍
(7)自来水厂用碘量法检测水中 的浓度,其实验操作如下:取
的浓度,其实验操作如下:取 的水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。再用
的水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。再用
 标准溶液滴定碘单质(
标准溶液滴定碘单质( ),达到滴.定终点时用去
),达到滴.定终点时用去
 标准溶液,测得该水样中
标准溶液,测得该水样中 的含量为
的含量为________ mg/L。
 的原理是在酸性条件下,
的原理是在酸性条件下, 与
与 反应生成
反应生成 和
和 用下图装置(夹持装置略)对其制备、吸收、释放并对其氧化性依次进行研究。
用下图装置(夹持装置略)对其制备、吸收、释放并对其氧化性依次进行研究。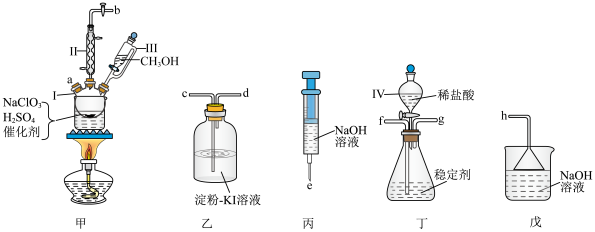
 易溶于水但不与水反应,气体浓度较大时易分解(爆炸),实验室用稳定剂吸收
易溶于水但不与水反应,气体浓度较大时易分解(爆炸),实验室用稳定剂吸收 ,生成
,生成 ,使用时加酸只释放出
,使用时加酸只释放出 一种气体。
一种气体。(1)仪器Ⅰ的名称为
(2)对比仪器Ⅲ和Ⅳ,实验中Ⅲ的优点是
(3)请写出甲中制备
 的化学方程式
的化学方程式(4)根据实验原理和目的,上述装置的连接顺序为:ea
(5)不能用排空气法来收集得到纯净的
 的原因是
的原因是(6)下列有关说法正确的是
A.装置乙主要用于检验是否有
 生成
生成B.仪器e中
 溶液主要用于停止反应,并吸收多余的
溶液主要用于停止反应,并吸收多余的
C.
 和
和 都为强氧化剂,在相同条件下,等质量时,
都为强氧化剂,在相同条件下,等质量时, 的氧化能力是
的氧化能力是 的2.5倍
的2.5倍(7)自来水厂用碘量法检测水中
 的浓度,其实验操作如下:取
的浓度,其实验操作如下:取 的水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。再用
的水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。再用
 标准溶液滴定碘单质(
标准溶液滴定碘单质( ),达到滴.定终点时用去
),达到滴.定终点时用去
 标准溶液,测得该水样中
标准溶液,测得该水样中 的含量为
的含量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学兴趣小组用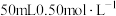 盐酸与
盐酸与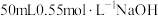 溶液进行中和反应反应热的测定实验,实验装置如图所示。试回答下列问题:
溶液进行中和反应反应热的测定实验,实验装置如图所示。试回答下列问题:

(1)实验时玻璃搅拌器的使用方法是___________ ;不能用铜质搅拌器代替玻璃搅拌器的理由是___________ 。
(2)NaOH溶液稍过量的原因是___________ 。
(3)某同学记录的实验数据如表所示。(已知:实验中盐酸和氢氧化钠溶液的密度均为 ,中和反应后溶液的比热容
,中和反应后溶液的比热容 )
)
依据该同学的实验数据计算,该实验测得反应放出的热量为___________ J。
(4)下列操作会导致实验结果出现偏差的是___________ (填字母)。
a.用量筒量取盐酸的体积时仰视读数
b.把量筒中的氢氧化钠溶液分多次倒入盐酸中
c.将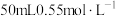 氢氧化钠溶液取成了
氢氧化钠溶液取成了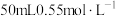 氢氧化钾溶液
氢氧化钾溶液
d.做本实验的当天室温较高
(5)如果将NaOH溶液换成等量的NaOH固体,那么实验中测得的中和反应反应热( )
)___________ (填“偏大”、“偏小”或“不变”)。
(6)如果用 盐酸与
盐酸与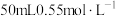 溶液进行实验,与上述实验相比,二者所放出的热量
溶液进行实验,与上述实验相比,二者所放出的热量___________ (填“相等”或“不相等”,下同),所求的中和反应反应热( )
)___________
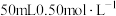 盐酸与
盐酸与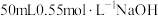 溶液进行中和反应反应热的测定实验,实验装置如图所示。试回答下列问题:
溶液进行中和反应反应热的测定实验,实验装置如图所示。试回答下列问题:
(1)实验时玻璃搅拌器的使用方法是
(2)NaOH溶液稍过量的原因是
(3)某同学记录的实验数据如表所示。(已知:实验中盐酸和氢氧化钠溶液的密度均为
 ,中和反应后溶液的比热容
,中和反应后溶液的比热容 )
)| 实验序号 | 起始温度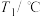 | 终止温度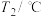 | |
| 盐酸 | 氢氧化钠溶液 | 混合溶液 | |
| 1 | 20.0 | 20.2 | 23.3 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.4 | 20.6 | 23.8 |
(4)下列操作会导致实验结果出现偏差的是
a.用量筒量取盐酸的体积时仰视读数
b.把量筒中的氢氧化钠溶液分多次倒入盐酸中
c.将
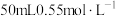 氢氧化钠溶液取成了
氢氧化钠溶液取成了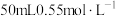 氢氧化钾溶液
氢氧化钾溶液d.做本实验的当天室温较高
(5)如果将NaOH溶液换成等量的NaOH固体,那么实验中测得的中和反应反应热(
 )
)(6)如果用
 盐酸与
盐酸与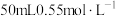 溶液进行实验,与上述实验相比,二者所放出的热量
溶液进行实验,与上述实验相比,二者所放出的热量 )
)
您最近一年使用:0次



