标号为①-⑩的元素,在元素周期表中的位置如下:
试回答下列问题:
(1)②号元素是______  填元素符号
填元素符号 ,⑨号元素的离子结构示意图为
,⑨号元素的离子结构示意图为______
(2)由①-⑩号元素组成的阴阳离子均为10电子的物质的化学式______ 、______  任写两种
任写两种 。
。
(3)用电子式表示①④号元素形成的最简单化合物的形成过程______
(4)③的最高价氧化物与⑧的单质在点燃条件下发生反应的化学方程式______
(5)①、⑤、⑦号元素形成的化合物的电子式是______ ,该化合物所含化学键的类型为______
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
1 | ① | ② | ||||||
2 | ③ | ④ | ⑤ | ⑥ | ||||
3 | ⑦ | ⑧ | ⑨ | ⑩ |
(1)②号元素是
 填元素符号
填元素符号 ,⑨号元素的离子结构示意图为
,⑨号元素的离子结构示意图为(2)由①-⑩号元素组成的阴阳离子均为10电子的物质的化学式
 任写两种
任写两种 。
。(3)用电子式表示①④号元素形成的最简单化合物的形成过程
(4)③的最高价氧化物与⑧的单质在点燃条件下发生反应的化学方程式
(5)①、⑤、⑦号元素形成的化合物的电子式是
更新时间:2020-03-13 11:40:26
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】部分短周期元素的性质或原子结构如表:
回答下列问题:
(1)X在元素周期表的位置____ ,画出W简单离子的结构示意图____ 。
(2)Y与Z按1:1形成的化合物的电子式为____ 。
(3)某同学设计了如图装置来探究碳、X、W元素的得电子能力。

①B中反应的化学方程式为____ ,能否说明得电子能力:W>碳,____ (填“能”或“否”),理由为____ 。
②C中足量酸性KMnO4溶液的作用是____ 。
③D装置可证明得电子能力:碳>X,D中试剂为____ ,实验现象为____ 。
| 元素编号 | 元素的性质或原子结构 |
| X | 其单质常用于计算机芯片 |
| Y | 最外层电子数为电子层数的3倍 |
| Z | 短周期失电子能力最强的元素 |
| W | L层比M多2个电子 |
| T | 第3周期元素的简单离子的半径最小 |
(1)X在元素周期表的位置
(2)Y与Z按1:1形成的化合物的电子式为
(3)某同学设计了如图装置来探究碳、X、W元素的得电子能力。

①B中反应的化学方程式为
②C中足量酸性KMnO4溶液的作用是
③D装置可证明得电子能力:碳>X,D中试剂为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】艾姆斯实验室已制造出包含钙、钾、铁和砷以及少量镍的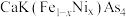 新型化合物材料,回答下列问题:
新型化合物材料,回答下列问题:
(1)化合物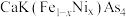 中的Fe属于元素周期表中
中的Fe属于元素周期表中___________ 区,基态Fe原子的原子结构示意图为___________ 。
(2)杀虫剂 中As原子采取
中As原子采取___________ 杂化。
(3) 基态价层电子排布式
基态价层电子排布式___________ 。
(4)在稀氨水介质中, 与丁二酮肟(分子式为
与丁二酮肟(分子式为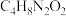 )反应可生成鲜红色沉淀,其分子结构如图所示,该分子中存在的化学键有)
)反应可生成鲜红色沉淀,其分子结构如图所示,该分子中存在的化学键有)___________ 。
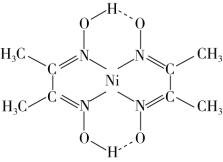
a.氢键 b. 键 c.
键 c. 键 d.配位键
键 d.配位键
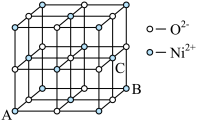
(5) 晶胞结构如下图所示,其中
晶胞结构如下图所示,其中 的配位数为
的配位数为___________ , 填入
填入 所形成的
所形成的___________ (填“四面体”或“八面体”)空隙中。
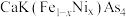 新型化合物材料,回答下列问题:
新型化合物材料,回答下列问题:(1)化合物
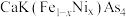 中的Fe属于元素周期表中
中的Fe属于元素周期表中(2)杀虫剂
 中As原子采取
中As原子采取(3)
 基态价层电子排布式
基态价层电子排布式(4)在稀氨水介质中,
 与丁二酮肟(分子式为
与丁二酮肟(分子式为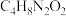 )反应可生成鲜红色沉淀,其分子结构如图所示,该分子中存在的化学键有)
)反应可生成鲜红色沉淀,其分子结构如图所示,该分子中存在的化学键有)
a.氢键 b.
 键 c.
键 c. 键 d.配位键
键 d.配位键(5)
 晶胞结构如下图所示,其中
晶胞结构如下图所示,其中 的配位数为
的配位数为 填入
填入 所形成的
所形成的
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知A、B、C、D、E均为中学化学中常见物质,在一定条件下相互转化关系如下图所示(反应条件和部分产物已省略)。
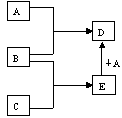
请回答:(1)若A为金属单质,B、C为非金属单质,且常温下B、C均为无色气体,D为黑色固体,则B的化学式为_________ ,A与E在一定条件下反应生成D的化学方程式为
_____________________________________________ 。
(2)若A为非金属单质,且常温下为黄绿色气体,B为金属单质,C为酸,且C的组成中含有与A相同的元素。则构成非金属单质A的元素原子结构示意图为___________ , A与E在一定条件下反应生成D的离子方程式为_____________________________________________ 。

请回答:(1)若A为金属单质,B、C为非金属单质,且常温下B、C均为无色气体,D为黑色固体,则B的化学式为
(2)若A为非金属单质,且常温下为黄绿色气体,B为金属单质,C为酸,且C的组成中含有与A相同的元素。则构成非金属单质A的元素原子结构示意图为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】I.高铁酸盐是一种新型、高效、多功能绿色水处理剂,工业上可用湿法制备高铁酸钾:2Fe(OH)3+3ClO-+4OH-=2FeO +3Cl-+5H2O。
+3Cl-+5H2O。
(1)FeO 中铁元素的化合价为
中铁元素的化合价为___________ ,在该反应中氧化剂与还原剂的物质的量之比为___________ 。
(2)请用单线桥表示反应中电子转移情况:___________ 。
(3)在下列反应中,水既不作氧化剂又不作还原剂是___________(填序号)。
II.为了庆祝元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。元素周期表反映了元素之间的内在联系,是学习、研究和应用化学的一种重要工具。下表是元素周期表的一部分,数字①~⑦代表前四周期七种主族元素。请按题目要求回答下列问题:___________ (填元素符号);它在周期表中的位置为___________ 。
(5)上述元素对应的单质中,既能与酸反应又能与碱反应的是___________ (填化学式),写出该单质与氢氧化钠反应的离子方程式___________ 。
 +3Cl-+5H2O。
+3Cl-+5H2O。(1)FeO
 中铁元素的化合价为
中铁元素的化合价为(2)请用单线桥表示反应中电子转移情况:
(3)在下列反应中,水既不作氧化剂又不作还原剂是___________(填序号)。
A.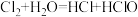 | B. |
C. | D. |
II.为了庆祝元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。元素周期表反映了元素之间的内在联系,是学习、研究和应用化学的一种重要工具。下表是元素周期表的一部分,数字①~⑦代表前四周期七种主族元素。请按题目要求回答下列问题:

(5)上述元素对应的单质中,既能与酸反应又能与碱反应的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下面是元素周期表的一部分,针对①—⑧元素填写下列空白)
(1)以上8种元素中化学性质最稳定的元素是______ (填元素符号)。
(2)⑤是第______ 周期第______ 主族
(3)元素⑥的最高价氧化物对应的水化物的化学式是______ 。
(4)①②④的半径由大到小的顺序为___________________
(5)元素⑦的最高化合价是______ 。
(6)元素④的单质在氧气中燃烧的化学方程式_______________
(7)元素⑤的最高价氧化物对应的水化物既能与强酸反应又能与强碱反应,请写出与NaOH溶液反应的离子方程式_______________ 。
族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
(2)⑤是第
(3)元素⑥的最高价氧化物对应的水化物的化学式是
(4)①②④的半径由大到小的顺序为
(5)元素⑦的最高化合价是
(6)元素④的单质在氧气中燃烧的化学方程式
(7)元素⑤的最高价氧化物对应的水化物既能与强酸反应又能与强碱反应,请写出与NaOH溶液反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下表为元素周期表的一部分,请参照元素①~⑦在表中的位置,回答下列问题:

(1)③的简单氢化物的结构式为__________ 。
(2)①、④、⑤三种元素组成化合物的电子式为__________ 。
(3)②、③、⑦的最高价氧化物对应的水化物酸性由强到弱的顺序是__________ (用化学式表示)。
(4)⑥的单质与NaOH溶液反应的离子方程式为__________ 。
(5)⑦的最简单氢化物是一种无色气体,遇到空气能发生爆炸性白燃,反应的化学方程式为__________ 。

(1)③的简单氢化物的结构式为
(2)①、④、⑤三种元素组成化合物的电子式为
(3)②、③、⑦的最高价氧化物对应的水化物酸性由强到弱的顺序是
(4)⑥的单质与NaOH溶液反应的离子方程式为
(5)⑦的最简单氢化物是一种无色气体,遇到空气能发生爆炸性白燃,反应的化学方程式为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐1】有机物A、B、C、D有如下转化关系。回答下列问题:

(1)乙烯的电子式为____________ ,分子中含有的共价键类型有________ (填极性键或非极性键)。
(2)写出反应的化学方程式和有机反应类型:
④__________________________________________ ,反应类型:________ 。
⑤__________________________________________ ,反应类型:________ 。

(1)乙烯的电子式为
(2)写出反应的化学方程式和有机反应类型:
④
⑤
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素:

(1)表中K元素在元素周期表中的位置为___________ 。
(2)基态Q原子的电子排布式为___________ 。基态Ⅰ原子简化电子排布式为___________ 。
(3)下列状态的F中,属于激发态原子的是___________(填标号)。
(4)基态 离子中未成对电子数为
离子中未成对电子数为___________ 。
(5)由C分别与P、B、G三种元素形成的二元化合物中,含离子键的是___________ (填化学式)。
(6)A和H的最高价氧化物对应的水化物酸性较强的是___________ (填化学式)。

(1)表中K元素在元素周期表中的位置为
(2)基态Q原子的电子排布式为
(3)下列状态的F中,属于激发态原子的是___________(填标号)。
A. | B. | C. | D.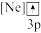 |
 离子中未成对电子数为
离子中未成对电子数为(5)由C分别与P、B、G三种元素形成的二元化合物中,含离子键的是
(6)A和H的最高价氧化物对应的水化物酸性较强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】A、B、C、D、E、F、G、H八种前四周期元素,原子序数依次增大,A、B、F三者原子序数之和为25,且知B、F同主族, 与G的气态氢化物的水溶液反应生成
与G的气态氢化物的水溶液反应生成 氢气
氢气 标准状况下
标准状况下 ,
,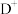 和E的离子具有相同的电子层结构,工业上用电解元素B和E能形成离子化合物的方法冶炼E单质,H元素常温下遇浓硫酸钝化,其一种核素质量数56,中子数30。试判断并回答下列问题:
和E的离子具有相同的电子层结构,工业上用电解元素B和E能形成离子化合物的方法冶炼E单质,H元素常温下遇浓硫酸钝化,其一种核素质量数56,中子数30。试判断并回答下列问题:
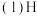 该元素在周期表中的位置
该元素在周期表中的位置__________ .
 由F、G二种元素形成化合物
由F、G二种元素形成化合物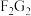 的电子式
的电子式______ ,含有化学键的类别为___________ .
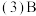 、C、F形成的最简单气态氢化物沸点由低到高的顺序依次为
、C、F形成的最简单气态氢化物沸点由低到高的顺序依次为________ 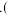 用化学式表示
用化学式表示
 由A、B、D、F四种元素可以组成两种盐,写出这两种盐反应的离子方程式
由A、B、D、F四种元素可以组成两种盐,写出这两种盐反应的离子方程式__________
 在碱性条件下,G的单质可与
在碱性条件下,G的单质可与 反应制备一种可用于净水的盐
反应制备一种可用于净水的盐 ,该反应的离子方程式是
,该反应的离子方程式是_______ .
 熔融盐燃料电池用熔融的碳酸盐作为电解质,负极充入燃料气
熔融盐燃料电池用熔融的碳酸盐作为电解质,负极充入燃料气 ,用空气与
,用空气与 的混合气作为正极的助燃气,以石墨为电极材料,制得燃料电池。写出充入
的混合气作为正极的助燃气,以石墨为电极材料,制得燃料电池。写出充入 的一极发生反应的电极反应式
的一极发生反应的电极反应式______ 。
 利用上述燃料电池,按图1所示装置进行电解,A、B、C、D均为铂电极,
利用上述燃料电池,按图1所示装置进行电解,A、B、C、D均为铂电极,
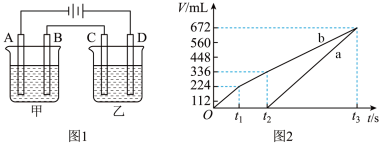
Ⅰ 甲槽电解的是
甲槽电解的是 一定浓度的NaCl与
一定浓度的NaCl与 的混合溶液,理论上两极所得气体的体积随时间变化的关系如图2所示
的混合溶液,理论上两极所得气体的体积随时间变化的关系如图2所示 气体体积已换算成标准状况下的体积,电解前后溶液的体积变化忽略不计
气体体积已换算成标准状况下的体积,电解前后溶液的体积变化忽略不计 。
。 的物质的量浓度为
的物质的量浓度为________  。
。
Ⅱ 乙槽为
乙槽为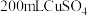 溶液,通电一段时间,当C极析出
溶液,通电一段时间,当C极析出 物质时停止通电,若使乙槽内的溶液完全复原,可向乙槽中加入
物质时停止通电,若使乙槽内的溶液完全复原,可向乙槽中加入________  填字母
填字母 。
。
A. B.
B. C.
C. D.
D.
 若通电一段时间后,向所得的乙槽溶液中加入
若通电一段时间后,向所得的乙槽溶液中加入 的
的 才能恰好恢复到电解前的浓度,则电解过程中转移的电子数为
才能恰好恢复到电解前的浓度,则电解过程中转移的电子数为________ 。
 与G的气态氢化物的水溶液反应生成
与G的气态氢化物的水溶液反应生成 氢气
氢气 标准状况下
标准状况下 ,
, 和E的离子具有相同的电子层结构,工业上用电解元素B和E能形成离子化合物的方法冶炼E单质,H元素常温下遇浓硫酸钝化,其一种核素质量数56,中子数30。试判断并回答下列问题:
和E的离子具有相同的电子层结构,工业上用电解元素B和E能形成离子化合物的方法冶炼E单质,H元素常温下遇浓硫酸钝化,其一种核素质量数56,中子数30。试判断并回答下列问题: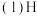 该元素在周期表中的位置
该元素在周期表中的位置 由F、G二种元素形成化合物
由F、G二种元素形成化合物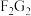 的电子式
的电子式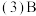 、C、F形成的最简单气态氢化物沸点由低到高的顺序依次为
、C、F形成的最简单气态氢化物沸点由低到高的顺序依次为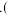 用化学式表示
用化学式表示
 由A、B、D、F四种元素可以组成两种盐,写出这两种盐反应的离子方程式
由A、B、D、F四种元素可以组成两种盐,写出这两种盐反应的离子方程式 在碱性条件下,G的单质可与
在碱性条件下,G的单质可与 反应制备一种可用于净水的盐
反应制备一种可用于净水的盐 ,该反应的离子方程式是
,该反应的离子方程式是 熔融盐燃料电池用熔融的碳酸盐作为电解质,负极充入燃料气
熔融盐燃料电池用熔融的碳酸盐作为电解质,负极充入燃料气 ,用空气与
,用空气与 的混合气作为正极的助燃气,以石墨为电极材料,制得燃料电池。写出充入
的混合气作为正极的助燃气,以石墨为电极材料,制得燃料电池。写出充入 的一极发生反应的电极反应式
的一极发生反应的电极反应式 利用上述燃料电池,按图1所示装置进行电解,A、B、C、D均为铂电极,
利用上述燃料电池,按图1所示装置进行电解,A、B、C、D均为铂电极,
Ⅰ
 甲槽电解的是
甲槽电解的是 一定浓度的NaCl与
一定浓度的NaCl与 的混合溶液,理论上两极所得气体的体积随时间变化的关系如图2所示
的混合溶液,理论上两极所得气体的体积随时间变化的关系如图2所示 气体体积已换算成标准状况下的体积,电解前后溶液的体积变化忽略不计
气体体积已换算成标准状况下的体积,电解前后溶液的体积变化忽略不计 。
。 的物质的量浓度为
的物质的量浓度为 。
。Ⅱ
 乙槽为
乙槽为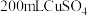 溶液,通电一段时间,当C极析出
溶液,通电一段时间,当C极析出 物质时停止通电,若使乙槽内的溶液完全复原,可向乙槽中加入
物质时停止通电,若使乙槽内的溶液完全复原,可向乙槽中加入 填字母
填字母 。
。A.
 B.
B. C.
C. D.
D.
 若通电一段时间后,向所得的乙槽溶液中加入
若通电一段时间后,向所得的乙槽溶液中加入 的
的 才能恰好恢复到电解前的浓度,则电解过程中转移的电子数为
才能恰好恢复到电解前的浓度,则电解过程中转移的电子数为
您最近一年使用:0次



