部分短周期元素的性质或原子结构如表:
回答下列问题:
(1)X在元素周期表的位置____ ,画出W简单离子的结构示意图____ 。
(2)Y与Z按1:1形成的化合物的电子式为____ 。
(3)某同学设计了如图装置来探究碳、X、W元素的得电子能力。

①B中反应的化学方程式为____ ,能否说明得电子能力:W>碳,____ (填“能”或“否”),理由为____ 。
②C中足量酸性KMnO4溶液的作用是____ 。
③D装置可证明得电子能力:碳>X,D中试剂为____ ,实验现象为____ 。
| 元素编号 | 元素的性质或原子结构 |
| X | 其单质常用于计算机芯片 |
| Y | 最外层电子数为电子层数的3倍 |
| Z | 短周期失电子能力最强的元素 |
| W | L层比M多2个电子 |
| T | 第3周期元素的简单离子的半径最小 |
(1)X在元素周期表的位置
(2)Y与Z按1:1形成的化合物的电子式为
(3)某同学设计了如图装置来探究碳、X、W元素的得电子能力。

①B中反应的化学方程式为
②C中足量酸性KMnO4溶液的作用是
③D装置可证明得电子能力:碳>X,D中试剂为
更新时间:2022-05-10 07:59:22
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题。
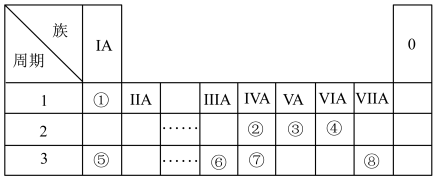
(1)①、②、③、④分别是_____ 、______ 、______ 、_____ (用元素符号表示)
(2)描述⑦、⑧在周期表中的位置:第___ 周期,第_____ 族、第___ 周期,第____ 族
(3)①、③、④、⑥元素中的两种元素可形成含10个电子的分子,它们是_____ 、_____
(4)写出⑤的原子结构示意图_____________
(5)⑧的单质与氢氧化钠溶液反应的离子方程式_______________

(1)①、②、③、④分别是
(2)描述⑦、⑧在周期表中的位置:第
(3)①、③、④、⑥元素中的两种元素可形成含10个电子的分子,它们是
(4)写出⑤的原子结构示意图
(5)⑧的单质与氢氧化钠溶液反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知X、Y、Z、R、W、Q六种元素中,X的原子序数为1;Y元素原子最外层电子数是内层电子总数的2倍;Z元素原子次外层电子数比其最外层电子数少4个;R元素原子最外层有1个电子,其阳离子与Z的阴离子原子核外电子总数相同;W元素原子K层和M层电子总数等于其L层电子数。请要求填空:
(1)Z元素形成的原子的结构示意图为___________ ;
(2)从前五种元素中选出三种元素组成化合物,其中属于碱的是___________ (填化学式);属于非电解质的是___________ (填一种物质的名称即可);
(3)现有标准状况下YZ和 混合气体8.96L,其质量为16g,则该气体中,YZ和
混合气体8.96L,其质量为16g,则该气体中,YZ和 的物质的量之比为
的物质的量之比为___________ ;
(4)55.0g化合物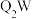 中含有
中含有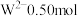 ,则Q的相对原子质量为
,则Q的相对原子质量为___________ ;
(5)将4.00gRZX溶于一定量水,所得溶液的体积为100mL,该溶液中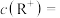
___________ ;
(6)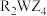 溶于水的电离方程式
溶于水的电离方程式___________ ;
(7)化合物 与
与 反应的化学方程式为
反应的化学方程式为___________ 。
(1)Z元素形成的原子的结构示意图为
(2)从前五种元素中选出三种元素组成化合物,其中属于碱的是
(3)现有标准状况下YZ和
 混合气体8.96L,其质量为16g,则该气体中,YZ和
混合气体8.96L,其质量为16g,则该气体中,YZ和 的物质的量之比为
的物质的量之比为(4)55.0g化合物
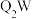 中含有
中含有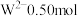 ,则Q的相对原子质量为
,则Q的相对原子质量为(5)将4.00gRZX溶于一定量水,所得溶液的体积为100mL,该溶液中
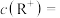
(6)
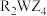 溶于水的电离方程式
溶于水的电离方程式(7)化合物
 与
与 反应的化学方程式为
反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E 5种元素,已知:
①A原子最外层电子数是次外层电子数的2倍,B的阴离子与C的阳离子跟氖原子的电子层结构相同。E原子M层上的电子比K层多5个。
②常温下B2是气体,它对氢气的相对密度是16。
③C的单质在B2中燃烧,生成淡黄色固体F。F与AB2反应可生成B2。
④D的单质在B2中燃烧,发出淡紫色火焰,生成有刺激性气味的气体DB2。DB2中D的质量分数为50%。根据以上情况回答:
(1)A是______ 、B是______ 、C是______ 、D是______ 、E是______ (写元素符号)。
(2)E的原子结构示意图__________ ,C的离子结构示意图__________ 。
(3)F和AB2反应的化学方程式________________________________________________ 。
①A原子最外层电子数是次外层电子数的2倍,B的阴离子与C的阳离子跟氖原子的电子层结构相同。E原子M层上的电子比K层多5个。
②常温下B2是气体,它对氢气的相对密度是16。
③C的单质在B2中燃烧,生成淡黄色固体F。F与AB2反应可生成B2。
④D的单质在B2中燃烧,发出淡紫色火焰,生成有刺激性气味的气体DB2。DB2中D的质量分数为50%。根据以上情况回答:
(1)A是
(2)E的原子结构示意图
(3)F和AB2反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】近年来,中国积极开展空间探索活动,“嫦娥”揽月、“天问”探火、“羲和”逐日、空间站巡天,不断深化人类对宇宙的认知,致力增进人类共同福祉。利用元素周期表认识和研究物质,可以助力我国科技的发展。

(1)液态a单质和液态c单质可用作火箭推进剂,二者反应的化学方程式为_______ 。
(2)嫦娥五号带回的月壤中含有e元素。e原子结构示意图为_______ 。
(3)我国自主研发了用于航空航天的f合金材料。d最高价氧化物对应的水化物溶液,与f最高价氧化物反应的离子方程式是_______ 。
(4)元素b广泛存在于大气和地壳和生物之中,由它组成的有机物更是生命的根本。在下图中相应位置写出3种含b元素物质的化学式(要求物质类别各不相同)。_________

(5)我国科学家发现土卫二星可能存在g元素。g氢化物的电子式为_______ ,该物质中含有的化学键类型为_______ (填“离子键”、“极性键”或“非极性键”)。

(1)液态a单质和液态c单质可用作火箭推进剂,二者反应的化学方程式为
(2)嫦娥五号带回的月壤中含有e元素。e原子结构示意图为
(3)我国自主研发了用于航空航天的f合金材料。d最高价氧化物对应的水化物溶液,与f最高价氧化物反应的离子方程式是
(4)元素b广泛存在于大气和地壳和生物之中,由它组成的有机物更是生命的根本。在下图中相应位置写出3种含b元素物质的化学式(要求物质类别各不相同)。

(5)我国科学家发现土卫二星可能存在g元素。g氢化物的电子式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】X、Y、L、M为核电荷数依次增大的前20号主族元素。X2是最轻的气体,Y、L与M三种元素的质子数均为5的倍数。回答下列问题:
(1)X与L组成的最简单化合物的电子式为_____ 。
(2)X与M组成的物质为_______ (填“共价”或“离子”)化合物,该物质可作为野外工作的应急燃料,其与水反应的化学方程式为______ 。
(3)Y的含氧酸的化学式为_____ 。其酸性来源不是本身电离出质子,而是能结合水分子电离的氢氧根离子,释放出质子,所以该酸为___ 元酸。
(4)L基态原子电子的最高能层符号为____ ,L的最高价含氧酸根离子的等电子体有__ 、__ (写出一个分子和一个离子)。
(1)X与L组成的最简单化合物的电子式为
(2)X与M组成的物质为
(3)Y的含氧酸的化学式为
(4)L基态原子电子的最高能层符号为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】短周期五种元素A、B、C、D、E的原子序数依次增大。A、B、C的单质在常温下都呈气态,C原子最外层电子数是电子层数的3倍,C和E位于同主族。D与A可以形成化合物DA2 。 A、B的单质依次为G、T,在密闭容器中充入一定量的G、T,一定条件下发生反应G+T→W(未配平),测得各物质的浓度如表所示。
回答下列问题:
(1)A、B、C能组成既含离子键又含共价键的化合物,则该化合物的化学式为___________ 。
(2)J、L是由A、B、C、E四种元素组成的两种酸式盐,J、L溶液混合可产生有刺激性气味的气体,写出这两种溶液发生反应的离子方程式:___________ ;J、L中能使酸性高锰酸钾溶液褪色的是___________ (填化学式)。
(3)B2A4—C2碱性燃料电池放电效率高。该电池放电时,负极反应式为___________ ,正极附近溶液的pH___________ (填“增大”“减小”或“不变”)。
(4)由上述五种元素中的四种组成的单质、化合物在一定条件下的转化关系(部分条件和产物已省略)如图所示:

①Y是___________ (填化学式);W的电子式为___________ 。
②B的最高价氧化物对应的水化物为Q,X与足量的Q溶液反应的化学方程式为___________ 。
| 物质 | T | G | W |
| 10 min时,c/(mol·L-1) | 0.5 | 0.8 | 0.2 |
| 20 min时,c/(mol·L-1) | 0.3 | 0.2 | 0.6 |
(1)A、B、C能组成既含离子键又含共价键的化合物,则该化合物的化学式为
(2)J、L是由A、B、C、E四种元素组成的两种酸式盐,J、L溶液混合可产生有刺激性气味的气体,写出这两种溶液发生反应的离子方程式:
(3)B2A4—C2碱性燃料电池放电效率高。该电池放电时,负极反应式为
(4)由上述五种元素中的四种组成的单质、化合物在一定条件下的转化关系(部分条件和产物已省略)如图所示:

①Y是
②B的最高价氧化物对应的水化物为Q,X与足量的Q溶液反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下表为元素周期表的一部分,请参照元素①~⑩在表中的位置,用化学用语回答下列问题:
(1)金属性最强的是_______ (填元素名称)。
(2)⑨的离子结构示意图为_______ 。
(3)⑤元素和⑩元素的最简单氢化物的稳定性由强到弱的关系是_______ (填化学式)。
(4)④、⑤、⑥的简单离子半径由大到小的顺序为_______ (用离子符号表示)。
(5)⑧、⑨、⑩最高价氧化物对应的水化物酸性由弱到强的顺序是_______ (填化学式)。
(6)用电子式表示④与⑥形成的原子个数比为1∶2的化合物的形成过程_______ 。
(7)⑦的最高价氧化物对应的水化物与⑥的最高价氧化物水化物的溶液发生反应,写出离子方程式_______ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | ⑤ | ||||
| 三 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||
(2)⑨的离子结构示意图为
(3)⑤元素和⑩元素的最简单氢化物的稳定性由强到弱的关系是
(4)④、⑤、⑥的简单离子半径由大到小的顺序为
(5)⑧、⑨、⑩最高价氧化物对应的水化物酸性由弱到强的顺序是
(6)用电子式表示④与⑥形成的原子个数比为1∶2的化合物的形成过程
(7)⑦的最高价氧化物对应的水化物与⑥的最高价氧化物水化物的溶液发生反应,写出离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A、B、C、D四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体 E,D的L层电子数等于 K、M两个电子层上的电子数之和。
(1)C离子的结构示意图为_______ 。D在周期表中位置 ______________ 。
(2)写出 E 的电子式:______________ 。
(3)A、D两元素形成的化合物属______________ (填“离子”或“共价”)化合物。
(4)写出D的最高价氧化物的水化物和A单质反应的化学方程式:_______ 。
(5)B原子与氢原子形成的粒子中,与NH3具有相同电子数的阴离子为__________ (填化学式),该阴离子的电子式为______________ 。
(6)用电子式表示C、D两元素形成化合物的过程_________ 。
(1)C离子的结构示意图为
(2)写出 E 的电子式:
(3)A、D两元素形成的化合物属
(4)写出D的最高价氧化物的水化物和A单质反应的化学方程式:
(5)B原子与氢原子形成的粒子中,与NH3具有相同电子数的阴离子为
(6)用电子式表示C、D两元素形成化合物的过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】W、X、Y、Z 是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知W的一种核素的质量数为18,中子数为10;X和Ne的核外电子数相差1;在Z所在的周期中,Z 元素的原子得电子能力最强;四种元素的最外层电子数之和为18。请回答下列问题:

(1)X元素位于元素周期表中位置为_______ 。
(2)X的单质和Y的单质相比,熔点较高的是_______ (写化学式)。Z所在族的简单氢化物中,沸点最高的是_________ (写化学式),原因为_________ 。
(3)W、X、Z三种元素形成的化合物中化学键类型为_______ ;X2W2的电子式为_______ 。
(4)Y与Z形成的化合物在常温下是一种液态,它和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式为_________ 。
(5)Z的氧化物很多,其中一种黄绿色气体M,其氧含量为47.41%,可用于水处理,M在液态和浓缩气态时具有爆炸性,则M的化学式为_________ 。M可与NaOH溶液反应生成两种稳定的盐,它们的物质的量之比为1︰5,该反应的化学方程式为_________ 。

(1)X元素位于元素周期表中位置为
(2)X的单质和Y的单质相比,熔点较高的是
(3)W、X、Z三种元素形成的化合物中化学键类型为
(4)Y与Z形成的化合物在常温下是一种液态,它和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式为
(5)Z的氧化物很多,其中一种黄绿色气体M,其氧含量为47.41%,可用于水处理,M在液态和浓缩气态时具有爆炸性,则M的化学式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某学习小组研究溶液中Fe2+的稳定性;进行如下实验,观察,记录结果。
实验I

(1)上述(NH4)2Fe(SO4)2溶液pH小于FeSO4的原因是_____________ (用化学用语表示)。溶液的稳定性:FeSO4_______ (NH4)2Fe(SO4)2(填“>”或“<”)。
(2)甲同学提出实验I中两溶液的稳定性差异可能是(NH4)2Fe(SO4)2溶液中的NH4+保护了Fe2+,因为NH4+有还原性,进行实验Ⅱ,否定了该观点,补全该实验_______ 。

(3)乙同学提出实验I中两溶液的稳定性差异是溶液酸性不同导致,进行实验Ⅲ;分别配制0.80mol•L-1pH为1、2、3、4的FeSO4溶液,发现pH=1的FeSO4溶液长时间无明显变化,pH越大,FeSO4溶液变黄的时间越短。
资料显示:亚铁盐溶液中存在反应 4Fe2++O2+10H2O 4Fe(OH)3+8H+由实验Ⅲ,乙同学可得出的结论是
4Fe(OH)3+8H+由实验Ⅲ,乙同学可得出的结论是_________ ,原因是_________ 。
(4)进一步研究在水溶液中Fe2+的氧化机理,测定同浓度FeSO4溶液在不同pH条件下,Fe2+的氧化速率与时间的关系如图(实验过程中溶液温度几乎无变化)。反应初期,氧化速率逐渐增大的原因可能是_________ 。

(5)综合以上实验,增强Fe2+稳定性的措施有_________ 。
实验I

(1)上述(NH4)2Fe(SO4)2溶液pH小于FeSO4的原因是
(2)甲同学提出实验I中两溶液的稳定性差异可能是(NH4)2Fe(SO4)2溶液中的NH4+保护了Fe2+,因为NH4+有还原性,进行实验Ⅱ,否定了该观点,补全该实验

(3)乙同学提出实验I中两溶液的稳定性差异是溶液酸性不同导致,进行实验Ⅲ;分别配制0.80mol•L-1pH为1、2、3、4的FeSO4溶液,发现pH=1的FeSO4溶液长时间无明显变化,pH越大,FeSO4溶液变黄的时间越短。
资料显示:亚铁盐溶液中存在反应 4Fe2++O2+10H2O
 4Fe(OH)3+8H+由实验Ⅲ,乙同学可得出的结论是
4Fe(OH)3+8H+由实验Ⅲ,乙同学可得出的结论是(4)进一步研究在水溶液中Fe2+的氧化机理,测定同浓度FeSO4溶液在不同pH条件下,Fe2+的氧化速率与时间的关系如图(实验过程中溶液温度几乎无变化)。反应初期,氧化速率逐渐增大的原因可能是

(5)综合以上实验,增强Fe2+稳定性的措施有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】(1)下图为实验室制备、收集少量HCl的装置。

① 制备HCl所用药品为浓硫酸和浓盐酸,则甲的最佳装置应选用下图中的_______ 。
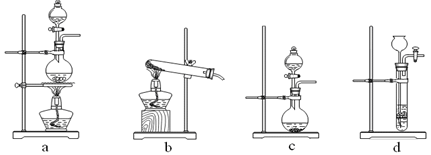
② 请解释能用浓硫酸和浓盐酸制备HCl气体的原因__________________________________ 。
③ 装置丙用来吸收过量的HCl气体,为防止倒吸,则烧杯中应该装入水和______________ 。
(2)以下为苯的取代反应的探究实验。
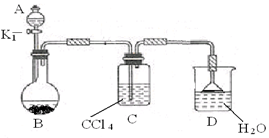
①按上图所示的装置图连接好各仪器。
②检验装置的气密性。
③在A中加入适量的苯和液溴的混合液体,在B中加入少量铁粉,塞上橡皮塞,打开K1,开始进行反应,放入适量混合液后,关闭K1。
写出B中发生反应的化学方程式___________________ 。装置C的作用是__________________ 。
④反应结束后,用试管取少量D中的溶液,加入___________________________
(描述试剂和现象),则证明B中的取代反应已经发生。
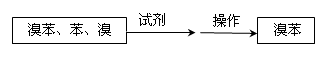
⑤把B中的固液混合物体过滤,分离出液体混合物,按下图方案精制含有苯和溴的溴苯。其中试剂为_________ ,操作名称为__________ 。

① 制备HCl所用药品为浓硫酸和浓盐酸,则甲的最佳装置应选用下图中的

② 请解释能用浓硫酸和浓盐酸制备HCl气体的原因
③ 装置丙用来吸收过量的HCl气体,为防止倒吸,则烧杯中应该装入水和
(2)以下为苯的取代反应的探究实验。

①按上图所示的装置图连接好各仪器。
②检验装置的气密性。
③在A中加入适量的苯和液溴的混合液体,在B中加入少量铁粉,塞上橡皮塞,打开K1,开始进行反应,放入适量混合液后,关闭K1。
写出B中发生反应的化学方程式
④反应结束后,用试管取少量D中的溶液,加入
(描述试剂和现象),则证明B中的取代反应已经发生。
⑤把B中的固液混合物体过滤,分离出液体混合物,按下图方案精制含有苯和溴的溴苯。其中试剂为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】已知草酸(H2C2O4)是一种二元弱酸,草酸及其盐广泛用于医药、印染、塑料等工业。
(1)已知25℃时,几种常见弱酸的Ka如下表所示:
①25℃时,浓度均为0.1mol·L-1的Na2C2O4、CH3COONa、NaCN、Na2CO3的pH由大到小的顺序是___ 。中和等体积、等pH的HCOOH和HCN消耗NaOH的量___ (填“前者大”“后者大”或“相等”)。
②下列关于0.1mol·L-1NaHC2O4溶液的说法正确的是___ 。
a.HC2O4-的电离程度大于水解程度,溶液显酸性
b.HC2O4-的水解程度大于电离程度程度,溶液显碱性
c.溶液中c(Na+)+c(H+)=c(HC2O4-)+c(OH-)+c(C2O42-)
d.溶液中c(H+)=c(OH-)+c(C2O42-)-c(H2C2O4)
(2)在t℃时,MgC2O4在水中的沉淀溶解平衡曲线如图1所示。又知t℃时Mg(OH)2的Ksp=5.6×10-12,下列说法不正确的是____

A.在t℃时,MgC2O4的Ksp=8.1×10-5mol2·L-2
B.在MgC2O4饱和溶液中加入Na2CO3固体,可使溶液由c点到b点
C.图中a点对应的是MgC2O4的不饱和溶液
D.在t℃时,MgC2O4(s)+2OH-(aq)⇌Mg(OH)2(s)+C2O42-(aq)平衡常数K=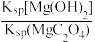
(3)草酸亚铁晶体(FeC2O4·2H2O)是一种浅黄色固体,难溶于水,受热易分解。某化学兴趣小组设计实验验证草酸亚铁晶体热分解的产物,探究过程如图2:
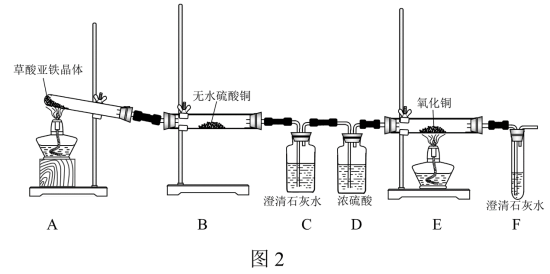
①从环保角度考虑,该套实验装置的明显缺陷是___ 。
②该兴趣小组进行上述实验时,从实验安全角度考虑,应先点燃___ (填“A”或“E”)处的酒精灯。
③若实验过程中观察到B中白色无水CuSO4变成蓝色,___ (补充实验现象),则可证明草酸亚铁晶体热分解的气体产物是H2O、CO和CO2。
④为探究草酸亚铁晶体分解的固体产物,兴趣小组同学准确称取3.60g草酸亚铁晶体(FeC2O4·2H2O),相对分子质量是180),充分加热,使其完全分解,冷却后称得剩余固体的质量为1.60g。若剩余固体只有一种铁的氧化物,通过计算确定该氧化物的化学式为___ 。草酸亚铁晶体分解的化学方程式为___ 。
(1)已知25℃时,几种常见弱酸的Ka如下表所示:
| 电解质 | H2C2O4 | CH3COOH | HCN | H2CO3 |
| 电离常数(mol·L-1) | K1=5.6×10-2 K2=5.4×10-3 | K1=1.7×10-5 | K2=6.2×10-10 | K1=4.2×10-7 K2=5.6×10-11 |
②下列关于0.1mol·L-1NaHC2O4溶液的说法正确的是
a.HC2O4-的电离程度大于水解程度,溶液显酸性
b.HC2O4-的水解程度大于电离程度程度,溶液显碱性
c.溶液中c(Na+)+c(H+)=c(HC2O4-)+c(OH-)+c(C2O42-)
d.溶液中c(H+)=c(OH-)+c(C2O42-)-c(H2C2O4)
(2)在t℃时,MgC2O4在水中的沉淀溶解平衡曲线如图1所示。又知t℃时Mg(OH)2的Ksp=5.6×10-12,下列说法不正确的是

A.在t℃时,MgC2O4的Ksp=8.1×10-5mol2·L-2
B.在MgC2O4饱和溶液中加入Na2CO3固体,可使溶液由c点到b点
C.图中a点对应的是MgC2O4的不饱和溶液
D.在t℃时,MgC2O4(s)+2OH-(aq)⇌Mg(OH)2(s)+C2O42-(aq)平衡常数K=
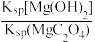
(3)草酸亚铁晶体(FeC2O4·2H2O)是一种浅黄色固体,难溶于水,受热易分解。某化学兴趣小组设计实验验证草酸亚铁晶体热分解的产物,探究过程如图2:

①从环保角度考虑,该套实验装置的明显缺陷是
②该兴趣小组进行上述实验时,从实验安全角度考虑,应先点燃
③若实验过程中观察到B中白色无水CuSO4变成蓝色,
④为探究草酸亚铁晶体分解的固体产物,兴趣小组同学准确称取3.60g草酸亚铁晶体(FeC2O4·2H2O),相对分子质量是180),充分加热,使其完全分解,冷却后称得剩余固体的质量为1.60g。若剩余固体只有一种铁的氧化物,通过计算确定该氧化物的化学式为
您最近一年使用:0次



