已知X、Y、Z、R、W、Q六种元素中,X的原子序数为1;Y元素原子最外层电子数是内层电子总数的2倍;Z元素原子次外层电子数比其最外层电子数少4个;R元素原子最外层有1个电子,其阳离子与Z的阴离子原子核外电子总数相同;W元素原子K层和M层电子总数等于其L层电子数。请要求填空:
(1)Z元素形成的原子的结构示意图为___________ ;
(2)从前五种元素中选出三种元素组成化合物,其中属于碱的是___________ (填化学式);属于非电解质的是___________ (填一种物质的名称即可);
(3)现有标准状况下YZ和 混合气体8.96L,其质量为16g,则该气体中,YZ和
混合气体8.96L,其质量为16g,则该气体中,YZ和 的物质的量之比为
的物质的量之比为___________ ;
(4)55.0g化合物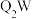 中含有
中含有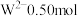 ,则Q的相对原子质量为
,则Q的相对原子质量为___________ ;
(5)将4.00gRZX溶于一定量水,所得溶液的体积为100mL,该溶液中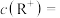
___________ ;
(6)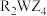 溶于水的电离方程式
溶于水的电离方程式___________ ;
(7)化合物 与
与 反应的化学方程式为
反应的化学方程式为___________ 。
(1)Z元素形成的原子的结构示意图为
(2)从前五种元素中选出三种元素组成化合物,其中属于碱的是
(3)现有标准状况下YZ和
 混合气体8.96L,其质量为16g,则该气体中,YZ和
混合气体8.96L,其质量为16g,则该气体中,YZ和 的物质的量之比为
的物质的量之比为(4)55.0g化合物
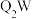 中含有
中含有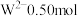 ,则Q的相对原子质量为
,则Q的相对原子质量为(5)将4.00gRZX溶于一定量水,所得溶液的体积为100mL,该溶液中
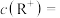
(6)
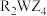 溶于水的电离方程式
溶于水的电离方程式(7)化合物
 与
与 反应的化学方程式为
反应的化学方程式为
更新时间:2024-03-09 22:33:01
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】如表列出了①~⑨九种元素在周期表中的位置:
请按要求回答下列问题。
(1)元素④的名称是___ ,元素④在周期表中所处位置___ ,从元素原子得失电子的角度看,元素④具有___ 性(填“氧化”或“还原”)。
(2)元素⑦的原子结构示意图是___ 。
(3)写出元素⑤形成的单质在氧气中燃烧的化学方程式___ ,这一反应是___ (填“吸热”或“放热”)反应。
| ⅠA | ||||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑧ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑨ |
(1)元素④的名称是
(2)元素⑦的原子结构示意图是
(3)写出元素⑤形成的单质在氧气中燃烧的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】为探究某橙色含结晶水的盐的组成和性质,设计并完成如下实验:
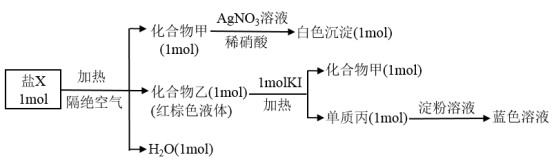
请回答:
(1)化合物甲所含阴离子的离子结构示意图为________________ 。
(2)X的化学式为________________ 。
(3)若分离化合物甲和单质丙组成的固体混合物,最简单的方法是________________ 。
(4)乙与KI反应的化学方程式为________________________________ 。
(5)乙的化学性质与其组成元素的单质相似,下列物质能与乙发生反应的是________ 。
A. B. Mg C.
B. Mg C. D. NaOH
D. NaOH
(6)下列关于卤族物质应用的说法不正确的是________ .
A.实验室常用电解饱和食盐水的方法制取氯气
B.氯气和二氧化氯均可用于自来水消毒,但二氧化氯更高效安全
C.工业上常用氢气与氯气充分混合再点燃的方法制取氯化氢,氯化氢溶于水后可得盐酸
D.可用于生产多种药剂,如熏蒸剂、杀虫剂、抗爆剂等
E.海带可用于治疗碘缺乏病
F.碘化银可用于人工降雨,也是胶片中必不可少的成分

请回答:
(1)化合物甲所含阴离子的离子结构示意图为
(2)X的化学式为
(3)若分离化合物甲和单质丙组成的固体混合物,最简单的方法是
(4)乙与KI反应的化学方程式为
(5)乙的化学性质与其组成元素的单质相似,下列物质能与乙发生反应的是
A.
 B. Mg C.
B. Mg C. D. NaOH
D. NaOH(6)下列关于卤族物质应用的说法不正确的是
A.实验室常用电解饱和食盐水的方法制取氯气
B.氯气和二氧化氯均可用于自来水消毒,但二氧化氯更高效安全
C.工业上常用氢气与氯气充分混合再点燃的方法制取氯化氢,氯化氢溶于水后可得盐酸
D.可用于生产多种药剂,如熏蒸剂、杀虫剂、抗爆剂等
E.海带可用于治疗碘缺乏病
F.碘化银可用于人工降雨,也是胶片中必不可少的成分
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】A、B、C、D、E五种元素,它们原子的核电荷数均小于18,且依次递增,A原子核内仅有一个质子;B原子的电子总数与D原子的最外层电子数相等;A原子与B原子的最外层电子数之和与C原子的最外层电子数相等;D原子有两个电子层,最外层电子数是次外层电子数的3倍,E的原子半径在所有短周期主族元素中最大。
(1)试推断它们各是什么元素,写出元素符号:
A_______ ,B________ ,C________ ,D________ ,E_________ 。
(2)画出D的离子结构示意图___________ 。
(3)D与E按个数比1∶1形成的化合物可与B的最高价氧化物反应生成D单质,反应的化学方程式为___________ 。
(4)A与D按个数比1∶1形成的化合物酸性条件下可与亚铁离子反应,反应后溶液呈黄色,反应的离子方程式为___________ 。(并用双线桥标出电子转移数目)
(1)试推断它们各是什么元素,写出元素符号:
A
(2)画出D的离子结构示意图
(3)D与E按个数比1∶1形成的化合物可与B的最高价氧化物反应生成D单质,反应的化学方程式为
(4)A与D按个数比1∶1形成的化合物酸性条件下可与亚铁离子反应,反应后溶液呈黄色,反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.已知下列十种物质①CH3COOH ②Cu ③NO ④干冰 ⑤硫酸 ⑥Ba (OH)2 ⑦Fe(OH)3胶体 ⑧液氨⑨稀硝酸 ⑩KAl(SO4)3 ⑪熔融 NaHSO4 ⑫酒精。根据上述提供的物质,回答下列问题:
(1)属于电解质的是_______ (填序号,下同),属于非电解质的是_______ ,在熔融状态下不导电而在水溶液下导电的电解质是_______ 。
(2)写出制备Fe(OH)3胶体的离子反应方程式_______ 。
Ⅱ.某50 mL无色溶液由Na+、Fe3+、Mg2+、 、
、 、Cl-、
、Cl-、 中的若干种离子组成,且各离子的物质的量浓度相等,现进行如下实验操作:
中的若干种离子组成,且各离子的物质的量浓度相等,现进行如下实验操作:
①取20 mL溶液于试管中,滴加过量稀HNO3,无明显现象;
②向①的溶液中滴加过量Ba(NO3)2溶液,产生2.33 g白色沉淀;
③取少量②的溶液,滴加AgNO3溶液有白色沉淀生成。
回答下列问题:
(3)在步骤②之前即可确定溶液中不存在的离子是_______ ,步骤②发生反应的离子方程式为_______ 。
(4)原溶液中含有的离子是_______ ,各离子的物质的量均为_______ mol。
(1)属于电解质的是
(2)写出制备Fe(OH)3胶体的离子反应方程式
Ⅱ.某50 mL无色溶液由Na+、Fe3+、Mg2+、
 、
、 、Cl-、
、Cl-、 中的若干种离子组成,且各离子的物质的量浓度相等,现进行如下实验操作:
中的若干种离子组成,且各离子的物质的量浓度相等,现进行如下实验操作:①取20 mL溶液于试管中,滴加过量稀HNO3,无明显现象;
②向①的溶液中滴加过量Ba(NO3)2溶液,产生2.33 g白色沉淀;
③取少量②的溶液,滴加AgNO3溶液有白色沉淀生成。
回答下列问题:
(3)在步骤②之前即可确定溶液中不存在的离子是
(4)原溶液中含有的离子是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】现有下列10种物质:
①冰水混合物 ②碱石灰 ③Mg ④ ⑤熔融KOH ⑥
⑤熔融KOH ⑥ 溶液⑦
溶液⑦ ⑧硫酸 ⑨
⑧硫酸 ⑨ ⑩固体
⑩固体 。回答下列问题。
。回答下列问题。
(1)属于混合物的是____________ 填编号,下同),属于强电解质且能导电的是___________ ,属于非电解质的是___________ 。
(2)将⑥和⑩均配成0.1mol/L的溶液按下表中的不同配比进行混合:
a.按丁方式混合后,所得溶液显___________ (填“酸”“碱”“中”)性;
b.按乙方式混合时,反应的离子方程式为___________ 。
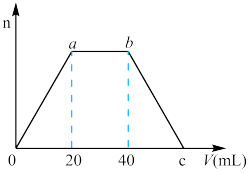
(3)向⑤和⑥制成混合溶液中通入足量的④气体,生成沉淀的物质的量(n)和通入气体体积(V)的关系如图所示,则c点的气体体积是___________ mL;混合溶液中KOH和 的物质的量之比为
的物质的量之比为___________ ;写出ab段发生的离子方程式_________ 。
①冰水混合物 ②碱石灰 ③Mg ④
 ⑤熔融KOH ⑥
⑤熔融KOH ⑥ 溶液⑦
溶液⑦ ⑧硫酸 ⑨
⑧硫酸 ⑨ ⑩固体
⑩固体 。回答下列问题。
。回答下列问题。(1)属于混合物的是
(2)将⑥和⑩均配成0.1mol/L的溶液按下表中的不同配比进行混合:
| 甲 | 乙 | 丙 | 丁 | 戊 | |
0.1mol/L  溶液的体积/mL 溶液的体积/mL | 10 | 10 | 10 | 10 | 10 |
0.1mol/L  溶液的体积/mL 溶液的体积/mL | 5 | 10 | 15 | 20 | 25 |
b.按乙方式混合时,反应的离子方程式为
(3)向⑤和⑥制成混合溶液中通入足量的④气体,生成沉淀的物质的量(n)和通入气体体积(V)的关系如图所示,则c点的气体体积是
 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】根据所学知识填写下列空白:
(1)现有下列十种物质:①HCl气体②Cu③C2H5OH④CO2⑤CuSO4•5H2O⑥NaHCO3⑦Ba(OH)2溶液⑧熔融Na2SO4⑨液氨⑩空气。
所给物质能导电的是_______ ;属于强电解质的是_______ ;属于非电解质的是_______ (填所给物质的序号)。
(2)如图所示,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物。它们的焰色反应均为黄色。
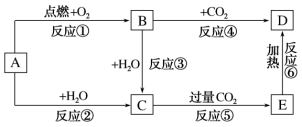
请填写下列空白:
①写出反应②的实验现象:_______ 。
②以上反应中属于氧化还原反应的有_______ (填编号)。
③反应②的离子反应方程式为_______ ;反应④的化学方程式为_______ ;向D中滴入少量盐酸的离子方程式为_______ 。
(1)现有下列十种物质:①HCl气体②Cu③C2H5OH④CO2⑤CuSO4•5H2O⑥NaHCO3⑦Ba(OH)2溶液⑧熔融Na2SO4⑨液氨⑩空气。
所给物质能导电的是
(2)如图所示,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物。它们的焰色反应均为黄色。

请填写下列空白:
①写出反应②的实验现象:
②以上反应中属于氧化还原反应的有
③反应②的离子反应方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】现有部分短周期元素的性质或原子结构如表:
(1)元素T位于元素周期表的第_______ 周期第_______ 族。写出T2-的原子结构示意图_______ 。
(2)元素Y氢元素形成一种离子YH4+,写出该微粒发生水解反应的离子方程式_______ 。
(3)元素Z与元素T相比,非金属性较强的是_______ (用元素符号表示),下列表述中能证明这一事实的是_______ 。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c. 一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是_______ (填化学式)。
| 元素编号 | 元素性质或原子结构 |
| T | M层电子数比K层电子数多4个 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
(2)元素Y氢元素形成一种离子YH4+,写出该微粒发生水解反应的离子方程式
(3)元素Z与元素T相比,非金属性较强的是
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c. 一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A、B、C、D、E为原子序数依次增大的五种短周期主族元素,其中仅含有一种金属元素,A单质是自然界中密度最小的气体,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族.B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成A2C和A2C2两种常见的液态化合物.请回答下列问题:
(1)D在周期表中的位置______ ,E的简单阴离子结构示意图_______ ,A2C2的结构式:
(2)C、D、E三种元素简单离子的离子半径由大到小的顺序是_____________________ 。
(3)请举一个事实说明C和E的非金属性强弱______________ .
(4)用含A元素最简单的有机化合物与炽热的氧化铜反应生成一种单质、液态氧化物和一种可以使澄清石灰水变浑浊的气体,其化学方程式为_____________________________ .
(1)D在周期表中的位置
(2)C、D、E三种元素简单离子的离子半径由大到小的顺序是
(3)请举一个事实说明C和E的非金属性强弱
(4)用含A元素最简单的有机化合物与炽热的氧化铜反应生成一种单质、液态氧化物和一种可以使澄清石灰水变浑浊的气体,其化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】A、B、C、D、E、F为六种短周期元素,相关信息如下:
根据以上信息提示,回答下列问题。
(1)C元素在周期表中的位置为_______ 。简单氢化物沸点最低的是(填化学式)_______ 。
(2)由B、C、D三元素按原子个数2∶3∶4之比形成物质的化学式为_______ ,化合物DEC所含化学键的类型有_______ (填“金属键”、“离子键”、“极性共价键”或“非极性共价键”)。
(3)将BD3通入到FEC溶液中可制得B2D4,该反应的离子方程式为_______ 。
(4)一种淡黄色固体F2C2,其电子式为_______ 。该固体与硫酸亚铁溶液(按物质的量之比为1∶1)反应。反应过程中有气体生成,则该反应的还原剂为_______ 。
| 序号 | 信息 |
| ① | A、B、C原子序数依次增大,均可与D形成含10e-的分子 |
| ② | C为地壳中含量最高的元素 |
| ③ | E与F同周期,且E在同周期元素中非金属性最强 |
| ④ | F为短周期中原子半径最大的元素 |
(1)C元素在周期表中的位置为
(2)由B、C、D三元素按原子个数2∶3∶4之比形成物质的化学式为
(3)将BD3通入到FEC溶液中可制得B2D4,该反应的离子方程式为
(4)一种淡黄色固体F2C2,其电子式为
您最近一年使用:0次
【推荐1】W、X、Y、Z、M、Q是原子序数依次增大的前四周期元素,其元素性质或原子结构如表所示。
(1)W、Z、Q的元素符号分别为_______ 、_______ 、_______ 。
(2)X的基态原子有_______ 种空间运动状态不同的电子,其中能量最高的电子所占据的原子轨道呈_______ 形。
(3)与Y处于同一周期的所有元素中,第一电离能比Y大的元素有_______ 种。[XW4]+的电子式为_______ 。
(4)M位于元素周期表的_______ 区,M3+简化的电子排布式为_______ 。
(5)Q在元素周期表中的位置为_______ ,其价层电子轨道表达式为_______ 。
(6)基态某原子的价层电子排布式为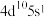 ,推断该元素位于
,推断该元素位于_______ 区。
(7)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成 。
。 与
与 的离子半径大小关系为
的离子半径大小关系为
_______ (填“大于”、“小于”或“等于”) ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是_______ 。
(8)下列各组多电子原子的能级能量比较不正确的是_______ (填序号)。
① ②
② ③
③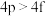 ④
④
| 元素 | 元素性质或原子结构 | ||||||||||||||||||
| W | 电子只有一种自旋取向 | ||||||||||||||||||
| X | 最外层电子排布式为nsnnpn+1 | ||||||||||||||||||
| Y | 非金属元素,且s能级上的电子总数与p能级上的电子总数相等 | ||||||||||||||||||
| Z |
| ||||||||||||||||||
| M | 前四周期元素中原子核外未成对电子数最多 | ||||||||||||||||||
| Q | 基态原子M能层全充满,N层没有成对电子 | ||||||||||||||||||
(2)X的基态原子有
(3)与Y处于同一周期的所有元素中,第一电离能比Y大的元素有
(4)M位于元素周期表的
(5)Q在元素周期表中的位置为
(6)基态某原子的价层电子排布式为
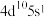 ,推断该元素位于
,推断该元素位于(7)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成
 。
。 与
与 的离子半径大小关系为
的离子半径大小关系为
 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是(8)下列各组多电子原子的能级能量比较不正确的是
①
 ②
② ③
③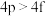 ④
④
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下表是元素周期表的一部分,数字①~⑨代表九种常见的短周期元素,请按题目要求回答下列问题:
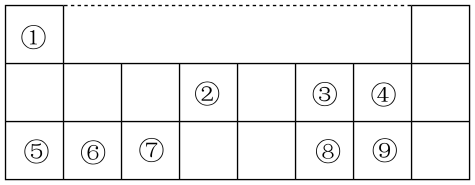
(1)元素⑧在周期表中的位置______ ;
(2)在①~⑨元素中,某种元素的氧化物可用于呼吸面具中氧气来源,请写出该氧化物与水反应的化学方程式______ 。
(3)等质量的单质⑦分别与足量的稀硫酸和氢氧化钠溶液反应,相同条件下产生的气体体积之比为______ 。
(4)元素⑨的单质可使湿润的淀粉-KI试纸变蓝,请写出离子方程式______ 。
(5)Uue是一种暂未合成的化学元素,与Na同主族,位于第八周期,被称为类钫,Uue元素的一种可能存在的核素 的原子核中有180个中子,则A=
的原子核中有180个中子,则A=______ 。
(6)①~⑨中,其中一种元素周期数为族序数的3倍,另一种元素与其同周期,且族序数是周期数的2倍,这两种元素形成的化合物的化学式为______ 。
Ⅱ、如图是某学校实验室从化学试剂商店采购的浓硫酸试剂标签上的部分内容。
(7)若实验室用该浓硫酸配制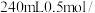 的稀硫酸,请计算需要该浓硫
的稀硫酸,请计算需要该浓硫______ mL(精确到小数点后1位)。
(8)配制过程中的正确操作顺序是:b、d______ 、e(填“字母”)。
a、用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶。
b、用量筒量取所需体积浓硫酸注入盛有约50mL蒸馏水的烧杯。
c、用胶头滴管滴加蒸馏水,至溶液的凹液面与刻度线相切。
d、用玻璃棒慢慢搅动,混合均匀。
e、盖好容量瓶瓶塞,反复上下颠倒,摇匀。
f、将稀释后的 溶液沿玻璃棒注入250mL容量瓶。
溶液沿玻璃棒注入250mL容量瓶。
g、往容量瓶中加入蒸馏水,直到液面在容量瓶刻度线下1~2cm处。
(9)下列操作将导致所配制的 溶液浓度偏大的是
溶液浓度偏大的是______ 。
a、移液过程有 溶液溅出瓶外
溶液溅出瓶外
b、移液后未洗涤烧杯和玻璃棒
c、稀释浓硫酸后未冷却就移液定容
d、加水超过刻度线,用胶头滴管吸出多余液体
e、洗涤时将量筒洗涤液也加入容量瓶

(1)元素⑧在周期表中的位置
(2)在①~⑨元素中,某种元素的氧化物可用于呼吸面具中氧气来源,请写出该氧化物与水反应的化学方程式
(3)等质量的单质⑦分别与足量的稀硫酸和氢氧化钠溶液反应,相同条件下产生的气体体积之比为
(4)元素⑨的单质可使湿润的淀粉-KI试纸变蓝,请写出离子方程式
(5)Uue是一种暂未合成的化学元素,与Na同主族,位于第八周期,被称为类钫,Uue元素的一种可能存在的核素
 的原子核中有180个中子,则A=
的原子核中有180个中子,则A=(6)①~⑨中,其中一种元素周期数为族序数的3倍,另一种元素与其同周期,且族序数是周期数的2倍,这两种元素形成的化合物的化学式为
Ⅱ、如图是某学校实验室从化学试剂商店采购的浓硫酸试剂标签上的部分内容。
(7)若实验室用该浓硫酸配制
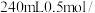 的稀硫酸,请计算需要该浓硫
的稀硫酸,请计算需要该浓硫| 硫酸化学纯(CP) 品名:硫酸 化学式:  相对分子质量:98 密度:  质量分数:98% |
(8)配制过程中的正确操作顺序是:b、d
a、用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶。
b、用量筒量取所需体积浓硫酸注入盛有约50mL蒸馏水的烧杯。
c、用胶头滴管滴加蒸馏水,至溶液的凹液面与刻度线相切。
d、用玻璃棒慢慢搅动,混合均匀。
e、盖好容量瓶瓶塞,反复上下颠倒,摇匀。
f、将稀释后的
 溶液沿玻璃棒注入250mL容量瓶。
溶液沿玻璃棒注入250mL容量瓶。g、往容量瓶中加入蒸馏水,直到液面在容量瓶刻度线下1~2cm处。
(9)下列操作将导致所配制的
 溶液浓度偏大的是
溶液浓度偏大的是a、移液过程有
 溶液溅出瓶外
溶液溅出瓶外b、移液后未洗涤烧杯和玻璃棒
c、稀释浓硫酸后未冷却就移液定容
d、加水超过刻度线,用胶头滴管吸出多余液体
e、洗涤时将量筒洗涤液也加入容量瓶
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D为短周期元素,请根据下表信息回答问题。
(1)B在气态氢化物的电子式为:________________ 。
(2)工业上电解法冶炼单质C的化学方程式为:___________ 。
(3)D的单质与A的一种氢化物反应生成具有漂白性的物质;D的单质与A的另一种氢化物反应生成A的单质。有关反应的化学方程式为:__________ ;___________ 。
| 元素 | A | B | C | D |
| 性质或结构信息 | 工业上通过分离液态空气获得其单质,单质能助燃 | 气态氢化物显碱性 | +3价阳离子的核外电子排布与氖原子相同 | 第三周期原子半径最小 |
(1)B在气态氢化物的电子式为:
(2)工业上电解法冶炼单质C的化学方程式为:
(3)D的单质与A的一种氢化物反应生成具有漂白性的物质;D的单质与A的另一种氢化物反应生成A的单质。有关反应的化学方程式为:
您最近一年使用:0次



