A、B、C、D、E、F为六种短周期元素,相关信息如下:
根据以上信息提示,回答下列问题。
(1)C元素在周期表中的位置为_______ 。简单氢化物沸点最低的是(填化学式)_______ 。
(2)由B、C、D三元素按原子个数2∶3∶4之比形成物质的化学式为_______ ,化合物DEC所含化学键的类型有_______ (填“金属键”、“离子键”、“极性共价键”或“非极性共价键”)。
(3)将BD3通入到FEC溶液中可制得B2D4,该反应的离子方程式为_______ 。
(4)一种淡黄色固体F2C2,其电子式为_______ 。该固体与硫酸亚铁溶液(按物质的量之比为1∶1)反应。反应过程中有气体生成,则该反应的还原剂为_______ 。
| 序号 | 信息 |
| ① | A、B、C原子序数依次增大,均可与D形成含10e-的分子 |
| ② | C为地壳中含量最高的元素 |
| ③ | E与F同周期,且E在同周期元素中非金属性最强 |
| ④ | F为短周期中原子半径最大的元素 |
(1)C元素在周期表中的位置为
(2)由B、C、D三元素按原子个数2∶3∶4之比形成物质的化学式为
(3)将BD3通入到FEC溶液中可制得B2D4,该反应的离子方程式为
(4)一种淡黄色固体F2C2,其电子式为
更新时间:2023-02-18 21:45:08
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验室用浓硫酸与铜丝加热生成的 制备少量
制备少量 并检验性质。
并检验性质。

(1)生成 并检验性质
并检验性质
操作及现象:点燃酒精灯,试管i中有白雾生成,铜丝表面产生气泡;试管ii中溶液红色褪去,试管iii中溶液变红,一段时间后,将铜丝抽离硫酸并停止加热。
①i中发生反应的化学方程式为___________ 。
②ii中现象说明 具有
具有___________ 作用。
③若将试管iii与试管ii位置互换,石蕊溶液变为红色能否作为 是酸性氧化物的证据?说明理由:
是酸性氧化物的证据?说明理由:___________ 。
制备 并检验性质进行实验:
并检验性质进行实验:

(2)A中溶液褪色,说明 具有
具有___________ 性。
(3)B中产生淡黄色沉淀的离子方程式为___________ 。
(4)C中无明显现象。
①甲同学通过检测 的生成证明
的生成证明 和
和 发生反应;取1mLC中溶液于试管中,
发生反应;取1mLC中溶液于试管中,___________ (填试剂和操作),产生白色沉淀。
②乙同学认为甲同学的实验没有排除 的影响,设计对比实验:
的影响,设计对比实验:___________ 。
综合甲、乙同学的实验可知, 能将
能将 氧化。
氧化。
 制备少量
制备少量 并检验性质。
并检验性质。
(1)生成
 并检验性质
并检验性质操作及现象:点燃酒精灯,试管i中有白雾生成,铜丝表面产生气泡;试管ii中溶液红色褪去,试管iii中溶液变红,一段时间后,将铜丝抽离硫酸并停止加热。
①i中发生反应的化学方程式为
②ii中现象说明
 具有
具有③若将试管iii与试管ii位置互换,石蕊溶液变为红色能否作为
 是酸性氧化物的证据?说明理由:
是酸性氧化物的证据?说明理由:制备
 并检验性质进行实验:
并检验性质进行实验:
(2)A中溶液褪色,说明
 具有
具有(3)B中产生淡黄色沉淀的离子方程式为
(4)C中无明显现象。
①甲同学通过检测
 的生成证明
的生成证明 和
和 发生反应;取1mLC中溶液于试管中,
发生反应;取1mLC中溶液于试管中,②乙同学认为甲同学的实验没有排除
 的影响,设计对比实验:
的影响,设计对比实验:综合甲、乙同学的实验可知,
 能将
能将 氧化。
氧化。
您最近一年使用:0次
【推荐2】面对新冠病毒,VB空气防护卡也成了“网红”,成为人们讨论的话题。商品介绍卡片中含有的主要活性成分——亚氯酸钠,在接触空气时可以释放安全可靠的低浓度二氧化氯( ),从而达到消除病毒、细菌活性的防护效果。
),从而达到消除病毒、细菌活性的防护效果。 的一种生产工艺如下:
的一种生产工艺如下:
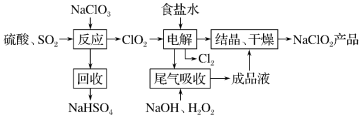
回答下列问题:
(1)写出“反应”步骤中生成 的化学反应方程式:
的化学反应方程式:_______ 。
(2)“电解”产生的 可用于工业制漂白液,写出制备漂白液的离子反应方程式:
可用于工业制漂白液,写出制备漂白液的离子反应方程式:_______ 。
(3)“尾气吸收”是吸收“电解”过程排出的少量 ,此吸收反应中,氧化剂与还原剂的物质的量之比为
,此吸收反应中,氧化剂与还原剂的物质的量之比为_______ ,该反应中还原产物是_______ 。
(4)有同学推测VB空气防护卡原理是因为 与空气中的
与空气中的 发生反应得到
发生反应得到 ,同时得到钠的两种正盐,试写出相应的化学反应方程式:
,同时得到钠的两种正盐,试写出相应的化学反应方程式:_______ 。
 ),从而达到消除病毒、细菌活性的防护效果。
),从而达到消除病毒、细菌活性的防护效果。 的一种生产工艺如下:
的一种生产工艺如下:
回答下列问题:
(1)写出“反应”步骤中生成
 的化学反应方程式:
的化学反应方程式:(2)“电解”产生的
 可用于工业制漂白液,写出制备漂白液的离子反应方程式:
可用于工业制漂白液,写出制备漂白液的离子反应方程式:(3)“尾气吸收”是吸收“电解”过程排出的少量
 ,此吸收反应中,氧化剂与还原剂的物质的量之比为
,此吸收反应中,氧化剂与还原剂的物质的量之比为(4)有同学推测VB空气防护卡原理是因为
 与空气中的
与空气中的 发生反应得到
发生反应得到 ,同时得到钠的两种正盐,试写出相应的化学反应方程式:
,同时得到钠的两种正盐,试写出相应的化学反应方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】某矿渣的成分为主要有Cu2O、还有Al2O3、Fe2O3、SiO2等杂质,工业上用该矿渣获取铜和胆矾的操作流程如下:
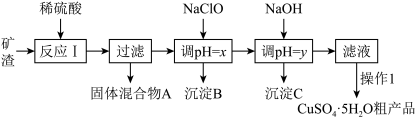
已知:①Cu2O+2H+=Cu+Cu2++H2O。
②部分阳离子以氢氧化物形式沉淀时溶液的pH如下表所示:
(1)为了加快反应Ⅰ的速率,可以采取的措施是___________ (写两条)。
(2)固体混合物A中的成分是___________ 。
(3)反应Ⅰ完成后,铁元素的存在形式为___________ (填离子符号);写出生成该离子的离子方程式___________ 。
(4)操作1主要包括:蒸发浓缩、冷却结晶、___________ 。
(5)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,利用题中所给信息分析沉淀B为___________ , 该反应的离子方程式为______

已知:①Cu2O+2H+=Cu+Cu2++H2O。
②部分阳离子以氢氧化物形式沉淀时溶液的pH如下表所示:
| 沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 5.4 | 4.0 | 2.7 | 5.8 |
| 沉淀完全pH | 6.7 | 5.2 | 3.7 | 8.8 |
(2)固体混合物A中的成分是
(3)反应Ⅰ完成后,铁元素的存在形式为
(4)操作1主要包括:蒸发浓缩、冷却结晶、
(5)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,利用题中所给信息分析沉淀B为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】某同学在学习元素化合物知识的过程中,发现含有相同元素的物质间在一定条件下存在转化规律,绘制如下转化关系图,图中A、B、C、D是由前18号元素组成的物质,且均含有同种元素。

请回答:
(1)若A为单质,C为淡黄色固体。
①则C与H2O反应的化学方程式为:_______ 。
②下列说法正确的是_______ (填字母)。
a.A可经一步反应转化为D
b.B、C均可作呼吸面具的供氧剂
c.B、C、D均可与CO2反应
(2)若A为能使湿润的红色石蕊试纸变蓝的气体,C为红棕色气体。
①A→B反应的化学方程式是_______ 。
②A与C在一定条件下反应生成E和水,E是空气中含量最多的气体,写出反应的化学方程式_______ 。
(3)若B能使品红溶液褪色加热后颜色恢复,则D与某红色金属单质反应生成B的方程式为_______ ,工业上使用过量氨水吸收B,离子方程式为_______ 。

请回答:
(1)若A为单质,C为淡黄色固体。
①则C与H2O反应的化学方程式为:
②下列说法正确的是
a.A可经一步反应转化为D
b.B、C均可作呼吸面具的供氧剂
c.B、C、D均可与CO2反应
(2)若A为能使湿润的红色石蕊试纸变蓝的气体,C为红棕色气体。
①A→B反应的化学方程式是
②A与C在一定条件下反应生成E和水,E是空气中含量最多的气体,写出反应的化学方程式
(3)若B能使品红溶液褪色加热后颜色恢复,则D与某红色金属单质反应生成B的方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某学习小组在实验室制取CO2气体的过程中,不慎用到了浓盐酸,导致制得的CO2气体中混有HCl气体,他们设计了如下除去氯化氢气体并探究CO2与过氧化钠(Na2O2)反应的实验,请回答下列问题:

(1)装置A的作用是____ ;A中不用饱和碳酸钠溶液的原因,理由是_____ (用离子反应方程式表示)
(2)为确定反应后装置B硬质玻璃管中固体的成分,小组同学取适量固体于试管中,加入足量的蒸馏水溶解形成溶液M,无气泡产生,则该固体中不含___ ,该小组同学继续进行探究。
【提出问题】反应后硬质玻璃管中固体的成分是什么?
【做出猜想】猜想一: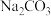 ,猜想二:
,猜想二: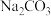 和
和 ,
,
(3)【实验验证】小组同学取上述固体形成的溶液 于试管中,向其中加入过量的
于试管中,向其中加入过量的____ 溶液,
A.氯化钡 B.氢氧化钙 C.亚硫酸钡 D.氢氧化钡
若产生白色沉淀,过滤,向滤液中滴加几滴酚酞试液,溶液变红,则证明猜想二成立。根据此猜想,写出B中一定发生的化学反应方程式:___
(4)【交流反思】小组中有同学认为,将上述滤液中滴加的酚酞试液换成硝酸铜溶液,也能得出同样的结论,你认为该同学的观点__ (填“正确”或“错误”),理由是:__ (用离子反应方程式表示)
(5)研究发现过氧化钠具有较强的氧化性,不仅可以和二氧化碳发生反应,还可以和SO2反应。写出该反应的化学方程式:___

(1)装置A的作用是
(2)为确定反应后装置B硬质玻璃管中固体的成分,小组同学取适量固体于试管中,加入足量的蒸馏水溶解形成溶液M,无气泡产生,则该固体中不含
【提出问题】反应后硬质玻璃管中固体的成分是什么?
【做出猜想】猜想一:
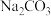 ,猜想二:
,猜想二: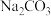 和
和 ,
,(3)【实验验证】小组同学取上述固体形成的溶液
 于试管中,向其中加入过量的
于试管中,向其中加入过量的A.氯化钡 B.氢氧化钙 C.亚硫酸钡 D.氢氧化钡
若产生白色沉淀,过滤,向滤液中滴加几滴酚酞试液,溶液变红,则证明猜想二成立。根据此猜想,写出B中一定发生的化学反应方程式:
(4)【交流反思】小组中有同学认为,将上述滤液中滴加的酚酞试液换成硝酸铜溶液,也能得出同样的结论,你认为该同学的观点
(5)研究发现过氧化钠具有较强的氧化性,不仅可以和二氧化碳发生反应,还可以和SO2反应。写出该反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下图是部分短周期元素的单质及其化合物的转化关系。已知A、B、C、D、E都是单质,常温常压下,A是固体,其余是气体,且C呈黄绿色。化合物H和I两种气体相遇时产生白烟,化合物G的焰色反应为黄色。反应①和②均在水溶液中进行。
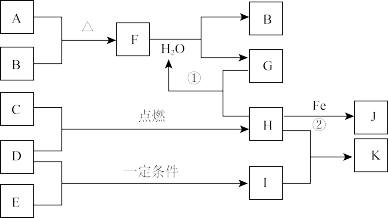
请回答下列问题:
(1)写出下列物质的化学式:A_______ 、K_______ ;
(2)F可水反应的化学方程式为_______ ,该反应中水的作用是_______ ;
a.氧化剂 b.还原剂
c.既是氧化剂又是还原剂 d.既不是氧化剂又不是还原剂
(3)向盛有J溶液的试管中滴加G溶液,可以观察到的现象为_______ ;
(4)C通入盛有G溶液的试管中可以得到漂白液,该反应的离子方程式为_______ ,
(5)D和E的反应在化工生产中可以用于氮的固定,对应的化学方程式为_______ 。

请回答下列问题:
(1)写出下列物质的化学式:A
(2)F可水反应的化学方程式为
a.氧化剂 b.还原剂
c.既是氧化剂又是还原剂 d.既不是氧化剂又不是还原剂
(3)向盛有J溶液的试管中滴加G溶液,可以观察到的现象为
(4)C通入盛有G溶液的试管中可以得到漂白液,该反应的离子方程式为
(5)D和E的反应在化工生产中可以用于氮的固定,对应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】如表是元素周期表的一部分,回答下列有关问题:.
(1)写出⑥的元素符号:___ ,画出⑫的原子结构示意图___ 。
(2)在这些元素的最高价氧化物对应水化物中,酸性最强的是___ ,碱性最强的是___ ,呈两性的氢氧化物是____ 。
(3)写出单质③在空气中燃烧生成产物的电子式____ 。
(4)用电子式表示出④的氯化物的形成过程___ 。
(5)写出实验室制取⑧的单质的离子方程式____ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)在这些元素的最高价氧化物对应水化物中,酸性最强的是
(3)写出单质③在空气中燃烧生成产物的电子式
(4)用电子式表示出④的氯化物的形成过程
(5)写出实验室制取⑧的单质的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】a、b、c、d、e、f、g为七种由短周期元素构成的粒子,它们都具有10个电子,其结构特点如下:
其中b的离子半径大于e的离子半径;d是由极性键构成的四原子分子;c和f在一定条件下形成一个g分子和一个d分子,试写出:
(1)a粒子的原子结构示意图___________
(2)b与e相应元素的最高价氧化物对应水化物的碱性强弱比较为___ >_____ (用化学式表示)。
(3)d与一种含有极性键双核18电子分子反应的化学方程式为______ 。
(4)g与一种含有非极性键双核18电子分子反应的化学方程式为__________
上述反应中,断裂化学键是__________ ,写出的化学键是________ (填“离子键”、“极性键”、“非极性键”、“氢键”)
| 粒子代码 | a | b | c | d | e | f | g |
| 原子核数 | 单核 | 单核 | 双核 | 多核 | 单核 | 多核 | 多核 |
| 电荷数(单位电荷) | 0 | 1+ | 1- | 0 | 2+ | 1+ | 0 |
其中b的离子半径大于e的离子半径;d是由极性键构成的四原子分子;c和f在一定条件下形成一个g分子和一个d分子,试写出:
(1)a粒子的原子结构示意图
(2)b与e相应元素的最高价氧化物对应水化物的碱性强弱比较为
(3)d与一种含有极性键双核18电子分子反应的化学方程式为
(4)g与一种含有非极性键双核18电子分子反应的化学方程式为
上述反应中,断裂化学键是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】V、W、X、Y、Z是五种常见的短周期主族元素,其中W、X、Y、Z原子半径随原子序数的变化如图所示:
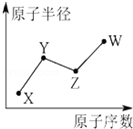
已知Y的最高价氧化物对应的水化物可与其简单氢化物反应可生成盐;Z是地壳中含量最多的元素;W原子的最外层电子数与Ne原子的最外层电子数相差1;V为原子核内有12个中子的二价金属,当2 .4克V与足量盐酸反应时,在标准状况下放出气体2.24L;请回答下列问题:
(1)指出Y元素在周期表中的位置_________ 。
(2)写出W的简单离子的结构示意图_______________ 。
(3)比较W的气态氢化物与H2S和HF的稳定性(由强到弱)____________ 。(填化学式)
(4)由W、Y两种元素组成的一种化合物,每个原子最外层均达到8电子稳定结构,写出该化合物的电子式____________ 。
(5)由X、Y、Z三种元素组成的化合物,是一种常见的化肥,其原子个数比为4:2:3,则该物质含有的化学键类型为_____________ 。
(6)V与W两元素最高价氧化物的水化物反应的化学方程式______________________ 。

已知Y的最高价氧化物对应的水化物可与其简单氢化物反应可生成盐;Z是地壳中含量最多的元素;W原子的最外层电子数与Ne原子的最外层电子数相差1;V为原子核内有12个中子的二价金属,当2 .4克V与足量盐酸反应时,在标准状况下放出气体2.24L;请回答下列问题:
(1)指出Y元素在周期表中的位置
(2)写出W的简单离子的结构示意图
(3)比较W的气态氢化物与H2S和HF的稳定性(由强到弱)
(4)由W、Y两种元素组成的一种化合物,每个原子最外层均达到8电子稳定结构,写出该化合物的电子式
(5)由X、Y、Z三种元素组成的化合物,是一种常见的化肥,其原子个数比为4:2:3,则该物质含有的化学键类型为
(6)V与W两元素最高价氧化物的水化物反应的化学方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】利用铜萃取剂M,通过如下反应实现铜离子的富集:
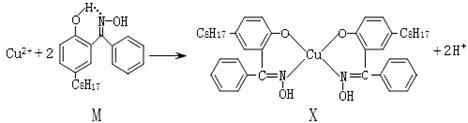
(1)X难溶于水、易溶于有机溶剂,其晶体类型为________ 晶体。
(2)X中非金属元素原子的第一电离能由大到小顺序为____ 。其中第一电离能最大的原子的杂化方式分别为_____
(3)上述反应中断裂和生成的化学键有______ (填序号)。
a.离子键 b.配位键 c.金属键 d.范德华力 e.共价键
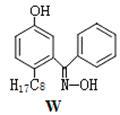
(4)M与W(分子结构如图)相比,M的水溶性小,更利于Cu2+的萃取。M水溶性小的主要原因是____________________________ 。
(5)如图为碳化硅的晶胞(其中●为碳原子,○为硅原子)。

①三个碳原子和三个硅原子相间构成一个_____ 式(船、椅)六元环。
②如果我们以一个硅原子为中心,则与硅原子次近的第二层有_______ 个原子。
③已知:碳原子半径为a×10-8cm,硅子半径为b×10-8cm,假设碳、硅原子是刚性小球,在晶体中彼此相切,计算碳化硅晶体的密度为____ g/cm3(只要求列出算式),查表知该密度比实测值偏小,其原因可能是 _________________________________________ 。


(1)X难溶于水、易溶于有机溶剂,其晶体类型为
(2)X中非金属元素原子的第一电离能由大到小顺序为
(3)上述反应中断裂和生成的化学键有
a.离子键 b.配位键 c.金属键 d.范德华力 e.共价键
(4)M与W(分子结构如图)相比,M的水溶性小,更利于Cu2+的萃取。M水溶性小的主要原因是
(5)如图为碳化硅的晶胞(其中●为碳原子,○为硅原子)。

①三个碳原子和三个硅原子相间构成一个
②如果我们以一个硅原子为中心,则与硅原子次近的第二层有
③已知:碳原子半径为a×10-8cm,硅子半径为b×10-8cm,假设碳、硅原子是刚性小球,在晶体中彼此相切,计算碳化硅晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】铁、钛、镁等金属及其化合物有广泛用途。回答下列问题:
(1)基态Ti原子的价层电子排布图是_______ ,基态Fe原子共有_______ 种不同能级的电子。
(2)某含钛半夹心结构催化剂R能催化乙烯、丙烯等的聚合,其结构如图所示:
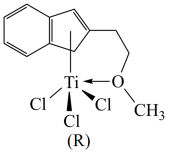
①组成R的元素中,电负性最大的是_______ (填元素符号),氧原子的杂化方式是_______ 。
②R中含有的化学键有_______ (填字母)。
A. 键 B.
键 B. 键 C.离子键 D.配位键 E.金属键
键 C.离子键 D.配位键 E.金属键
(1)基态Ti原子的价层电子排布图是
(2)某含钛半夹心结构催化剂R能催化乙烯、丙烯等的聚合,其结构如图所示:

①组成R的元素中,电负性最大的是
②R中含有的化学键有
A.
 键 B.
键 B. 键 C.离子键 D.配位键 E.金属键
键 C.离子键 D.配位键 E.金属键
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】已知A、B、C、D、E五种元素的核电荷数依次增大,除E为第四周期元素外,其余都是短周期元素,其中A、B、C是同一周期的非金属元素,A元素最外层电子数是内层电子数的2倍,B元素基态原子的最外层有3个未成对电子,化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构,E元素的+3价离子的3d能级为半充满状态。(答题时用A、B、C、D、E对应的元素符号表示)
(1)A的一种氢化物A2H2,其中心原子采取的杂化形式为___________ ,分子中含有___________ 个δ键,__________ π键。
(2)写出化合物DC的电子式_____ ,E原子的核外电子排布式________ 。
(3)由E元素形成的金属的晶胞结构如下图,则该晶胞中含有金属原子的数目为_______________ 。

(4)化合物E(CO)5常温下为液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此判断E(CO)5晶体属于__________ (填晶体类型)。
(1)A的一种氢化物A2H2,其中心原子采取的杂化形式为
(2)写出化合物DC的电子式
(3)由E元素形成的金属的晶胞结构如下图,则该晶胞中含有金属原子的数目为

(4)化合物E(CO)5常温下为液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此判断E(CO)5晶体属于
您最近一年使用:0次



