将CaCl2投入过氧化氢(H2O2)溶液中,并通入适量气体,可得到CaO2·8H2O白色沉淀。
已知:①CaO2·8H2O属微溶性化合物;②过氧化物受热或在强酸性条件下比较容易分解;③由于大量水分子参与结晶,该反应放热;④H2O2是一种弱酸,具有微弱的酸性,CaO2可看作它对应的一种盐。
(1)制取上述过氧化钙晶体的反应条件应包括____ (选择填空)
a 适当低温 b 高温 c 强酸性 d 反应物浓度足够高
(2)通入的气体是______ 。
(3)写出该反应的化学方程式。___________
(4)产物被滤出后用蒸馏水淋洗。如何确定“洗净”____________
已知:①CaO2·8H2O属微溶性化合物;②过氧化物受热或在强酸性条件下比较容易分解;③由于大量水分子参与结晶,该反应放热;④H2O2是一种弱酸,具有微弱的酸性,CaO2可看作它对应的一种盐。
(1)制取上述过氧化钙晶体的反应条件应包括
a 适当低温 b 高温 c 强酸性 d 反应物浓度足够高
(2)通入的气体是
(3)写出该反应的化学方程式。
(4)产物被滤出后用蒸馏水淋洗。如何确定“洗净”
14-15高三上·上海浦东新·期末 查看更多[1]
(已下线)上海市浦东新区2014届高三上学期期末质量测试化学试题
更新时间:2020-03-23 20:37:32
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】钠元素在自然界中以多种化合物的形式存在。NaCl、 、
、 、
、 是重要的化工原料,具有多种用途。
是重要的化工原料,具有多种用途。
Ⅰ.完成下列问题
(1)以上物质可在呼吸面具和潜水艇中作为氧气的来源的是___________ ,可治疗胃酸过多的是___________ 。
(2)查阅资料知: 在一定条件下可以转化为
在一定条件下可以转化为 ,亚硝酸钠外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食
,亚硝酸钠外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食 会导致血红蛋白中的
会导致血红蛋白中的 转化为
转化为 而中毒,误食
而中毒,误食 后可服用维生素C解毒,表明维生素C具有
后可服用维生素C解毒,表明维生素C具有___________ (填“氧化性”或“还原性”)
Ⅱ.化工专家侯德榜发明的侯氏制碱法为我国经济发展做出了重要贡献。某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备 ,进一步处理得到产品
,进一步处理得到产品 和,实验流程如图:
和,实验流程如图:
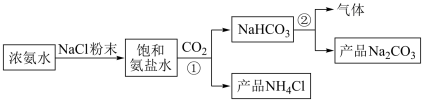
回答下列问题:
(3)产品 可用作氮肥,
可用作氮肥, 属于
属于___________ (填“离子”或“共价”)化合物。
(4)下图装置A和装置B均可用于实验室制备 ,其中装置A的优点是
,其中装置A的优点是___________ , 和盐酸反应的离子方程式为
和盐酸反应的离子方程式为___________ 。

(5)向饱和氨盐水中通入 会产生
会产生 沉淀,从溶液中分离出
沉淀,从溶液中分离出 沉淀的操作名称是
沉淀的操作名称是___________ 。
(6)步骤②生成 的化学方程式为
的化学方程式为___________ ,热稳定性
___________ (填“>”或“<”) 。
。
(7)该方法制得的纯碱中往往会含有NaCl杂质,为检验杂质的存在,简单的检验方案是:取少量试样溶于水后,___________ 。
 、
、 、
、 是重要的化工原料,具有多种用途。
是重要的化工原料,具有多种用途。Ⅰ.完成下列问题
(1)以上物质可在呼吸面具和潜水艇中作为氧气的来源的是
(2)查阅资料知:
 在一定条件下可以转化为
在一定条件下可以转化为 ,亚硝酸钠外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食
,亚硝酸钠外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食 会导致血红蛋白中的
会导致血红蛋白中的 转化为
转化为 而中毒,误食
而中毒,误食 后可服用维生素C解毒,表明维生素C具有
后可服用维生素C解毒,表明维生素C具有Ⅱ.化工专家侯德榜发明的侯氏制碱法为我国经济发展做出了重要贡献。某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备
 ,进一步处理得到产品
,进一步处理得到产品 和,实验流程如图:
和,实验流程如图:
回答下列问题:
(3)产品
 可用作氮肥,
可用作氮肥, 属于
属于(4)下图装置A和装置B均可用于实验室制备
 ,其中装置A的优点是
,其中装置A的优点是 和盐酸反应的离子方程式为
和盐酸反应的离子方程式为
(5)向饱和氨盐水中通入
 会产生
会产生 沉淀,从溶液中分离出
沉淀,从溶液中分离出 沉淀的操作名称是
沉淀的操作名称是(6)步骤②生成
 的化学方程式为
的化学方程式为
 。
。(7)该方法制得的纯碱中往往会含有NaCl杂质,为检验杂质的存在,简单的检验方案是:取少量试样溶于水后,
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】请用三种不同的方法区分厨房中的淀粉和食盐_______ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某溶液中可能含有K+、Na+、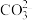 、Cl-中的一种或几种,为鉴别其中所含离子,现进行如下实验:
、Cl-中的一种或几种,为鉴别其中所含离子,现进行如下实验:
请回答下列问题:
(1)原溶液中一定存在的离子是______ (填离子符号,下同),一定不存在的离子是______________ ,可能存在的离子是__________________ 。
(2)为进一步确定原溶液中可能存在的离子是否存在,应进行的实验操作及判断依据是_________
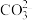 、Cl-中的一种或几种,为鉴别其中所含离子,现进行如下实验:
、Cl-中的一种或几种,为鉴别其中所含离子,现进行如下实验:序号 | 实验操作及现象 |
步骤① | 取原溶液,进行焰色反应,显黄色,透过蓝色钴玻璃观察无紫色 |
步骤② | 取原溶液,向溶液中加入盐酸,有气体产生 |
请回答下列问题:
(1)原溶液中一定存在的离子是
(2)为进一步确定原溶液中可能存在的离子是否存在,应进行的实验操作及判断依据是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】钴具有广泛用途,其正三价化合物具有强氧化性。利用含钴废料(主要成分为Co3O4,还含有少量的铝箔、LiCoO2等杂质)制备碳酸钴的工艺流程如下图所示:

(1)Co2+萃取的反应原理如下:Co2++2HR(有机层) CoR2+2H+,则从有机相中分离出CoSO4需向有机溶剂中加入以下哪种试剂__________ (填选项字母)。
CoR2+2H+,则从有机相中分离出CoSO4需向有机溶剂中加入以下哪种试剂__________ (填选项字母)。
(2)“沉钴”时,Na2CO3的滴速过快或浓度太大,可生成碱式碳酸钴(CoCO3)2·3Co(OH)2沉淀,会导致产品不纯。生成(CoCO3)2·3Co(OH)2沉淀的化学方程式为__________ 。

(1)Co2+萃取的反应原理如下:Co2++2HR(有机层)
 CoR2+2H+,则从有机相中分离出CoSO4需向有机溶剂中加入以下哪种试剂__________ (填选项字母)。
CoR2+2H+,则从有机相中分离出CoSO4需向有机溶剂中加入以下哪种试剂__________ (填选项字母)。| A.H2SO4 | B.NaOH | C.Co(OH)2 | D.HR |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氯化亚铜(CuCl)是一种难溶于水的白色粉末,不溶于乙醇,可溶于浓盐酸和氨水,在潮湿空气中被氧化成绿色的碱式氯化铜[Cu2(OH)3Cl]。工业上常以海绵铜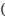 主要成分是Cu,含有少量CuO为原料生产CuCl,其工艺流程如图:
主要成分是Cu,含有少量CuO为原料生产CuCl,其工艺流程如图:
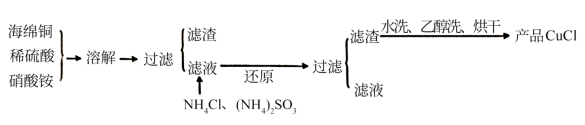
(1)配平“溶解”过程中发生的氧化还原反应的离子方程式:
__ Cu+___ NO +
+___ =___ Cu2++___ NO↑+___ H2O
(2)“还原”过程中,作还原剂的是SO ,氧化产物SO
,氧化产物SO ;写出“还原”过程中发生反应的离子方程式:
;写出“还原”过程中发生反应的离子方程式:___ 。
(3)写出CuCl在潮湿的空气中被氧化的化学方程式:__ 。
(4)析出的CuCl晶体水洗后要立即用无水酒精洗涤,并在真空干燥机内于70℃下干燥2h,冷却密封包装。密封包装的原因是___ 。
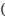 主要成分是Cu,含有少量CuO为原料生产CuCl,其工艺流程如图:
主要成分是Cu,含有少量CuO为原料生产CuCl,其工艺流程如图:
(1)配平“溶解”过程中发生的氧化还原反应的离子方程式:
 +
+(2)“还原”过程中,作还原剂的是SO
 ,氧化产物SO
,氧化产物SO ;写出“还原”过程中发生反应的离子方程式:
;写出“还原”过程中发生反应的离子方程式:(3)写出CuCl在潮湿的空气中被氧化的化学方程式:
(4)析出的CuCl晶体水洗后要立即用无水酒精洗涤,并在真空干燥机内于70℃下干燥2h,冷却密封包装。密封包装的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氯化铁是常见的水处理剂,无水FeCl3的熔点为555K、沸点为588K。工业上制备无水FeCl3的一种工艺如下:

(1)取0.5mL三氯化铁溶液滴入50mL沸水中,再煮沸片得红褐色氢氧化铁胶体,其离子方程式可表示为:___ ,胶体粒子的直径一般不超过___ 。
(2)吸收塔中吸收剂X是___ 。
(3)温度超过673K,捕集器中的物质相对分子质量为325,该物质的分子式为___ 。
(4)通常用碘量法测定FeCl3的质量分数:称取mg无水氯化铁样品,溶于稀盐酸,再转移到100mL容量瓶,用蒸馏水定容;取出10.00mL,加入稍过量的KI溶液,充分反应后,用淀粉作指示剂并用cmol/LNa2S2O3溶液滴定(I2+2S2O =2I-+S4O
=2I-+S4O ),共用去VmL。则样品中氯化铁的质量分数为:
),共用去VmL。则样品中氯化铁的质量分数为:___ 。

(1)取0.5mL三氯化铁溶液滴入50mL沸水中,再煮沸片得红褐色氢氧化铁胶体,其离子方程式可表示为:
(2)吸收塔中吸收剂X是
(3)温度超过673K,捕集器中的物质相对分子质量为325,该物质的分子式为
(4)通常用碘量法测定FeCl3的质量分数:称取mg无水氯化铁样品,溶于稀盐酸,再转移到100mL容量瓶,用蒸馏水定容;取出10.00mL,加入稍过量的KI溶液,充分反应后,用淀粉作指示剂并用cmol/LNa2S2O3溶液滴定(I2+2S2O
 =2I-+S4O
=2I-+S4O ),共用去VmL。则样品中氯化铁的质量分数为:
),共用去VmL。则样品中氯化铁的质量分数为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】清洗和制绒是硅晶片制作的重要步骤之一,硅片化学清洗的主要目的是除去硅片表面杂质(如某些有机物,无机盐,金属、Si、SiO2粉尘等)。常用的化学清洗剂有高纯水、有机溶剂、双氧水、浓酸、强碱等。其中去除硅的氧化物,通常用一定浓度的HF溶液,室温条件下将硅片浸泡1至数分钟。制绒是在硅片表面形成金字塔形的绒面,增加硅对太阳光的吸收。单晶制绒通常用NaOH、Na2SiO3等混合溶液在75~90℃反应25~35 min,效果良好。回答下列问题
Ⅰ.(1)写出晶片制绒反应的离子方程式__________ ,对单晶制绒1990年化学家Seidel提出了一种的电化学模型,他指出Si与NaOH溶液的反应,首先是Si与OH一反应,生成SiO44一,然后SiO44一迅速水解生成H4SiO4。基于此原理分析反应中氧化剂为_______ 。
Ⅱ.在工业中利用镁制取硅:2Mg+SiO2 2MgO+Si,同时有副反应发生:2Mg+Si
2MgO+Si,同时有副反应发生:2Mg+Si Mg2Si,Mg2Si遇盐酸迅速反应生成SiH4(硅烷),SiH4在常温下是一种不稳定、易分解的气体。如图是进行Mg与SiO2反应的实验装置:
Mg2Si,Mg2Si遇盐酸迅速反应生成SiH4(硅烷),SiH4在常温下是一种不稳定、易分解的气体。如图是进行Mg与SiO2反应的实验装置:
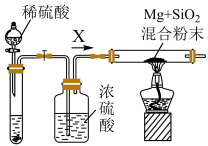
(2)由于氧气的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用________ (填序号)。
a.Na2SO3 b.锌粒 c.纯碱
(3)实验开始时,必须先通入X气体,再加热反应物,其理由是________ ,当反应开始后,移走酒精灯反应能继续进行,其原因是____________ 。
Ⅰ.(1)写出晶片制绒反应的离子方程式
Ⅱ.在工业中利用镁制取硅:2Mg+SiO2
 2MgO+Si,同时有副反应发生:2Mg+Si
2MgO+Si,同时有副反应发生:2Mg+Si Mg2Si,Mg2Si遇盐酸迅速反应生成SiH4(硅烷),SiH4在常温下是一种不稳定、易分解的气体。如图是进行Mg与SiO2反应的实验装置:
Mg2Si,Mg2Si遇盐酸迅速反应生成SiH4(硅烷),SiH4在常温下是一种不稳定、易分解的气体。如图是进行Mg与SiO2反应的实验装置:
(2)由于氧气的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用
a.Na2SO3 b.锌粒 c.纯碱
(3)实验开始时,必须先通入X气体,再加热反应物,其理由是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】如图为某化工企业生产流程示意图:

(1)③中发生置换反应的化学方程式为______ ;③中通入氩气的作用是:_____ 。
(2)从MgCl2溶液中获取无水MgCl2的方法是_____ 。

(1)③中发生置换反应的化学方程式为
(2)从MgCl2溶液中获取无水MgCl2的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】A.【物质结构与性质】
甲基呋喃与氨在高温下反应得到甲基吡咯:


(1)Zn的基态原子核外电子排布式为______________ 。
(2)配合物[Zn(NH3)3(H2O)]2+中,与Zn2+形成配位键的原子是_____________ (填元素符号)。
(3)1 mol甲基呋喃分子中含有σ键的数目为_______________ mol。
(4)甲基吡咯分子中碳原子轨道的杂化轨道类型是____________ 。与NH3分子互为等电子体的阳离子为_____________ 。
(5)甲基吡咯的熔沸点高于甲基呋喃的原因是____________ 。
(6)锌的某种化合物晶胞结构如图所示,则构成该化合物的两种粒子个数比为____________

B.【实验化学】
硫酰氯(SO2Cl2)可用作有机化学的氯化剂,在药物和染料的制取中也有重要作用。某化学学习小组拟用干燥的Cl2和SO2在活性炭催化下制取硫酰氯。反应的化学方程式为:SO2(g)+ Cl2(g) =SO2Cl2(l) ΔH =−97.3 kJ·mol−1,实验装置如图所示(部分夹持装置未画出)。

已知:硫酰氯通常条件下为无色液体,熔点−54.1℃,沸点69.1℃。在潮湿空气中“发烟”;100°C以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解。
回答下列问题:
(1)装置丙的冷凝管中冷凝水的入口是_____________ (填“a”或“b”),装置己的作用是____________ ;如何控制两种反应物体积相等:______________ 。
(2)装置戊上方分液漏斗中最好选用下列试剂:_____________ (选填字母)。
A.蒸馏水 B.饱和食盐水 C.浓氢氧化钠溶液 D.6.0 mol·L−1盐酸
(3)若缺少装置乙和丁(均盛放浓硫酸),潮湿氯气和二氧化硫发生反应的化学方程式是_____________ 。
(4)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯:2ClSO3H SO2Cl2 + H2SO4,分离两种产物的方法是
SO2Cl2 + H2SO4,分离两种产物的方法是____________ (选填字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
甲基呋喃与氨在高温下反应得到甲基吡咯:


(1)Zn的基态原子核外电子排布式为
(2)配合物[Zn(NH3)3(H2O)]2+中,与Zn2+形成配位键的原子是
(3)1 mol甲基呋喃分子中含有σ键的数目为
(4)甲基吡咯分子中碳原子轨道的杂化轨道类型是
(5)甲基吡咯的熔沸点高于甲基呋喃的原因是
(6)锌的某种化合物晶胞结构如图所示,则构成该化合物的两种粒子个数比为

B.【实验化学】
硫酰氯(SO2Cl2)可用作有机化学的氯化剂,在药物和染料的制取中也有重要作用。某化学学习小组拟用干燥的Cl2和SO2在活性炭催化下制取硫酰氯。反应的化学方程式为:SO2(g)+ Cl2(g) =SO2Cl2(l) ΔH =−97.3 kJ·mol−1,实验装置如图所示(部分夹持装置未画出)。

已知:硫酰氯通常条件下为无色液体,熔点−54.1℃,沸点69.1℃。在潮湿空气中“发烟”;100°C以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解。
回答下列问题:
(1)装置丙的冷凝管中冷凝水的入口是
(2)装置戊上方分液漏斗中最好选用下列试剂:
A.蒸馏水 B.饱和食盐水 C.浓氢氧化钠溶液 D.6.0 mol·L−1盐酸
(3)若缺少装置乙和丁(均盛放浓硫酸),潮湿氯气和二氧化硫发生反应的化学方程式是
(4)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯:2ClSO3H
 SO2Cl2 + H2SO4,分离两种产物的方法是
SO2Cl2 + H2SO4,分离两种产物的方法是A.重结晶 B.过滤 C.蒸馏 D.萃取
您最近一年使用:0次



