根据反应:2Na2CO3+ SnO2+4S Na2SO4 + Na2SnS3+2CO2↑。回答下列问题:
Na2SO4 + Na2SnS3+2CO2↑。回答下列问题:
(1)上述反应涉及的元素中,非金属性最强的元素的最外层电子排布式为_____________ 在上述反应的生成物中,属于分子晶体的结构式___________________ 。
(2)在上述反应中单质物质的原子核外共有______ 种不同运动状态的电子,有_____ 种不同能量的电子。
(3)上述反应中,金属性最强的元素与铝元素相比较,可作为判断金属性强弱依据的是__________ (选填编号)。
a.能否置换出铝盐溶液中铝
b.Al(OH)3能否溶解在该元素最高价氧化物对应水化物中
c.单质与氢气化合的难易程度
d.单质与同浓度的稀盐酸发生反应的快慢程度
(4)常温下,测得Na2SnS3溶液pH>7,请用离子方程式表示其原因:___ 。
 Na2SO4 + Na2SnS3+2CO2↑。回答下列问题:
Na2SO4 + Na2SnS3+2CO2↑。回答下列问题:(1)上述反应涉及的元素中,非金属性最强的元素的最外层电子排布式为
(2)在上述反应中单质物质的原子核外共有
(3)上述反应中,金属性最强的元素与铝元素相比较,可作为判断金属性强弱依据的是
a.能否置换出铝盐溶液中铝
b.Al(OH)3能否溶解在该元素最高价氧化物对应水化物中
c.单质与氢气化合的难易程度
d.单质与同浓度的稀盐酸发生反应的快慢程度
(4)常温下,测得Na2SnS3溶液pH>7,请用离子方程式表示其原因:
2013·上海闵行·一模 查看更多[1]
(已下线)上海市闵行区2013年高考一模化学试题
更新时间:2020-03-30 09:40:31
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】氮、铁、钴等元素的化合物在现代农业、科技、国防建设中有着许多独特的用途。
(1)铁、钴位于周期表的_______ 区, 的电子式为
的电子式为_______ ,N、C、O的第一电离能由大到小的顺序为_______ , 中心离子的电子排布式为
中心离子的电子排布式为_______ ,已知 的几何构型为正八面体形,推测
的几何构型为正八面体形,推测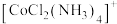 的空间结构有
的空间结构有_______ 种。
(2)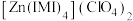 是
是 的一种配合物,IMI的结构为
的一种配合物,IMI的结构为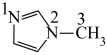 ,IMI中大π键可表示为
,IMI中大π键可表示为
_______ (已知苯中的大π键可表示为 ),该配合物的配位原子为
),该配合物的配位原子为_______ (填序号),配位数为_______ ,IMI的某种衍生物与甘氨酸形成的离子化合物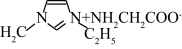 常温下为液态而非固态。原因是
常温下为液态而非固态。原因是_______ 。
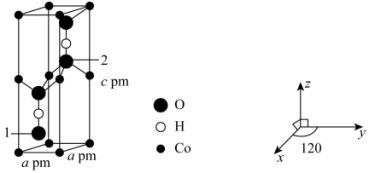
(3)Co可以形成六方晶系晶体,晶胞结构如图所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子坐标。已知晶胞含对称中心,其中1号O原子的坐标为(0.6667,0.3333,0.1077),则2号O原子的坐标为_______ 。设 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为_______  (用代数式表示)。
(用代数式表示)。
(1)铁、钴位于周期表的
 的电子式为
的电子式为 中心离子的电子排布式为
中心离子的电子排布式为 的几何构型为正八面体形,推测
的几何构型为正八面体形,推测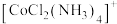 的空间结构有
的空间结构有(2)
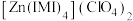 是
是 的一种配合物,IMI的结构为
的一种配合物,IMI的结构为 ,IMI中大π键可表示为
,IMI中大π键可表示为 ),该配合物的配位原子为
),该配合物的配位原子为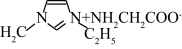 常温下为液态而非固态。原因是
常温下为液态而非固态。原因是(3)Co可以形成六方晶系晶体,晶胞结构如图所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子坐标。已知晶胞含对称中心,其中1号O原子的坐标为(0.6667,0.3333,0.1077),则2号O原子的坐标为
 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为 (用代数式表示)。
(用代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】化学选修物质结构与性质2015年8月12号接近午夜时分,天津滨海新区一处集装箱码头发生爆炸。发生爆炸的是集装箱内的易燃易爆物品,爆炸火光震天,并产生巨大蘑菇云。
回答下列问题:
(1)在组成NH4NO3、NaCN两种物质的元素中第一电离能最大的是_______ (填元素符号),解释原因_____________________ 。
(2)二甲基二硫和甲酸中,在水中溶解度较大的是______ (填名称),原因是__________________ ;烧碱所属的晶体类型为________ ;硫化碱(Na2S)的S2-的基态电子排布式是__________________________ 。
(3)硝酸铵中,NO3-的立体构型为_______ ,中心原子的杂化轨道类型为___________ 。
(4)1mol化合物NaCN中CN-所含的π键数为___________ ,与CN-互为等电子体的分子有_________ 。(CN)2又称为拟卤素,实验室可以用氰化钠、二氧化锰和浓硫酸在加热条件下制得,写成该制备的化学方程式____________ 。
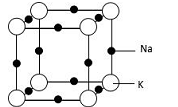
(5)钠钾合金属于金属晶体,其某种合金的晶胞结构如图所示。合金的化学式为____________ ;晶胞中K 原子的配位数为___ ;已知金属原子半径r(Na)=186pm、r(K)=227pm,计算晶体的空间利用率 __________________ (列出计算式,不需要计算出结果)。
回答下列问题:
(1)在组成NH4NO3、NaCN两种物质的元素中第一电离能最大的是
(2)二甲基二硫和甲酸中,在水中溶解度较大的是
(3)硝酸铵中,NO3-的立体构型为
(4)1mol化合物NaCN中CN-所含的π键数为
(5)钠钾合金属于金属晶体,其某种合金的晶胞结构如图所示。合金的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】(一)往硫酸铜水溶液中加入氨水,首先生成难溶物,继续加氨水,难溶物溶解,而且所得溶液的颜色比原来明显加深,得到了一种含2+的溶液,此离子的立体结构如图所示(4个NH3与Cu2+共面,跟H2O﹣Cu2+﹣H2O轴线垂直).请回答以下问题:
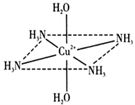
(1)硫酸铜水溶液加氨水的变化过程,用离子方程式表示为生成深蓝色溶液:__________ .
(2)此深蓝色的离子中Cu2+与H2O和NH3形成的是________ 键,请在图中表示此化学键________ .此深蓝色离子的空间结构呈________ 形.
(二).由氧化物经氯化作用生成氯化物是工业生产氯化物的常用方法,Cl2、CCl4是常用的氯化剂。如:Na2O+Cl2=2NaCl+O2、CaO+Cl2=CaCl2+O2、SiO2+2CCl4=SiCl4+2COCl2、Cr2O3+3CCl4=2CrCl3+3COCl2。请回答下列问题:
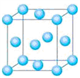
⑴与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有______ (填元素符号),其中一种金属的晶胞结构如图所示,该晶胞中含有金属原子的数目为_____ 。
(2)COCl2俗称光气,分子中C原子采取sp2杂化成键,其中碳氧原子之间共价键是____ (填序号)
a.2个σ键 b.2个π键 c.1个σ键、1个π键
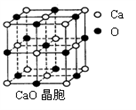
(3)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为_________ 。CaO晶体和NaCl晶体中离子排列方式相同,其晶格能分别为:CaO-3401kJ•mol-1、NaCl-786kJ•mol-1。导致两者晶格能差异的主要原因是_____________________________________________ 。

(1)硫酸铜水溶液加氨水的变化过程,用离子方程式表示为生成深蓝色溶液:
(2)此深蓝色的离子中Cu2+与H2O和NH3形成的是
(二).由氧化物经氯化作用生成氯化物是工业生产氯化物的常用方法,Cl2、CCl4是常用的氯化剂。如:Na2O+Cl2=2NaCl+O2、CaO+Cl2=CaCl2+O2、SiO2+2CCl4=SiCl4+2COCl2、Cr2O3+3CCl4=2CrCl3+3COCl2。请回答下列问题:
⑴与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有

(2)COCl2俗称光气,分子中C原子采取sp2杂化成键,其中碳氧原子之间共价键是
a.2个σ键 b.2个π键 c.1个σ键、1个π键
(3)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。请回答下列问题:
I.(1)Y在元素周期表中的位置为________________ 。
(2)五种元素原子半径由大到小的顺序是(写元素符号)____________________ 。
(3)X、Z两元素能形成两种化合物的电子式分别为______________ 和________ 。
Ⅱ.生活中Q的氯化物是重要的调味品。随着对饮食健康的重视,出现了各种特种类型。
(1)常说“饮食过咸会伤骨”,下列物质中可以作为补钙药品主要成分的是__ (填标号)。
A.CaCO3 B.CaO C.Ca(OH)2 D.Ca
(2)调味品中Q的含量降低,替而代之氯化钾和硫酸镁,可防治高血压和心血管病,往其溶液中滴入氨水,发生反应的离子方程式是________________________ 。
(3)调味品中也可加入硒元素,硒是人体微量元素中的“抗癌之王”,写出证明硒元素非金属性比硫元素弱的一个实验事实:__________________________ 。
(4)调味品中加入碘酸钾可防治碘缺乏症,其中的碘酸钾(KIO3)在酸性溶液中可氧化亚硫酸钠,生成物能使淀粉变蓝,1mol KIO3被还原时,转移电子________ mol,写出主要生成物的化学式_________________________________________ 。
I.(1)Y在元素周期表中的位置为
(2)五种元素原子半径由大到小的顺序是(写元素符号)
(3)X、Z两元素能形成两种化合物的电子式分别为
Ⅱ.生活中Q的氯化物是重要的调味品。随着对饮食健康的重视,出现了各种特种类型。
(1)常说“饮食过咸会伤骨”,下列物质中可以作为补钙药品主要成分的是
A.CaCO3 B.CaO C.Ca(OH)2 D.Ca
(2)调味品中Q的含量降低,替而代之氯化钾和硫酸镁,可防治高血压和心血管病,往其溶液中滴入氨水,发生反应的离子方程式是
(3)调味品中也可加入硒元素,硒是人体微量元素中的“抗癌之王”,写出证明硒元素非金属性比硫元素弱的一个实验事实:
(4)调味品中加入碘酸钾可防治碘缺乏症,其中的碘酸钾(KIO3)在酸性溶液中可氧化亚硫酸钠,生成物能使淀粉变蓝,1mol KIO3被还原时,转移电子
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题。
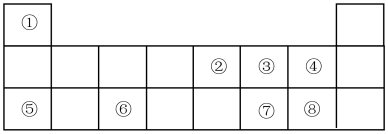
(1)元素③、④、⑤、⑥原子半径最大的为___________ (填元素符号)。
(2)②在元素周期表中的位置为___________ 。
(3)上述8种元素中,非金属性最强的是___________ (填元素符号)。
(4)元素②、③形成的气态氧化物中,更稳定的为___________ (填化学式)。
(5)元素⑤和⑧形成的化合物的电子式为___________ 。
(6)由①③⑤三种元素组成的简单化合物中含有的化学键类型为___________ ;元素⑦的最高价氧化物对应的水化物与元素⑤最高价氧化物对应的水化物溶液反应的离子方程式为___________ 。

(1)元素③、④、⑤、⑥原子半径最大的为
(2)②在元素周期表中的位置为
(3)上述8种元素中,非金属性最强的是
(4)元素②、③形成的气态氧化物中,更稳定的为
(5)元素⑤和⑧形成的化合物的电子式为
(6)由①③⑤三种元素组成的简单化合物中含有的化学键类型为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】153年前门捷列夫制得世界上第一张元素周期表,它反映了元素之间的内在联系,是对元素的一种很好的自然分类。如图为现代元素周期表的一部分,请回答下列问题:(以下问题均用相应的化学用语表达)
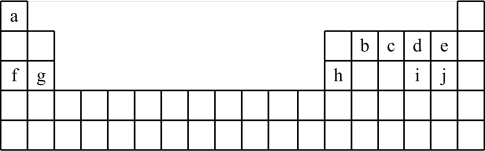
(1)在这10种元素中,非金属性最强的元素在周期表中的位置是______ 。
(2)由a、d、f三种元素形成的化合物含有的化学键有______ (填写化学键类型),属于______ 化合物。
(3)元素b、c形成的简单气态氢化物中较稳定的是_____ ;d、h、i、j的简单离子半径由大到小的顺序排列为_____ 。
(4)用电子式表示c2的形成过程_____ 。
(5)在含有a、g、h简单阳离子的100mL溶液中,逐滴滴加5mol/L的NaOH溶液到过量,生成沉淀的质量与加入的NaOH溶液的体积关系如图所示。由图中数据分析计算:
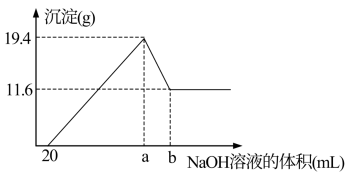
①沉淀减少时发生的离子方程式:______ 。
②a点的数值为:______ mL。

(1)在这10种元素中,非金属性最强的元素在周期表中的位置是
(2)由a、d、f三种元素形成的化合物含有的化学键有
(3)元素b、c形成的简单气态氢化物中较稳定的是
(4)用电子式表示c2的形成过程
(5)在含有a、g、h简单阳离子的100mL溶液中,逐滴滴加5mol/L的NaOH溶液到过量,生成沉淀的质量与加入的NaOH溶液的体积关系如图所示。由图中数据分析计算:

①沉淀减少时发生的离子方程式:
②a点的数值为:
您最近一年使用:0次



