化学选修物质结构与性质2015年8月12号接近午夜时分,天津滨海新区一处集装箱码头发生爆炸。发生爆炸的是集装箱内的易燃易爆物品,爆炸火光震天,并产生巨大蘑菇云。
回答下列问题:
(1)在组成NH4NO3、NaCN两种物质的元素中第一电离能最大的是_______ (填元素符号),解释原因_____________________ 。
(2)二甲基二硫和甲酸中,在水中溶解度较大的是______ (填名称),原因是__________________ ;烧碱所属的晶体类型为________ ;硫化碱(Na2S)的S2-的基态电子排布式是__________________________ 。
(3)硝酸铵中,NO3-的立体构型为_______ ,中心原子的杂化轨道类型为___________ 。
(4)1mol化合物NaCN中CN-所含的π键数为___________ ,与CN-互为等电子体的分子有_________ 。(CN)2又称为拟卤素,实验室可以用氰化钠、二氧化锰和浓硫酸在加热条件下制得,写成该制备的化学方程式____________ 。
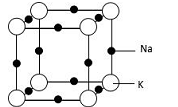
(5)钠钾合金属于金属晶体,其某种合金的晶胞结构如图所示。合金的化学式为____________ ;晶胞中K 原子的配位数为___ ;已知金属原子半径r(Na)=186pm、r(K)=227pm,计算晶体的空间利用率 __________________ (列出计算式,不需要计算出结果)。
回答下列问题:
(1)在组成NH4NO3、NaCN两种物质的元素中第一电离能最大的是
(2)二甲基二硫和甲酸中,在水中溶解度较大的是
(3)硝酸铵中,NO3-的立体构型为
(4)1mol化合物NaCN中CN-所含的π键数为
(5)钠钾合金属于金属晶体,其某种合金的晶胞结构如图所示。合金的化学式为

更新时间:2016-12-09 15:30:10
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。已知:①CuCl可以由CuCl2用适当的还原剂如SO2、SnCl2等还原制得:
2Cu2++2Cl-+SO2+2H2O=2CuCl↓+4H++
2CuCl+SnCl2=2CuCl↓+SnCl4
②CuCl2溶液与乙二胺(H2N—CH2—CH2—NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写):
(1)配离子[Cu(En)2]2+的中心原子基态外围电子排布式为_______ ,H、N、O三种元素的电负性由大到小的顺序是_______ ;
(2)SO2分子的空间构型为_______ ;
(3)乙二胺分子中氮原子轨道的杂化类型为_______ ,乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是_______ 。
(4)配离子[Cu(En)2]2+的配位数为_______ ;
(5)配离子[Cu(En)2]2+含有的微粒间的作用力类型有_______(填字母);
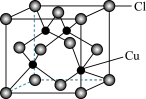
(6)CuCl的晶胞结构如图所示,其中Cl-的配位数(即与Cl- 最近距离的Cu+的个数)为_______ 。
2Cu2++2Cl-+SO2+2H2O=2CuCl↓+4H++

2CuCl+SnCl2=2CuCl↓+SnCl4
②CuCl2溶液与乙二胺(H2N—CH2—CH2—NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写):
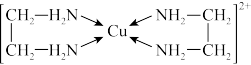
(1)配离子[Cu(En)2]2+的中心原子基态外围电子排布式为
(2)SO2分子的空间构型为
(3)乙二胺分子中氮原子轨道的杂化类型为
(4)配离子[Cu(En)2]2+的配位数为
(5)配离子[Cu(En)2]2+含有的微粒间的作用力类型有_______(填字母);
| A.配位键 | B.极性键 | C.离子键 | D.非极性键 | E.氢键 | F.金属键 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】在HClO4-NaClO4介质中,K5[Co3+O4W12O36](简记为Co3+W)催化氧化NH2OH的过程如下:
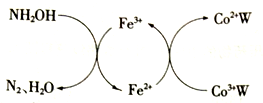
(1)Co2+基态核外电子排布式为________ 。
(2)NH2OH分子中氮原子轨道的杂化类型是_______ ,lmolNH2OH分子中含有σ键的数目为_______ 。
(3)N、H、O三种元素的电负性由小到大的顺序为_________ 。
(4)ClO4-的空间构型为__________ 。
(5)一种铁、碳形成的间隙化合物的晶体结构如右图所示,其中碳原子位于铁原子形成的八面体的中心,每个铁原子又为两个八面体共用,则该化合物的化学式为_________ 。


(1)Co2+基态核外电子排布式为
(2)NH2OH分子中氮原子轨道的杂化类型是
(3)N、H、O三种元素的电负性由小到大的顺序为
(4)ClO4-的空间构型为
(5)一种铁、碳形成的间隙化合物的晶体结构如右图所示,其中碳原子位于铁原子形成的八面体的中心,每个铁原子又为两个八面体共用,则该化合物的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】卤素单质及其化合物是物质世界不可缺少的组成部分。请利用所学物质结构与性质的相关知识回答下列问题:
(1)At原子的核外价电子排布式为______________________ ;I3+中心原子杂化方式为_______ ;ClO2-的空间构型为__________ 。基态氟原子核外电子有________ 种空间运动状态。
(2)已知高碘酸有两种结构,化学式分别为H5IO6( )和HIO4;前者为五元酸,后者为一元酸,请比较二者的酸性强弱:H5IO6
)和HIO4;前者为五元酸,后者为一元酸,请比较二者的酸性强弱:H5IO6 ______ HIO4(填“>”、“=”或“<”).
(3)TiCl4熔点为-24℃,沸点为136.4℃。可溶于甲苯,固态TiCl4属于_________ 晶体。
(4)用锌还原TiCl4的盐酸溶液,可制得绿色配合物[TiCl(H2O)5]Cl2·H2O。1mol该配合物中含有σ键数目为__________ 。
(5)CaF2晶胞结构如下图

①晶体中距离最近的2个Ca2+(X)与一个F-(Y)形成的夹角(∠XYX)为___________ 。
②CaF2的摩尔质量为78g/mol,晶胞密度为ρg/cm3,阿伏伽德罗常数为NA,则晶体中两个最近的Ca2+间中心距离为____________ cm
(1)At原子的核外价电子排布式为
(2)已知高碘酸有两种结构,化学式分别为H5IO6(
 )和HIO4;前者为五元酸,后者为一元酸,请比较二者的酸性强弱:H5IO6
)和HIO4;前者为五元酸,后者为一元酸,请比较二者的酸性强弱:H5IO6 (3)TiCl4熔点为-24℃,沸点为136.4℃。可溶于甲苯,固态TiCl4属于
(4)用锌还原TiCl4的盐酸溶液,可制得绿色配合物[TiCl(H2O)5]Cl2·H2O。1mol该配合物中含有σ键数目为
(5)CaF2晶胞结构如下图

①晶体中距离最近的2个Ca2+(X)与一个F-(Y)形成的夹角(∠XYX)为
②CaF2的摩尔质量为78g/mol,晶胞密度为ρg/cm3,阿伏伽德罗常数为NA,则晶体中两个最近的Ca2+间中心距离为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】磷存在于人体所有细胞中,是维持骨骼和牙齿的必要物质,几乎参与所有生理上的化学反应。回答下列问题:
(1)基态P原子的价电子排布式为____ 。
(2)磷的一种同素异形体是白磷(P4),其分子的空间构型为____ ,键角为____ ,推测其在CS2中的溶解度____ (填“大于”“等于”或“小于”)其在水中的溶解度。
(3)两种三角锥形气态氢化物膦(PH3)和氨(NH3)的键角分别为93.6°和107°,试分析PH3的键角小于NH3的原因__________ 。
(4)常温下PCl5是一种白色晶体,其立方晶系晶胞结构模型如图所示,由A、B两种微粒构成。将其加热至148 ℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CCl4、SF6互为等电子体,则A为____ ,其中心原子杂化轨道类型为_______ 。

(5)磷化硼(BP)是一种超硬耐磨涂层材料,如图为其立方晶胞,其中每个原子均满足8电子稳定结构,P原子的配位数为______ 。已知B—P键的键长为x cm,则磷化硼晶体的密度为____ g·cm-3(列出计算式即可)。
(1)基态P原子的价电子排布式为
(2)磷的一种同素异形体是白磷(P4),其分子的空间构型为
(3)两种三角锥形气态氢化物膦(PH3)和氨(NH3)的键角分别为93.6°和107°,试分析PH3的键角小于NH3的原因
(4)常温下PCl5是一种白色晶体,其立方晶系晶胞结构模型如图所示,由A、B两种微粒构成。将其加热至148 ℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CCl4、SF6互为等电子体,则A为

(5)磷化硼(BP)是一种超硬耐磨涂层材料,如图为其立方晶胞,其中每个原子均满足8电子稳定结构,P原子的配位数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】金属材料及其化合物应用十分广泛。回答下列问题:
(1)基态Mn原子核外未成对电子有___________ 个。
(2)NH3可以和很多过渡金属离子形成配合物,NH3的空间构型为___________ ,其中N原子的杂化轨道类型为___________ 。
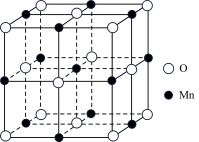
(3)已知锰的某种氧化物的晶胞如图所示,其中锰离子的化合价为___________ ,其配位数为___________ 。
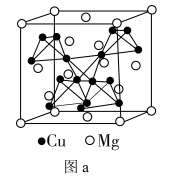
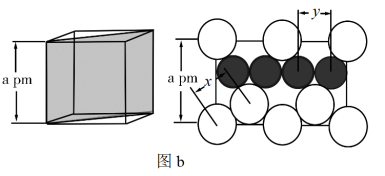
(4)图a是MgCu2的结构,Mg以金刚石方式堆积,八面体空隙和半数的四面体空隙中,填入以四面体方式排列的Cu。图b是沿立方格子对角面取得的截图。可见,Mg原子之间最短距离x=___________ pm,Cu原子之间最短距离y=___________ pm,。设阿伏加德罗常数的值为NA,则MgCu2的密度是___________ g·cm-3(列出计算表达式)。
(1)基态Mn原子核外未成对电子有
(2)NH3可以和很多过渡金属离子形成配合物,NH3的空间构型为
(3)已知锰的某种氧化物的晶胞如图所示,其中锰离子的化合价为

(4)图a是MgCu2的结构,Mg以金刚石方式堆积,八面体空隙和半数的四面体空隙中,填入以四面体方式排列的Cu。图b是沿立方格子对角面取得的截图。可见,Mg原子之间最短距离x=


您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】有X、Y、Z、W、R、Q为前四周期元素,原子序数依次增大。X、Y最外层电子排布可表示为asa,bsbbpb(a≠b),Y、Z、W是位于P区的同一周期的元素,Y与W原子核外的未成对电子数相等,RW2与ZW2-为等电子体,Q为过渡金属元素,其原子核外没有未成对电子。请回答下列问题:
(1)Q的最外层电子排布式为_________ ,RW2的分子立体构型是_________________
(2)Y、Z、W的最简单氢化物中,键角最小的是_______ (用分子式表示), YW与Z2互为等电子体,ZW的结构式为____________ (若有配位键,请用“→”表示)。
(3)ZX3可以与X+结合成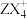 ,这个过程中发生改变的是
,这个过程中发生改变的是____ (填序号)。
a.微粒的空间构型 b.Z原子的杂化类型
c.X-Z-X的键角 d.微粒的电子数
(4)QR在荧光体,光导体材料、涂料、颜料等行业中应用广泛。立方QR晶体结构如图所示,一个晶胞中含有的Q原子数为____________ 。与R原子最近且距离相等的R原子有_____ 个。该晶胞棱长与最近的两个R原子的距离之比为_______
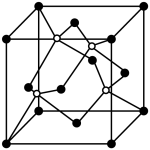
(1)Q的最外层电子排布式为
(2)Y、Z、W的最简单氢化物中,键角最小的是
(3)ZX3可以与X+结合成
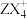 ,这个过程中发生改变的是
,这个过程中发生改变的是a.微粒的空间构型 b.Z原子的杂化类型
c.X-Z-X的键角 d.微粒的电子数
(4)QR在荧光体,光导体材料、涂料、颜料等行业中应用广泛。立方QR晶体结构如图所示,一个晶胞中含有的Q原子数为

您最近一年使用:0次
【推荐1】N、F、Cu及其化合物在化工、医药、材料等方面应用十分广泛。回答下列有关问题:
(1)N原子中最高能级的电子的电子云轮廓图为___________ ;基态Cu+的核外电子排布式为____________ 。
(2)化合物(CH3)3N可用于制备医药、农药。分子中N原子杂化方式为________ ,该物质能溶于水的原因是_____________________ 。
(3)[H2F]+[SbF6]-(氟锑酸)是一种超强酸,其阳离子的空间构型为_____________ ,写出一种与[H2F]+互为等电子体的分子______________ (写化学式)。
(4)氮、铜形成的一种化合物的晶胞结构如图所示。与每个Cu原子紧邻的Cu原子有____ 个,令阿伏加 德罗常数的值为NA,该晶体的密度为______ g/cm3。(列出计算式)
(1)N原子中最高能级的电子的电子云轮廓图为
(2)化合物(CH3)3N可用于制备医药、农药。分子中N原子杂化方式为
(3)[H2F]+[SbF6]-(氟锑酸)是一种超强酸,其阳离子的空间构型为
(4)氮、铜形成的一种化合物的晶胞结构如图所示。与每个Cu原子紧邻的Cu原子有

您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐2】已知A是一种气态烃,其密度是标准状况下H2的14倍,常用来衡量一个国家石油化工发展水平。下列关系图中部分产物可能略去。试回答下列问题:
(此卤代烃与NaOH水溶液的反应中,R代表烃基,X代表卤素原子)
(1)C分子的官能团的名称为___________ ,D中碳原子的杂化方式为___________ 。
(2)反应①~⑦中属于取代反应的是___________ 。
(3)C与F以物质的量之比2:1反应生成G,反应④的化学方程式为___________ 。
(4)B物质可在催化剂作用下被空气中的氧气氧化,写出反应的化学方程式为___________ 。
(5)聚苯乙烯的结构简式为___________ 。
(6)M是D的同分异构体,写出一种符合下列要求的M的结构简式___________ 。
①能与 发生反应 ②一氯取代物有两种结构
发生反应 ②一氯取代物有两种结构
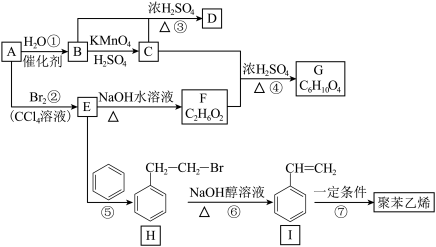

(此卤代烃与NaOH水溶液的反应中,R代表烃基,X代表卤素原子)
(1)C分子的官能团的名称为
(2)反应①~⑦中属于取代反应的是
(3)C与F以物质的量之比2:1反应生成G,反应④的化学方程式为
(4)B物质可在催化剂作用下被空气中的氧气氧化,写出反应的化学方程式为
(5)聚苯乙烯的结构简式为
(6)M是D的同分异构体,写出一种符合下列要求的M的结构简式
①能与
 发生反应 ②一氯取代物有两种结构
发生反应 ②一氯取代物有两种结构
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】《我在故宫修文物》这部纪录片里关于古代青铜器的修复引起了某研学小组的兴趣。“修旧如旧”是文物保护的主旨。
(1)查阅高中教材得知铜锈为 ,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值。参与形成铜绿的物质有
,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值。参与形成铜绿的物质有 和
和_______ ,基态 原子的电子排布式为
原子的电子排布式为_______ 。
(2)继续查阅中国知网,了解到铜锈的成分非常复杂,主要成分有 和
和 。考古学家将铜锈分为无害锈和有害锈,结构如图所示:
。考古学家将铜锈分为无害锈和有害锈,结构如图所示:
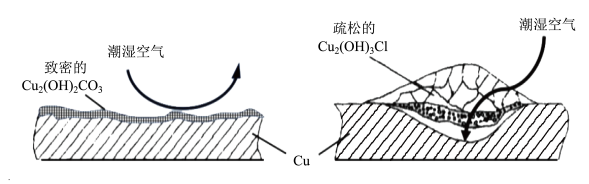
 和
和 分别属于无害锈和有害锈,请解释原因
分别属于无害锈和有害锈,请解释原因_______ 。
(3)文献显示有害锈的形成过程中会产生 (白色不溶于水的固体),请结合下图回答:
(白色不溶于水的固体),请结合下图回答:
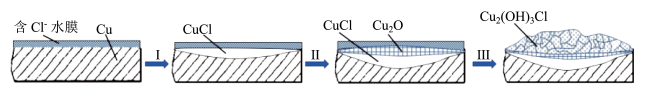
①过程I的正极反应物是_______ 。
②过程I负极的电极反应式是_______ 。
(4)青铜器的修复有以下三种方法:
i.柠檬酸浸法:将腐蚀文物直接放在2%-3%的柠檬酸溶液中浸泡除锈;
ii.碳酸钠法:将腐蚀文物置于含 的缓冲溶液中浸泡,使
的缓冲溶液中浸泡,使 转化为难溶的
转化为难溶的 ;
;
iii. 保护法:
保护法:
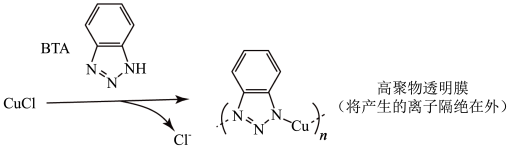
①写出碳酸钠法的离子方程式_______ 。
②三种方法中, 保护法应用最为普遍,分析其可能的优点有
保护法应用最为普遍,分析其可能的优点有_______ 。
A.在青铜器表面形成一层致密的透明保护膜
B.替换出锈层中的 ,能够高效的除去有害锈
,能够高效的除去有害锈
C.和酸浸法相比,不破坏无害锈,可以保护青铜器的艺术价值,做到“修旧如旧”
(1)查阅高中教材得知铜锈为
 ,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值。参与形成铜绿的物质有
,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值。参与形成铜绿的物质有 和
和 原子的电子排布式为
原子的电子排布式为(2)继续查阅中国知网,了解到铜锈的成分非常复杂,主要成分有
 和
和 。考古学家将铜锈分为无害锈和有害锈,结构如图所示:
。考古学家将铜锈分为无害锈和有害锈,结构如图所示:
 和
和 分别属于无害锈和有害锈,请解释原因
分别属于无害锈和有害锈,请解释原因(3)文献显示有害锈的形成过程中会产生
 (白色不溶于水的固体),请结合下图回答:
(白色不溶于水的固体),请结合下图回答:
①过程I的正极反应物是
②过程I负极的电极反应式是
(4)青铜器的修复有以下三种方法:
i.柠檬酸浸法:将腐蚀文物直接放在2%-3%的柠檬酸溶液中浸泡除锈;
ii.碳酸钠法:将腐蚀文物置于含
 的缓冲溶液中浸泡,使
的缓冲溶液中浸泡,使 转化为难溶的
转化为难溶的 ;
;iii.
 保护法:
保护法:
①写出碳酸钠法的离子方程式
②三种方法中,
 保护法应用最为普遍,分析其可能的优点有
保护法应用最为普遍,分析其可能的优点有A.在青铜器表面形成一层致密的透明保护膜
B.替换出锈层中的
 ,能够高效的除去有害锈
,能够高效的除去有害锈C.和酸浸法相比,不破坏无害锈,可以保护青铜器的艺术价值,做到“修旧如旧”
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】2016年诺贝尔化学奖授予在“分子机器设计和合成”领域有突出成就的三位科学家,其研究对象之一“分子开关”即与大环主体分子苯芳烃、硫或氮杂环杯芳烃等有关。回答下列问题:
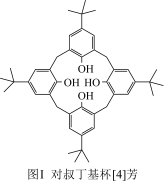
(1)对叔丁基杯[4]芳烃(如图Ⅰ所示)可用于ⅢB族元素对应离子的萃取,如La3+、Sc2+。写出基态二价钪离子(Sc2+)的核外电子排布式:____ ,其中电子占据的轨道数为_____ 个。
(2)对叔丁基杯[4]芳烃由4个羟基构成杯底,其中羟基氧原子的杂化方式为_____ ,羟基间的相互作用力为_____ 。
(3)不同大小的苯芳烃能识别某些离子,如:N3-、SCN−等。一定条件下,SCN−与MnO2反应可得到(SCN)2,试写出(SCN)2的结构式_______ 。
(4)NH3分子在独立存在时H-N-H键角为106.7°。如图 [Zn(NH3)6]2+离子的部分结构以及H-N-H键角的测量值。解释配合物中H-N-H键角变为109.5°的原因:____ 。
(5)橙红色的八羰基二钴[Co2(CO)8]的熔点为52℃,可溶于乙醇、乙醚、苯等有机溶剂。该晶体属于___ 晶体,八羰基二钴在液氨中被金属钠还原成四羰基钴酸钠[NaCo(CO)4],四羧基钴酸钠中含有的化学键为_____ 。
(6)已知C60分子结构和C60晶胞示意图(如图Ⅱ、图Ⅲ所示):

则一个C60分子中含有σ键的个数为______ ,C60晶体密度的计算式为____ g·cm−3。(NA为阿伏伽德罗常数的值)
(1)对叔丁基杯[4]芳烃(如图Ⅰ所示)可用于ⅢB族元素对应离子的萃取,如La3+、Sc2+。写出基态二价钪离子(Sc2+)的核外电子排布式:

(2)对叔丁基杯[4]芳烃由4个羟基构成杯底,其中羟基氧原子的杂化方式为
(3)不同大小的苯芳烃能识别某些离子,如:N3-、SCN−等。一定条件下,SCN−与MnO2反应可得到(SCN)2,试写出(SCN)2的结构式
(4)NH3分子在独立存在时H-N-H键角为106.7°。如图 [Zn(NH3)6]2+离子的部分结构以及H-N-H键角的测量值。解释配合物中H-N-H键角变为109.5°的原因:
(5)橙红色的八羰基二钴[Co2(CO)8]的熔点为52℃,可溶于乙醇、乙醚、苯等有机溶剂。该晶体属于
(6)已知C60分子结构和C60晶胞示意图(如图Ⅱ、图Ⅲ所示):

则一个C60分子中含有σ键的个数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】常见的太阳能电池有单晶硅太阳能电池、多晶硅太阳能电池、GaAs 太阳能电池及铜铟镓硒薄膜太阳能电池等。
(1)基态亚铜离子(Cu+)的价电子排布图为_________ ;高温下CuO 容易转化为Cu2O,试从原子结构角度解释原因:_____ 。
(2)镓、砷、硒三种元素位于第四周期,其第一电离能从大到小的顺序为_____ (用元素符号表示)
(3)GaCl3和AsF3的立体构型分别是_____ ,_____ 。
(4)硼酸(H3BO3)本身不能电离出H+,在水中易结合一个OH-生成[B(OH)4]-,而体现弱酸性。
①[B(OH) 4]-中B 原子的杂化类型为_____ 。②[B(OH)4 ]-的结构式为_____ 。
(5)金刚石的晶胞如图,若以硅原子代替金刚石晶体中的碳原子,便得到晶体硅;若将金刚石晶体中一半的碳原子换成硅原子,且碳、硅原子交替,即得到碳化硅晶体(金刚砂)。
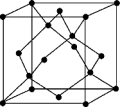
①金刚石、晶体硅、碳化硅的熔点由高到低的排列顺序是_____ (用化学式表示);②金刚石的晶胞参数为a pm(1pm=10-12 m)。1cm3晶体的平均质量为_____ g(只要求列算式,阿伏伽德罗常数为NA)。
(1)基态亚铜离子(Cu+)的价电子排布图为
(2)镓、砷、硒三种元素位于第四周期,其第一电离能从大到小的顺序为
(3)GaCl3和AsF3的立体构型分别是
(4)硼酸(H3BO3)本身不能电离出H+,在水中易结合一个OH-生成[B(OH)4]-,而体现弱酸性。
①[B(OH) 4]-中B 原子的杂化类型为
(5)金刚石的晶胞如图,若以硅原子代替金刚石晶体中的碳原子,便得到晶体硅;若将金刚石晶体中一半的碳原子换成硅原子,且碳、硅原子交替,即得到碳化硅晶体(金刚砂)。

①金刚石、晶体硅、碳化硅的熔点由高到低的排列顺序是
您最近一年使用:0次
【推荐3】(1)基态Fe原子的简化电子排布式为______________________ 。
(2)常温下,Fe(CO)5为黄色液体,易溶于非极性溶剂。写出CO的电子式______________ ;Fe(CO)5分子中σ键与π键之比为______________ 。
(3)Ni能与类卤素(SCN)2反应生成Ni(SCN)2。Ni(SCN)2中第一电离能最大的元素是_____________ ;(SCN)2分子中硫原子的杂化方式是_____________ ;
(4)硝酸铜溶于氨水形成[Cu(NH3)4](NO3)2的深蓝色溶液。
①[Cu(NH3)4](NO3)2中阴离子的立体构型是_________________ 。
②与NH3互为等电子体的一种阴离子为_____________ (填化学式);氨气在一定的压强下,测得的密度比该压强下理论密度略大,请解释原因__________ 。
(5)金属晶体可看成金属原子在三维空间中堆积而成,单质铝中铝原子采用铜型模式堆积,原子空间利用率为74%,则铝原子的配位数为________________ 。
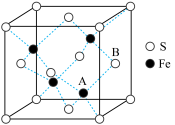
(6)铁和硫形成的某种晶胞结构如右图所示,晶胞参数a=xpm,则该物质的化学式为___________________ ;A原子距离B原子所在立方体侧面的最短距离为________________ pm(用x表示); 该晶胞的密度为____________ g·cm-3。(阿伏加 德罗常数用NA表示)
(2)常温下,Fe(CO)5为黄色液体,易溶于非极性溶剂。写出CO的电子式
(3)Ni能与类卤素(SCN)2反应生成Ni(SCN)2。Ni(SCN)2中第一电离能最大的元素是
(4)硝酸铜溶于氨水形成[Cu(NH3)4](NO3)2的深蓝色溶液。
①[Cu(NH3)4](NO3)2中阴离子的立体构型是
②与NH3互为等电子体的一种阴离子为
(5)金属晶体可看成金属原子在三维空间中堆积而成,单质铝中铝原子采用铜型模式堆积,原子空间利用率为74%,则铝原子的配位数为
(6)铁和硫形成的某种晶胞结构如右图所示,晶胞参数a=xpm,则该物质的化学式为

您最近一年使用:0次



