某氯化铁样品含有少量 杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行:
杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行:

请根据上面流程,回答以下问题:
(1)“操作I”是配制溶液,所用到的玻璃仪器除烧杯玻璃棒、容量瓶外,还必须有______ (填仪器名称)。
(2)下列操作可能使所配溶液浓度偏小的是______ (填写序号)。
①未洗涤烧杯和玻璃棒
②定容时俯视容量瓶的刻度线
③配溶液前容量瓶中有少量蒸馏水
④摇匀后,发现液面低于刻度线后继续加水至凹液面与刻度线相切
(3)请写出加入氯水发生的离子反应方程式______
(4)检验沉淀是否已经洗涤干净的操作是______
(5)若原样品质量a为100g,灼烧至固体质量不再变化时,最终得到6.0g红棕色固体,样品中铁元素的质量分数是______
(6)取红棕色固体溶于稀硫酸配成溶液甲,用于验证 与
与 发生了氧化还原反应,使用的药品和装置如图所示,则下列说法
发生了氧化还原反应,使用的药品和装置如图所示,则下列说法不合理 的是______
A.能表明 的还原性弱于
的还原性弱于 的现象是B中蓝色溶液褪色
的现象是B中蓝色溶液褪色
B.装置C中使用倒置的漏斗,其目的是防止倒吸
C.为了验证A中发生了氧化还原反应,加入用稀盐酸酸化的 溶液产生白色沉淀
溶液产生白色沉淀
D.为了验证A中的 全部被
全部被 还原了,可先加入氯水,再加KSCN溶液
还原了,可先加入氯水,再加KSCN溶液
 杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行:
杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行:
请根据上面流程,回答以下问题:
(1)“操作I”是配制溶液,所用到的玻璃仪器除烧杯玻璃棒、容量瓶外,还必须有
(2)下列操作可能使所配溶液浓度偏小的是
①未洗涤烧杯和玻璃棒
②定容时俯视容量瓶的刻度线
③配溶液前容量瓶中有少量蒸馏水
④摇匀后,发现液面低于刻度线后继续加水至凹液面与刻度线相切
(3)请写出加入氯水发生的离子反应方程式
(4)检验沉淀是否已经洗涤干净的操作是
(5)若原样品质量a为100g,灼烧至固体质量不再变化时,最终得到6.0g红棕色固体,样品中铁元素的质量分数是
(6)取红棕色固体溶于稀硫酸配成溶液甲,用于验证
 与
与 发生了氧化还原反应,使用的药品和装置如图所示,则下列说法
发生了氧化还原反应,使用的药品和装置如图所示,则下列说法
A.能表明
 的还原性弱于
的还原性弱于 的现象是B中蓝色溶液褪色
的现象是B中蓝色溶液褪色B.装置C中使用倒置的漏斗,其目的是防止倒吸
C.为了验证A中发生了氧化还原反应,加入用稀盐酸酸化的
 溶液产生白色沉淀
溶液产生白色沉淀D.为了验证A中的
 全部被
全部被 还原了,可先加入氯水,再加KSCN溶液
还原了,可先加入氯水,再加KSCN溶液
19-20高二·浙江·期末 查看更多[1]
(已下线)【新东方】 2020-84
更新时间:2020-02-28 09:18:48
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】为了验证木炭和浓硫酸反应产物,选用如图所示装置(内含物质)进行实验。
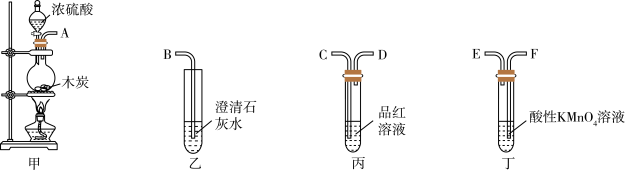
(1)写出装置甲中所发生反应的化学方程式:_______ 。
(2)如果要检验产物水,检验装置应连在_______ (填“甲、乙、丙、丁”)装置之后;用药品_______ ;现象_______ 。
(3)为了检验CO2和SO2设置了如下的装置连接甲-丙-丁-丙-乙。若检验出有SO2生成,则第一个装置丙的现象是_______ ;若实验检验出有CO2生成,则装置乙、第二个丙中的现象分别为:装置乙中_______ ,装置第二个丙中_______ ;装置丁中酸性KMnO4溶液的作用是_______ ;为了测出CO2,第二个丙装置_______ (“能,不能”)撤销。不能则说明原因;若能,证明有CO2生成,填写撤销第二个丙装置后丁装置中的现象。_______ 。

(1)写出装置甲中所发生反应的化学方程式:
(2)如果要检验产物水,检验装置应连在
(3)为了检验CO2和SO2设置了如下的装置连接甲-丙-丁-丙-乙。若检验出有SO2生成,则第一个装置丙的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某化学兴趣小组的同学为探究二氧化硫的化学性质,设计了如下图所示的实验装置。

回答下列问题:
(1)某同学拧开分液漏斗下面的活塞后发现浓硫酸开始时能流出,但一会儿就停止下流,请分析原因:_______ 。
(2)加入浓硫酸后,点燃酒精灯,烧瓶中发生反应的化学方程式为_______ 。
(3)反应开始后,观察到B、C两瓶中溶液均褪色,出现该实验现象分别是由于SO2具有_______ 性和_______ 性。指出实验装置设计的不足之处:_______ 。
(4)充分反应后,兴趣小组同学发现铜有剩余,其推测烧瓶中H2SO4是否消耗完,并说明理由:_______ 。

回答下列问题:
(1)某同学拧开分液漏斗下面的活塞后发现浓硫酸开始时能流出,但一会儿就停止下流,请分析原因:
(2)加入浓硫酸后,点燃酒精灯,烧瓶中发生反应的化学方程式为
(3)反应开始后,观察到B、C两瓶中溶液均褪色,出现该实验现象分别是由于SO2具有
(4)充分反应后,兴趣小组同学发现铜有剩余,其推测烧瓶中H2SO4是否消耗完,并说明理由:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】为检验浓硫酸和木炭反应的产物,某同学设计如图所示装置进行实验。据此回答下列问题:

(1)指出上述装置中的一处错误:___________ ;写出装置A中发生反应的化学方程式:___________ 。
(2)装置B中无水硫酸铜的作用是___________ ;证明产物中有CO2的实验现象是___________ ;浓硫酸与木炭的反应体现了浓H2SO4的___________ 性。
(3)取下装置C,在该试管口套上气球,将无色溶液加热恢复至红色,冷却后,发现溶液颜色___________ (填“变深”或"变浅”)。
(4)装置C可以用装置F代替,则装置F中SO2与Fe3+发生反应的离子方程式为___________ ,某同学为验证SO2与Fe3+发生反应,设计如下实验:取适量反应后的溶液,滴加少量溴水,溴水褪色说明发生反应。该方案是否合理并说明理由:___________ 。

(1)指出上述装置中的一处错误:
(2)装置B中无水硫酸铜的作用是
(3)取下装置C,在该试管口套上气球,将无色溶液加热恢复至红色,冷却后,发现溶液颜色
(4)装置C可以用装置F代替,则装置F中SO2与Fe3+发生反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】已知Fe2O3与H2的反应会因温度不同而生成Fe3O4.某兴趣小组在用H2还原Fe2O3的实验中,用磁铁吸出生成的黑色粉末X。为确定X的组成,他有进行了相关实验探究。
(1)甲同学认为黑色粉末X能磁铁吸引,因此X是铁单质。但乙用学不同意他的观点,原因是___________
(2)乙同学:先将少量黑色粉末X放入盛有足量硫酸铜溶液的烧杯中,搅拌,固体部分溶解,有红色物质析出,过滤:利用磁铁除去滤渣中的红色物质,然后向剩余滤渣中加入盐酸,滴加几滴KSCN溶液,溶液出现红色。通过分析现象,乙同学得出X的组成是Fe和Fe3O4。
①写出剩余滤渣与盐酸反应的离子方程式:____ ,滴加KSCN溶液的目的是____
②若在粉末X中直接加入盐酸、KSCN溶液,溶液不出现红色,则不出现红色的原因是(用离子方程式表示)______ 。
(3)丙同学的实验方案如下:

①加入H2O2时,发生反应的离子方程式为___ ,操作Z所需的玻璃仪器有___
②通过以上数据,可得出288g黑色粉末X中各成分的物质的量为___
(1)甲同学认为黑色粉末X能磁铁吸引,因此X是铁单质。但乙用学不同意他的观点,原因是
(2)乙同学:先将少量黑色粉末X放入盛有足量硫酸铜溶液的烧杯中,搅拌,固体部分溶解,有红色物质析出,过滤:利用磁铁除去滤渣中的红色物质,然后向剩余滤渣中加入盐酸,滴加几滴KSCN溶液,溶液出现红色。通过分析现象,乙同学得出X的组成是Fe和Fe3O4。
①写出剩余滤渣与盐酸反应的离子方程式:
②若在粉末X中直接加入盐酸、KSCN溶液,溶液不出现红色,则不出现红色的原因是(用离子方程式表示)
(3)丙同学的实验方案如下:

①加入H2O2时,发生反应的离子方程式为
②通过以上数据,可得出288g黑色粉末X中各成分的物质的量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下列框图中的字母分别代表一种常见的物质或其溶液,相互之间的转化关系如图所示(部分产物及反应条件已略去)。已知A、B为气态单质,F是地壳中含量最多的金属元素的单质;E、H、I为氧化物,E为黑色固体,I为红棕色气体;M为红褐色沉淀。

请回答下列问题:
(1)A在B中燃烧的现象是__________________________________________ 。
(2)D+E→B的反应中,被氧化与被还原的物质的物质的量比是_________________________ 。
(3)G+J→M的离子方程式是____________________________________ 。
(4)Y受热分解的化学方程式是______________________________________ 。
(5)检验硫酸铁溶液中是否存在Fe2+的试剂是____________________ 。

请回答下列问题:
(1)A在B中燃烧的现象是
(2)D+E→B的反应中,被氧化与被还原的物质的物质的量比是
(3)G+J→M的离子方程式是
(4)Y受热分解的化学方程式是
(5)检验硫酸铁溶液中是否存在Fe2+的试剂是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】现有金属单质A、B和气体甲、乙、丙以及物质C、D、E、F,它们之间能发生如下反应。(图中有些反应的产物和反应条件没有标出)

请回答下列问题:
(1)丙的电子式为_____________ ;
(2)写出下列反应的离子方程式:④_____________________________ ;⑤____________________________ 。
(3)写出D溶液与Al反应的化学方程式____________________ 。
(4)浓硫酸具有强氧化性却可以用B材料车运输,是因为_________________ 。
(5)为鉴定B单质,将试样用稀盐酸溶解,取上层清液后需再加入的试剂(填写字母代号)是_____________ 。
A.碘水 B.NaOH溶液 C.KSCN溶液 D.Na2SO3溶液

请回答下列问题:
(1)丙的电子式为
(2)写出下列反应的离子方程式:④
(3)写出D溶液与Al反应的化学方程式
(4)浓硫酸具有强氧化性却可以用B材料车运输,是因为
(5)为鉴定B单质,将试样用稀盐酸溶解,取上层清液后需再加入的试剂(填写字母代号)是
A.碘水 B.NaOH溶液 C.KSCN溶液 D.Na2SO3溶液
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某校研究性学习小组用已部分生锈(Fe2O3)的废铁屑,制作印刷电路板的腐蚀剂,即FeCl3溶液。实验操作过程如下:

根据要求回答问题:
(1)用浓盐酸配制250mL 0.2mol•L-1稀盐酸,图中有两处错误分别是_____________ ,______________ 。
(2)废铁屑用盐酸处理后,还含有不溶性杂质,为获取澄清的A溶液,进行物质分离的操作名称是___________ 。
(3)若FeCl2溶液中混有少量的FeCl3溶液,现要加入一种试剂除去FeCl3,请写出除杂的离子方程式______________________ 。
(4)配制250mL 0.2mol•L-1稀盐酸时,下列操作会造成结果偏高的是( )
A.配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出
B.转移溶液前溶液未冷却至室温
C.未洗涤烧杯和玻璃棒
D.定容时俯视容量瓶的刻度线
E.容量瓶洗涤干净后,瓶内壁有少量水滴。


根据要求回答问题:
(1)用浓盐酸配制250mL 0.2mol•L-1稀盐酸,图中有两处错误分别是
(2)废铁屑用盐酸处理后,还含有不溶性杂质,为获取澄清的A溶液,进行物质分离的操作名称是
(3)若FeCl2溶液中混有少量的FeCl3溶液,现要加入一种试剂除去FeCl3,请写出除杂的离子方程式
(4)配制250mL 0.2mol•L-1稀盐酸时,下列操作会造成结果偏高的是
A.配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出
B.转移溶液前溶液未冷却至室温
C.未洗涤烧杯和玻璃棒
D.定容时俯视容量瓶的刻度线
E.容量瓶洗涤干净后,瓶内壁有少量水滴。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】铁是人类较早使用的金属之一,运用所学知识,回答下列问题。
I.电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)写出FeCl3溶液与金属铜发生反应的离子方程式___________ 。
(2)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,准备采用下列步骤:
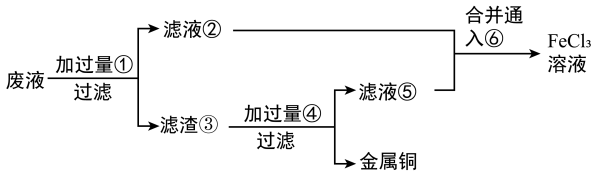
请写出上述过程中滤渣③中所含成分的化学式___________ ,物质⑥的化学式___________ 。
II.已知FeCl3易吸收空气里的水分而潮解,100℃左右时易升华,实验室制备FeCl3的装置如图所示。
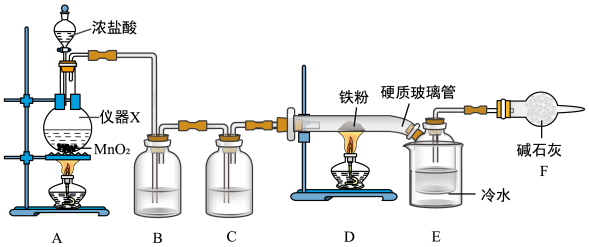
回答下列问题:
(1)仪器X的名称为___________ ,装置A中发生反应的化学方程式为___________ 。
(2)装置B中溶液为___________ ,C的作用是___________ 。
(3)加热时,先点燃装置A的酒精灯,当___________ 时,再点燃装置D的酒精灯。
(4)用粗硬质玻璃管直接连接装置D和E,比用细导管连接的优点是___________ 。
(5)装置F中碱石灰的成分是NaOH和CaO混合物,其作用是(提示:从不同角度作答2条)___________ 。
I.电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)写出FeCl3溶液与金属铜发生反应的离子方程式
(2)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,准备采用下列步骤:

请写出上述过程中滤渣③中所含成分的化学式
II.已知FeCl3易吸收空气里的水分而潮解,100℃左右时易升华,实验室制备FeCl3的装置如图所示。

回答下列问题:
(1)仪器X的名称为
(2)装置B中溶液为
(3)加热时,先点燃装置A的酒精灯,当
(4)用粗硬质玻璃管直接连接装置D和E,比用细导管连接的优点是
(5)装置F中碱石灰的成分是NaOH和CaO混合物,其作用是(提示:从不同角度作答2条)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】苯甲酸可用于医药、染料载体、增塑剂、果汁饮料的保香剂和食品防腐剂等的生产。某化学兴趣小组欲在实验室制备苯甲酸、回收二氧化锰并测定其纯度,进行如下实验:
苯甲酸实验室制备原理为: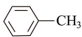 +2KMnO4
+2KMnO4
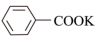 +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O
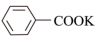

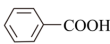
实验装置如图所示。
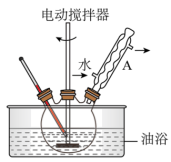
已知:甲苯的密度是0.872g·L-1;苯甲酸微溶于冷水,溶于热水。
实验步骤:
Ⅰ.在50mL三颈烧瓶中加入1.5mL甲苯、20mL水和5.0g高锰酸钾,油浴加热至反应结束。
Ⅱ.将反应液趁热减压过滤,得到滤渣1,滤液呈紫色,加入少量亚硫酸钠使紫色褪去,进行二次减压过滤,得到滤渣2;将滤液放入冰水浴中,然后加酸酸化,有晶体析出,减压过滤,洗涤、干燥,得到苯甲酸晶体。
Ⅲ.回收二氧化锰:将滤渣2和滤纸一并转移到坩埚中,加热灼烧,所得固体与干燥后的滤渣1合并,称重得2.5 g固体。
Ⅳ.二氧化锰纯度的测定:称取0.5g回收的二氧化锰,放于烧杯中,再加入25 mL 0.3 mol·L-1草酸钠溶液及50 mL12 mol·L-1硫酸,加热至二氧化碳不再产生,稀释至250 mL,加热至近沸。趁热以浓度为0.05mol·L-1的高锰酸钾标准液滴定过量的草酸钠,消耗高锰酸钾的体积为16.0mL。
已知:MnO2 + +4H+=Mn2++2CO2↑+2H2O
+4H+=Mn2++2CO2↑+2H2O
回答下列问题:
(1)仪器A的名称为___________ ,
(2)步骤Ⅰ中,判断反应结束的现象是___________ 。
(3)步骤Ⅱ中加酸酸化,加的酸可以是___________ (填序号)。
①稀硫酸 ②盐酸
滤液放入冰水浴的原因是___________ 。
(4)滤渣2的主要成分为MnO(OH)2,请写出生成MnO(OH)2的离子方程式:___________ 。
(5)二氧化锰的纯度为___________ %。
苯甲酸实验室制备原理为:
 +2KMnO4
+2KMnO4
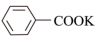 +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O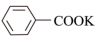


实验装置如图所示。

已知:甲苯的密度是0.872g·L-1;苯甲酸微溶于冷水,溶于热水。
实验步骤:
Ⅰ.在50mL三颈烧瓶中加入1.5mL甲苯、20mL水和5.0g高锰酸钾,油浴加热至反应结束。
Ⅱ.将反应液趁热减压过滤,得到滤渣1,滤液呈紫色,加入少量亚硫酸钠使紫色褪去,进行二次减压过滤,得到滤渣2;将滤液放入冰水浴中,然后加酸酸化,有晶体析出,减压过滤,洗涤、干燥,得到苯甲酸晶体。
Ⅲ.回收二氧化锰:将滤渣2和滤纸一并转移到坩埚中,加热灼烧,所得固体与干燥后的滤渣1合并,称重得2.5 g固体。
Ⅳ.二氧化锰纯度的测定:称取0.5g回收的二氧化锰,放于烧杯中,再加入25 mL 0.3 mol·L-1草酸钠溶液及50 mL12 mol·L-1硫酸,加热至二氧化碳不再产生,稀释至250 mL,加热至近沸。趁热以浓度为0.05mol·L-1的高锰酸钾标准液滴定过量的草酸钠,消耗高锰酸钾的体积为16.0mL。
已知:MnO2 +
 +4H+=Mn2++2CO2↑+2H2O
+4H+=Mn2++2CO2↑+2H2O 回答下列问题:
(1)仪器A的名称为
(2)步骤Ⅰ中,判断反应结束的现象是
(3)步骤Ⅱ中加酸酸化,加的酸可以是
①稀硫酸 ②盐酸
滤液放入冰水浴的原因是
(4)滤渣2的主要成分为MnO(OH)2,请写出生成MnO(OH)2的离子方程式:
(5)二氧化锰的纯度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】过碳酸钠(2 Na2CO3·3 H2O2)广泛用于化工、造纸、纺织、食品等行业,一种以芒硝(Na2SO4·10 H2 O)、H2O2等为原料制备过碳酸钠的工艺流程如下:
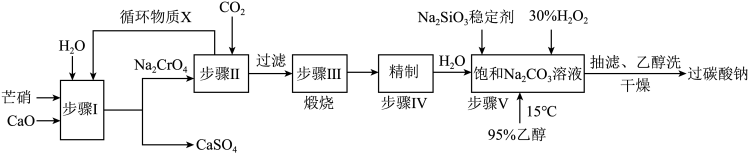
已知2CrO42-+2H+=Cr2O72-+H2O , pH小于5时几乎均以Cr2O72-形式存在,pH大于8.5时几乎均以CrO42-形式存在。
回答下列问题:
(1)Na2CrO4中Cr元素的化合价为___
(2)Ksp(CaCrO4)___ (填“>”或“<”)Ksp(CaSO4)。
(3)流程中循环物质X为___ (填化学式)。
(4)步骤II中发生反应的化学方程式为_________
(5)步骤I一III是为了制得纯碱,从环境保护的角度看,可能的不足之处是___
(6)步骤V合成时,加入95%的乙醇的目的是___
(7)测定产品活性氧的实验步骤如下:准确称取mg产品,用硫酸溶解后,用c mol·L-1的KMnO4标准溶液滴定至终点,消耗KMnO4标准溶液V mL。
①滴定到终点时,溶液呈___ (填“无色”或“浅红色”)。
②过氧化物的活性氧是指过氧化物单独用催化剂催化分解时放出氧气的质量与样品的质量之比。该实验测得的产品中活性氧为___ (列出计算表达式)。

已知2CrO42-+2H+=Cr2O72-+H2O , pH小于5时几乎均以Cr2O72-形式存在,pH大于8.5时几乎均以CrO42-形式存在。
回答下列问题:
(1)Na2CrO4中Cr元素的化合价为
(2)Ksp(CaCrO4)
(3)流程中循环物质X为
(4)步骤II中发生反应的化学方程式为
(5)步骤I一III是为了制得纯碱,从环境保护的角度看,可能的不足之处是
(6)步骤V合成时,加入95%的乙醇的目的是
(7)测定产品活性氧的实验步骤如下:准确称取mg产品,用硫酸溶解后,用c mol·L-1的KMnO4标准溶液滴定至终点,消耗KMnO4标准溶液V mL。
①滴定到终点时,溶液呈
②过氧化物的活性氧是指过氧化物单独用催化剂催化分解时放出氧气的质量与样品的质量之比。该实验测得的产品中活性氧为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】硫酸是工农业生产的重要化工原料。以黄铁矿(FeS2)为原料生产硫酸的工艺流程如下图所示。_______ 。
(2)黄铁矿燃烧主要经过以下两个过程:
Ⅰ.分解:2FeS2 2FeS+S2
2FeS+S2
Ⅱ.燃烧:4FeS+7O2 2Fe2O3+4SO2、
2Fe2O3+4SO2、_______ 。
(3)98.3%浓硫酸吸收SO3,反应的化学方程式为_______ 。
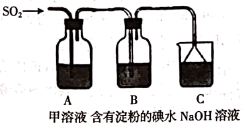
(4)硫酸工业尾气经处理后排空。空气中二氧化硫的简易测定方法如下图所示。_______ 色。
②连接仪器,在测定地点慢慢抽气,每次抽气100mL,直到溶液的颜色全部褪尽为止,共抽气n次。
a.抽气时溶液褪色,反应的化学方程式是_______ 。
b.空气中二氧化硫的含量为_______ mg·L﹣1。
③若空气中二氧化硫的允许含量以0.02mg·L﹣1为标准,则抽气次数n≥_______ 次才符合标准,否则超标。

(2)黄铁矿燃烧主要经过以下两个过程:
Ⅰ.分解:2FeS2
 2FeS+S2
2FeS+S2Ⅱ.燃烧:4FeS+7O2
 2Fe2O3+4SO2、
2Fe2O3+4SO2、(3)98.3%浓硫酸吸收SO3,反应的化学方程式为
(4)硫酸工业尾气经处理后排空。空气中二氧化硫的简易测定方法如下图所示。
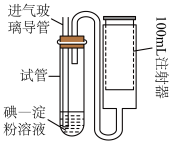
②连接仪器,在测定地点慢慢抽气,每次抽气100mL,直到溶液的颜色全部褪尽为止,共抽气n次。
a.抽气时溶液褪色,反应的化学方程式是
b.空气中二氧化硫的含量为
③若空气中二氧化硫的允许含量以0.02mg·L﹣1为标准,则抽气次数n≥
您最近一年使用:0次




