某课外兴趣小组为了探究碱性溶液中Mg2+、AlO2-与溶液pH的关系,进行下列实验:向含有0.1 mol HCl、0.1 mol MgCl2、1.0 mol AlCl3的混合溶液中逐渐加入NaOH溶液,均至反应后溶液体积1 L。测得部分实验数据如下表:
试回答:
(1)向混合溶液中加入NaOH溶液至pH=9,能否有Mg(OH)2沉淀出现__________ (填“能”或“否”),由此你得到的初步结论是___________________________________ 。
(2)向混合溶液中加入NaOH溶液至pH=10,需要NaOH溶液中有多少克NaOH?(最后结果保留两位小数)______
| pH | 9 | 10 | 11 |
| c(Mg2+)/ mol·L-1 | 10-1 | 10-3 | 10-5 |
| c(AlO2-)/mol·L-1 | 10-2 | 10-1 | 1 |
试回答:
(1)向混合溶液中加入NaOH溶液至pH=9,能否有Mg(OH)2沉淀出现
(2)向混合溶液中加入NaOH溶液至pH=10,需要NaOH溶液中有多少克NaOH?(最后结果保留两位小数)
8-9高三·上海奉贤·期末 查看更多[1]
(已下线)上海市奉贤区2010届高三摸底测试化学试题
更新时间:2020-04-01 13:09:49
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】(1)3.1 g Na2X含有Na+ 0.1 mol,则Na2X的摩尔质量为________ ,X的相对原子质量为________ 。
(2)同温同压下,同体积的甲烷和氢气分子数之比为_______ ,原子个数之比为_____ ,质量之比为_________ ,电子数之比为________ 。
(3)用等体积的0.1 mol·L-1的BaCl2溶液,可使相同体积的Fe2(SO4)3、Na2SO4、Al2(SO4)3三种溶液中的SO42-都恰好完全沉淀,则三种硫酸盐的物质的量浓度之比为_____ 。
(2)同温同压下,同体积的甲烷和氢气分子数之比为
(3)用等体积的0.1 mol·L-1的BaCl2溶液,可使相同体积的Fe2(SO4)3、Na2SO4、Al2(SO4)3三种溶液中的SO42-都恰好完全沉淀,则三种硫酸盐的物质的量浓度之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】(1)在标准状况下,由CO和CO2组成的混合气体8.96L,质量是16g。此混合物中CO和CO2的物质的量之比是_____________ ,CO的体积分数是_____________ ,该混合气体对于氢气的相对密度为________ 。
(2) 1.12g金属铁跟某稀盐酸恰好完全反应,得到100mL溶液,试计算:
①生成的气体在标准状况下的体积是_________________
②反应后所得溶液中溶质的物质的量浓度是______________________
(2) 1.12g金属铁跟某稀盐酸恰好完全反应,得到100mL溶液,试计算:
①生成的气体在标准状况下的体积是
②反应后所得溶液中溶质的物质的量浓度是
您最近一年使用:0次
【推荐3】铜是重要的工业原料,现有Cu、Cu2O组成的混合物,某研究性学习小组为了探究其组成情况,取35.2 g该混合物加入0.5 L 3.6mol/L的稀硝酸中,固体物质完全反应,溶液中铜元素均为Cu2+,且生成4.48 L(标准状况)的NO。向所得溶液中加入a L 2.0 mol/L的NaOH溶液,恰好使溶液中的Cu2+沉淀完全。
(1)Cu与稀硝酸反应的离子方程式为_______ ;
(2)a=_______ L;
(3)求混合物中Cu的质量分数_______ 。
(1)Cu与稀硝酸反应的离子方程式为
(2)a=
(3)求混合物中Cu的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】向含amol NH4Fe(SO4)2和amol NH4HSO4溶液中逐滴加入bmol Ba(OH)2溶液,请计算
⑴当b=1,a=2时,溶液中产生沉淀的质量是___________ g
⑵当b=2.5a时,溶液中产生沉淀的质量是__________________ g(用a或b的表达式表示)
⑴当b=1,a=2时,溶液中产生沉淀的质量是
⑵当b=2.5a时,溶液中产生沉淀的质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】天然水常含有较多钙、镁离子而称之为硬水,硬水软化是指除去钙、镁离子。若某天然水中离子含量如下表:
现要用化学方法软化10m3这种天然水,则需要先加入Ca(OH)2_______ g以除去Mg2+和HCO ,后加入Na2CO3
,后加入Na2CO3_______ g以除去Ca2+(要求写出计算过程)。
| 离子 | Ca2+ | Mg2+ | HCO | 其他 |
| 含量(mol/L) | 1.2×10-3 | 6.0×10-4 | 8.0×10-4 | / |
 ,后加入Na2CO3
,后加入Na2CO3
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】取20mL硫酸和盐酸的混合液体,加入过量的氯化钡溶液,产生4.66g白色沉淀,然后继续向溶液中加入ag(足量)铁粉,产生的气体的体积为896mL(标准状况下)。
(1)写出上述过程中发生的离子方程式_______________________________________
________________________________________________________________________ 。
(2)计算原混合液体中,硫酸物质的量浓度是_________________ mol/L,盐酸物质的量浓度是_____________________ mol/L(写出计算过程)。
(1)写出上述过程中发生的离子方程式
(2)计算原混合液体中,硫酸物质的量浓度是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】我国《生活饮用水卫生标准》中规定生活用水中锅的排放量不超过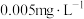 。处理含镉废水可采用化学沉淀法。
。处理含镉废水可采用化学沉淀法。
(1)写出磷酸镉 沉淀溶解平衡常数的表达式:
沉淀溶解平衡常数的表达式: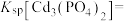
____________ 。
(2)一定温度下, 的
的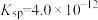 ,
, 的
的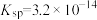 ,该温度下
,该温度下____________ [填“ ”或“
”或“ ”]的饱和溶液中
”]的饱和溶液中 浓度较大。
浓度较大。
(3)向某含镉废水中加入 ,当
,当 浓度达到
浓度达到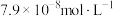 时,废水中
时,废水中 的浓度为
的浓度为_________________  [已知:
[已知: ,此时
,此时____________ (填“符合”或“不符合”)《生活饮用水卫生标准》。
(4)常温下,向50 mL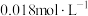 的
的 溶液中加入50 mL
溶液中加入50 mL  的盐酸,生成沉淀。已知该温度下,
的盐酸,生成沉淀。已知该温度下, ,忽略溶液体积的变化。
,忽略溶液体积的变化。
①反应后,溶液的pH=__________________
②如果向反应后的溶液中继续加入50 mL 的盐酸,
的盐酸,______ (填“有”或“无”)白色沉淀生成。
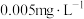 。处理含镉废水可采用化学沉淀法。
。处理含镉废水可采用化学沉淀法。(1)写出磷酸镉
 沉淀溶解平衡常数的表达式:
沉淀溶解平衡常数的表达式: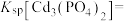
(2)一定温度下,
 的
的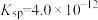 ,
, 的
的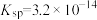 ,该温度下
,该温度下 ”或“
”或“ ”]的饱和溶液中
”]的饱和溶液中 浓度较大。
浓度较大。(3)向某含镉废水中加入
 ,当
,当 浓度达到
浓度达到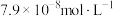 时,废水中
时,废水中 的浓度为
的浓度为 [已知:
[已知: ,此时
,此时(4)常温下,向50 mL
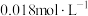 的
的 溶液中加入50 mL
溶液中加入50 mL  的盐酸,生成沉淀。已知该温度下,
的盐酸,生成沉淀。已知该温度下, ,忽略溶液体积的变化。
,忽略溶液体积的变化。①反应后,溶液的pH=
②如果向反应后的溶液中继续加入50 mL
 的盐酸,
的盐酸,
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】(1)已知在25℃时,Ksp[Mg(OH)2]=3.2×10-11,假设饱和Mg(OH)2溶液的浓度为1 g/mL,则Mg(OH)2的溶解度为_________ g。
(2)在25℃时,向0.02 mol•L-1的MgCl2溶液中加入NaOH固体,如要生成Mg(OH)2沉淀,应使溶液中的c(OH-)最小为__ mol•L-1。
(3)25℃时,向浓度均为0.02mol•L﹣1的MgCl2和CuCl2混合溶液中逐滴加入NaOH溶液,先生成沉淀__ (填化学式);当两种沉淀共存时,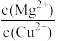 =
=__ 。(已知25℃时,Ksp[Cu(OH)2]=2.2×10-20)(每个小题都写出计算过程)
(2)在25℃时,向0.02 mol•L-1的MgCl2溶液中加入NaOH固体,如要生成Mg(OH)2沉淀,应使溶液中的c(OH-)最小为
(3)25℃时,向浓度均为0.02mol•L﹣1的MgCl2和CuCl2混合溶液中逐滴加入NaOH溶液,先生成沉淀
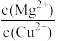 =
=
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】(1)已知Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=2.6×10-39。常温下,某酸性CuCl2溶液中含有少量的FeCl3,为了得到纯净的CuCl2·2H2O晶体,应加入___________ (填氧化物的化学式),调节溶液的pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=________ 。过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2·2H2O晶体。
(2)某碳素钢锅炉内水垢的主要成分是碳酸钙、硫酸钙、氢氧化镁、铁锈、二氧化硅等。水垢需及时清洗除去。清洗流程如下:
Ⅰ.加入NaOH和Na2CO3混合液,加热,浸泡数小时;
Ⅱ.放出洗涤废液,清水冲洗锅炉,加入稀盐酸和少量NaF溶液,浸泡;
Ⅲ.向洗涤液中加入Na2SO3溶液;
Ⅳ.清洗达标,用NaNO2溶液钝化锅炉。
①用稀盐酸溶解碳酸钙的离子方程式是_____________________________ 。
②已知:25 ℃时有关物质的溶度积
根据数据,结合化学平衡原理解释清洗CaSO4的过程________________ 。(用溶解平衡表达式和必要的文字叙述加以说明);在步骤Ⅰ浸泡过程中还会发生反应MgCO3(s)+2OH-(aq) Mg(OH)2(s)+CO32-(aq),该反应的平衡常数K=
Mg(OH)2(s)+CO32-(aq),该反应的平衡常数K=________ (保留两位有效数字)。
③步骤Ⅲ中,加入Na2SO3溶液的目的是_______________________________ 。
(2)某碳素钢锅炉内水垢的主要成分是碳酸钙、硫酸钙、氢氧化镁、铁锈、二氧化硅等。水垢需及时清洗除去。清洗流程如下:
Ⅰ.加入NaOH和Na2CO3混合液,加热,浸泡数小时;
Ⅱ.放出洗涤废液,清水冲洗锅炉,加入稀盐酸和少量NaF溶液,浸泡;
Ⅲ.向洗涤液中加入Na2SO3溶液;
Ⅳ.清洗达标,用NaNO2溶液钝化锅炉。
①用稀盐酸溶解碳酸钙的离子方程式是
②已知:25 ℃时有关物质的溶度积
| 物质 | CaCO3 | CaSO4 | Mg(OH)2 | MgCO3 |
| Ksp | 2.8×10-9 | 9.1×10-6 | 1.8×10-11 | 6.8×10-6 |
 Mg(OH)2(s)+CO32-(aq),该反应的平衡常数K=
Mg(OH)2(s)+CO32-(aq),该反应的平衡常数K=③步骤Ⅲ中,加入Na2SO3溶液的目的是
您最近一年使用:0次



