纯碱工业始于 18 世纪末,至今已有两百多年。在纯碱工业史上,比利时人索尔维,中国人侯德榜等都作出了突出的贡献。据此完成下面小题。
1.下图是1861年索尔维发明的制碱法中物质转化关系图,其中I~IV代表四个主要化学反应,a~i代表除H2O以外不同的物质。若不计其他损耗,,下列说法正确的是( )
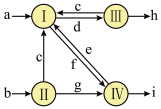
2.从母液中析出的NaHCO3中含有NH4Cl,需洗涤后再进行灼烧。若省略洗涤操作,则最终对所得纯碱纯度影响叙述正确的是( )
3.化工专家侯德榜发明的"侯氏制碱法"大大推进了纯碱工业的发展,其最重要贡献是( )
1.下图是1861年索尔维发明的制碱法中物质转化关系图,其中I~IV代表四个主要化学反应,a~i代表除H2O以外不同的物质。若不计其他损耗,,下列说法正确的是( )

| A.水溶液呈碱性的物质只有e、g、h |
| B.水溶液呈酸性的物质只有c、f、i |
| C.每消耗1mol a,同时消耗0.5mol b |
| D.每消耗1mol h,同时消耗0.5mol i |
| A.无明显影响 | B.NH4Cl杂质含量上升 |
| C.NaCl杂质含量上升 | D.NaOH杂质含量上升 |
| A.找到了新型高效的催化剂 | B.充分利用了能量 |
| C.提高了纯碱产品的纯度 | D.提升了Na+的利用率 |
更新时间:2020-04-03 10:50:11
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】(1)物质的量浓度均为0.1 mol/L的下列溶液:①NH4Cl、②Na2CO3、③NaHCO3、④NaHSO4、⑤CH3COOH、⑥NaOH,pH由大到小的顺为: _______ (填数字代号)
(2)氢气燃烧热值高。实验测得,在常温常压下,1 g H2完全燃烧生成液态水,放出142.9 kJ热量。则H2燃烧的热化学方程式为_______ 。
(3)常温下,0.1 mol/L的NaHCO3溶液的pH大于8,则溶液中C(H2CO3)_______ C( CO ) (填>、=或<),原因
) (填>、=或<),原因_______ (用离子方程式和必要的文字说明)
(4)常温下,pH=a某强酸溶液V1 L,pH=b某强碱溶液V2 L,已知a+b=12,两溶液混合后pH=7,求V1 和V2的关系______
(5)25℃下,某Na2SO4溶液中c(SO )=5×10-4 mol·L-1,取该溶液1 mL,加水稀释至10 mL,则稀释后溶液中c (Na+)∶c (OH-)=
)=5×10-4 mol·L-1,取该溶液1 mL,加水稀释至10 mL,则稀释后溶液中c (Na+)∶c (OH-)=_______
(6)常温下,已知Ksp(Mg(OH)2)=1.8×10-11,则Mg(OH)2在pH=12.00的NaOH溶液中的Mg2+浓度为_______ mol·L-1
(2)氢气燃烧热值高。实验测得,在常温常压下,1 g H2完全燃烧生成液态水,放出142.9 kJ热量。则H2燃烧的热化学方程式为
(3)常温下,0.1 mol/L的NaHCO3溶液的pH大于8,则溶液中C(H2CO3)
 ) (填>、=或<),原因
) (填>、=或<),原因(4)常温下,pH=a某强酸溶液V1 L,pH=b某强碱溶液V2 L,已知a+b=12,两溶液混合后pH=7,求V1 和V2的关系
(5)25℃下,某Na2SO4溶液中c(SO
 )=5×10-4 mol·L-1,取该溶液1 mL,加水稀释至10 mL,则稀释后溶液中c (Na+)∶c (OH-)=
)=5×10-4 mol·L-1,取该溶液1 mL,加水稀释至10 mL,则稀释后溶液中c (Na+)∶c (OH-)=(6)常温下,已知Ksp(Mg(OH)2)=1.8×10-11,则Mg(OH)2在pH=12.00的NaOH溶液中的Mg2+浓度为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】电解饱和食盐水,可以有效的利用海水资源,下图是电解饱和氯化钠溶液的示意图。

(1)电解饱和氯化钠溶液的离子方程式为_____ 。
(2)电极A接电源的_____ (填“正”或“负”极。饱和氯化钠溶液从_____ (填a或c)口进入, 溶液从
溶液从_____ (填b或d)口导出。
(3)阳离子交换膜的作用是_____ 。
某研究小组用微生物电池模拟淡化海水,同时做电解实验,实验装置如图所示,C、D是铂电极。已知:苯酚的分子式为 。
。

(4)丙装置中D电极为_____ 极。(填“阴”或“阳”或“正”或“负”)。
(5)若乙是铁片镀铜装置,A、B质量相同。A电极材料:_____ ;当B和A的质量差为 时,丙装置中C极产生的气体在标准状况下的体积是
时,丙装置中C极产生的气体在标准状况下的体积是_____ L。
(6)甲装置中:
①a极的电极反应式为_____ 。(苯酚用分子式表示)
②理论上每消除 苯酚,同时消除
苯酚,同时消除_____  。
。

(1)电解饱和氯化钠溶液的离子方程式为
(2)电极A接电源的
 溶液从
溶液从(3)阳离子交换膜的作用是
某研究小组用微生物电池模拟淡化海水,同时做电解实验,实验装置如图所示,C、D是铂电极。已知:苯酚的分子式为
 。
。
(4)丙装置中D电极为
(5)若乙是铁片镀铜装置,A、B质量相同。A电极材料:
 时,丙装置中C极产生的气体在标准状况下的体积是
时,丙装置中C极产生的气体在标准状况下的体积是(6)甲装置中:
①a极的电极反应式为
②理论上每消除
 苯酚,同时消除
苯酚,同时消除 。
。
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】已知20℃下,饱和食盐水质量分数为26.5%,密度为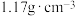 。用惰性电极电解50mLNaCl饱和溶液,分别收集两极气体,一段时间后,测定装置中溶液密度变为1.024
。用惰性电极电解50mLNaCl饱和溶液,分别收集两极气体,一段时间后,测定装置中溶液密度变为1.024 。不考虑溶液体积的变化、水气挥发、气体的溶解。请回答:
。不考虑溶液体积的变化、水气挥发、气体的溶解。请回答:
(1)该饱和食盐水的物质的量浓度为___________  。
。
(2)所得 理论上可制得漂白粉有效成分的质量为:
理论上可制得漂白粉有效成分的质量为:___________ g。(写出计算过程)
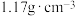 。用惰性电极电解50mLNaCl饱和溶液,分别收集两极气体,一段时间后,测定装置中溶液密度变为1.024
。用惰性电极电解50mLNaCl饱和溶液,分别收集两极气体,一段时间后,测定装置中溶液密度变为1.024 。不考虑溶液体积的变化、水气挥发、气体的溶解。请回答:
。不考虑溶液体积的变化、水气挥发、气体的溶解。请回答:(1)该饱和食盐水的物质的量浓度为
 。
。(2)所得
 理论上可制得漂白粉有效成分的质量为:
理论上可制得漂白粉有效成分的质量为:
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】电化学知识在物质制备领域的应用前景看好。
(1)利用反应6NO2+8NH3= 7N2 + 12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示。

①A电极的电极反应式为___________ 。
②下列关于该电池的说法正确的是___________ 。
A.电子从右侧电极经过负载后流向左侧电极
B.为使电池持续放电,离子交换膜需选用阴离子交换膜
C.电池工作一段时间,溶液的pH不变
D.当有4.48LNO2被处理时,转移电子物质的量为0.8mol
(2)以甲烷为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池,目前得到广泛的研究,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:

①B极上的电极反应式为___________ 。
②若用该燃料电池作电源,用石墨作电极电解硫酸铜溶液,当阳极收集到11.2 L(标准状况)气体时,消耗甲烷的体积为___________ L(标准状况下)。
(3)阳离子交换膜法电解饱和食盐水具有综合能耗低、环境污染小等优点。生产流程如下图所示:

①电解饱和食盐水的化学方程式为___________ 。
②电解结束后,能够脱去阳极液中游离氯的试剂或方法是___________ (填字母序号)。
A.Na2SO4 B.Na2SO3
C.热空气吹出 D.降低阳极区液面上方的气压
(4)按如图1所示装置进行电解,A、B、C、D均为铂电极,回答下列问题。

已知一:甲槽电解的是200 mL一定浓度的NaCl与CuSO4的混合溶液,理论上两极所得气体体积随时间变化的关系如图2所示(气体体积已换算成标准状况下的体积,电解前后溶液的体积变化忽略不计)。
①原混合溶液中NaCl的物质的量浓度为___________ mol·L-1,CuSO4的物质的量浓度为___________ mol·L-1。
已知二:乙槽为200 mL CuSO4溶液:
②当C极析出0.64 g物质时,乙槽溶液中生成的H2SO4为___________ mol。电解后,若使乙槽内的溶液完全复原,可向乙槽中加入___________ 。
A.Cu(OH)2 B.CuO C.CuCO3 D.Cu2(OH)2CO3
③若通电一段时间后,向所得的乙槽溶液中加入0.2 mol的Cu(OH)2才能恰好恢复到电解前的浓度,则电解过程中转移的电子数为___________ (用NA表示)。
(1)利用反应6NO2+8NH3= 7N2 + 12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示。

①A电极的电极反应式为
②下列关于该电池的说法正确的是
A.电子从右侧电极经过负载后流向左侧电极
B.为使电池持续放电,离子交换膜需选用阴离子交换膜
C.电池工作一段时间,溶液的pH不变
D.当有4.48LNO2被处理时,转移电子物质的量为0.8mol
(2)以甲烷为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池,目前得到广泛的研究,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:

①B极上的电极反应式为
②若用该燃料电池作电源,用石墨作电极电解硫酸铜溶液,当阳极收集到11.2 L(标准状况)气体时,消耗甲烷的体积为
(3)阳离子交换膜法电解饱和食盐水具有综合能耗低、环境污染小等优点。生产流程如下图所示:

①电解饱和食盐水的化学方程式为
②电解结束后,能够脱去阳极液中游离氯的试剂或方法是
A.Na2SO4 B.Na2SO3
C.热空气吹出 D.降低阳极区液面上方的气压
(4)按如图1所示装置进行电解,A、B、C、D均为铂电极,回答下列问题。

已知一:甲槽电解的是200 mL一定浓度的NaCl与CuSO4的混合溶液,理论上两极所得气体体积随时间变化的关系如图2所示(气体体积已换算成标准状况下的体积,电解前后溶液的体积变化忽略不计)。
①原混合溶液中NaCl的物质的量浓度为
已知二:乙槽为200 mL CuSO4溶液:
②当C极析出0.64 g物质时,乙槽溶液中生成的H2SO4为
A.Cu(OH)2 B.CuO C.CuCO3 D.Cu2(OH)2CO3
③若通电一段时间后,向所得的乙槽溶液中加入0.2 mol的Cu(OH)2才能恰好恢复到电解前的浓度,则电解过程中转移的电子数为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】氨和硝酸都是重要的化学品。
(1)画出采用氨催化氧化法合成硝酸的反应原理流程图:(要求注明试剂、反应条件)___
(示例: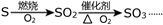 )
)
(2)向饱和氯化钠和浓氨水的混合溶液中通入过量CO2从而析出NaHCO3晶体,是侯氏制碱法的关键步骤,用一个化学方程式表示该反应原理_________________________________ 。在0.1 mol/L的稀氨水中,下列式子成立的是____________ 。
(3)A是中学化学常见气体,打开装有A的集气瓶,瓶口出现白雾,将A与氨气混合,立即出现大量白烟,生成物质B,则A的分子式为_________ ,物质B中所含的化学键类型有____________ 。
(4)将6.4 g铜粉投入一定量的浓硝酸中,铜完全溶解,产生标准状况下的混合气体3.36 L,其中两种成分气体的体积比为__________ ,反应中总共消耗的硝酸_______________ mol。
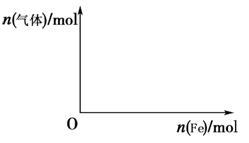
(5)向含4 mol HNO3的稀溶液中,逐渐加入铁粉至过量。假设生成的气体只有一种,请在坐标系中画出n(气体)随n(Fe)变化的示意图,并标出n(气体)的最大值_______ 。
(6)氨气和硝酸生产的氮肥硝酸铵受热或受撞击容易分解,若分解时只生成两种氧化物,写出该反应的化学方程式_________________________ 。
(1)画出采用氨催化氧化法合成硝酸的反应原理流程图:(要求注明试剂、反应条件)
(示例:
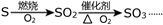 )
)(2)向饱和氯化钠和浓氨水的混合溶液中通入过量CO2从而析出NaHCO3晶体,是侯氏制碱法的关键步骤,用一个化学方程式表示该反应原理
| A.c(NH3·H2O) + c(NH3) + c(NH4+) =0.1 mol/L |
| B.c(NH3·H2O) > c(NH3) + c(NH4+) |
| C.c(H+) > c(OH-) |
| D.c(NH4+) + c(H+) = c(OH-) |
(3)A是中学化学常见气体,打开装有A的集气瓶,瓶口出现白雾,将A与氨气混合,立即出现大量白烟,生成物质B,则A的分子式为
(4)将6.4 g铜粉投入一定量的浓硝酸中,铜完全溶解,产生标准状况下的混合气体3.36 L,其中两种成分气体的体积比为
(5)向含4 mol HNO3的稀溶液中,逐渐加入铁粉至过量。假设生成的气体只有一种,请在坐标系中画出n(气体)随n(Fe)变化的示意图,并标出n(气体)的最大值

(6)氨气和硝酸生产的氮肥硝酸铵受热或受撞击容易分解,若分解时只生成两种氧化物,写出该反应的化学方程式
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】焦亚硫酸钠(Na2S2O5)常用作食品漂白剂。其制备工艺流程如下:

已知:反应Ⅱ包含2NaHSO3 Na2S2O5+H2O等多步反应。
Na2S2O5+H2O等多步反应。
(1)实验室制取氨气的化学方程式:____________________________________________ 。
(2)“灼烧”时发生反应的化学方程式:__________________________________________ 。
(3)已知Na2S2O5与稀硫酸反应放出SO2,其离子方程式为:________________________ 。
(4)副产品X的化学式是:____________ ;可循环利用的物质是:__________________ 。
(5)为了减少产品Na2S2O5中杂质含量,需控制反应Ⅱ中气体与固体的物质的量之比约为_______ 。

已知:反应Ⅱ包含2NaHSO3
 Na2S2O5+H2O等多步反应。
Na2S2O5+H2O等多步反应。(1)实验室制取氨气的化学方程式:
(2)“灼烧”时发生反应的化学方程式:
(3)已知Na2S2O5与稀硫酸反应放出SO2,其离子方程式为:
(4)副产品X的化学式是:
(5)为了减少产品Na2S2O5中杂质含量,需控制反应Ⅱ中气体与固体的物质的量之比约为
您最近一年使用:0次
填空题
|
较难
(0.4)
真题
【推荐3】工业上可用食盐和石灰石为主要原料,经不同的方法生产纯碱。请回答下列问题:
(1)卢布兰芳是以食盐、石灰石、浓硫酸、焦炭为原料,在高温下进行煅烧,再浸取,结晶而制得纯碱。
①食盐和浓硫酸反应的化学方程式为__________________ ;
②硫酸钠和焦炭、石灰石反应的化学方程式为___________________ (已知产物之一为CaS);
(2)氨碱法的工艺如下图所示,得到的碳酸氢钠经煅烧生成纯碱。
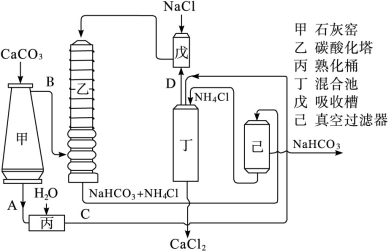
①图中的中间产物C是_______ ,D_______ 。(写化学式);
②装置乙中发生反应的化学方程式为_________________ ;
(3)联合制碱法对氨碱法的改进,其优点是____________________ ;
(4)有人认为碳酸氢钾与碳酸氢钠的化学性质相似,故也可用氨碱法以氯化钾和石灰石为原料制碳酸钾。请结合下图的溶解度(S)随温度变化曲线,分析说明是否可行____________________ ?

(1)卢布兰芳是以食盐、石灰石、浓硫酸、焦炭为原料,在高温下进行煅烧,再浸取,结晶而制得纯碱。
①食盐和浓硫酸反应的化学方程式为
②硫酸钠和焦炭、石灰石反应的化学方程式为
(2)氨碱法的工艺如下图所示,得到的碳酸氢钠经煅烧生成纯碱。

①图中的中间产物C是
②装置乙中发生反应的化学方程式为
(3)联合制碱法对氨碱法的改进,其优点是
(4)有人认为碳酸氢钾与碳酸氢钠的化学性质相似,故也可用氨碱法以氯化钾和石灰石为原料制碳酸钾。请结合下图的溶解度(S)随温度变化曲线,分析说明是否可行

您最近一年使用:0次




