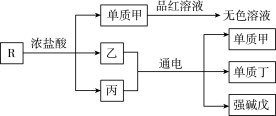
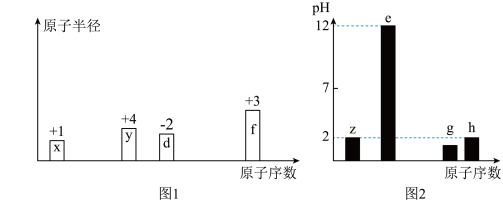
有八种短周期主族元素x、y、z、d、e、f、g、h,其中x、y、d、f随着原子序数的递增,其原子半径的相对大小、最高正价或最低负价的变化如图1所示。 z、e、g、h的最高价氧化物对应水化物溶液(浓度均为0.01mol/L)的pH与原子序数的关系如图2所示。
根据上述信息进行判断,下列说法正确的是( )

根据上述信息进行判断,下列说法正确的是( )
| A.d、e、f、g 形成的简单离子中,半径最大的是d离子 |
| B.d与e形成的化合物中只存在离子键 |
| C.x、y、z、d、e、f、g、h的单质中,f的熔点最高 |
| D.x与y可以形成多种化合物,可能存在非极性共价键 |
2020·山东枣庄·模拟预测 查看更多[5]
宁夏银川市第六中学2022-2023学年高三上学期第二次月考化学试题(已下线)专题07 元素周期表和周期律-备战2023年高考化学母题题源解密(广东卷)(已下线)押广东卷化学第13题 元素周期律-备战2022年高考化学临考题号押题青海省湟川中学2019-2020学年高二下学期期中考试化学试题山东省枣庄三中、高密一中、莱西一中2020届高三下学期第一次在线联考化学试题
更新时间:2020-04-05 15:22:25
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】X、Y、Z、W均为短周期元素,原子序数依次递增.Y元素最外层电子数是电子层数的3倍,Z元素在元素周期表中的周期数等于族序数,Z的简单阳离子与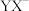 含有相同的电子数,W元素的最外层电子数是最内层电子数的2倍。下列说法不正确的是
含有相同的电子数,W元素的最外层电子数是最内层电子数的2倍。下列说法不正确的是
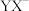 含有相同的电子数,W元素的最外层电子数是最内层电子数的2倍。下列说法不正确的是
含有相同的电子数,W元素的最外层电子数是最内层电子数的2倍。下列说法不正确的是A.X和Y可以组成 型化合物 型化合物 |
B.第一电离能大小: |
C.简单离子半径: |
| D.Z、W的最高价氧化物均具有很高的熔点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】X、Y、Z、W四种主族元素,它们在周期表中位置如图所示,下列说法不正确的是
| X | ||||
| Y | Z | |||
| W |
| A.X元素的气态氢化物稳定性比Y元素强 |
| B.Y、Z、X三种元素的原子半径依次减小,且Z元素的氧化物对应的水化物酸性比Y元素的强 |
| C.化合物YZ4和氢气反应可以生成Y单质 |
| D.W元素与X元素可以形成WX3分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,辛是由C元素形成的单质。已知:甲+乙=丁+辛,甲+丙=戊+辛;常温下0.1 mol/L丁溶液的pH为13。下列说法正确的是
| A.元素B在周期表中的位置为第二周期第VIA族 |
| B.元素B、C、D的原子半径由大到小的顺序为r(D)>r(C)>r(B) |
| C.1.0 L0.1 mol/L戊溶液中阴离子总的物质的量小于0.1 mol |
| D.1 mol甲与足量的乙完全反应共转移了约6.02×1023个电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】化合物A是一种常用的表面活性剂,结构如图所示。已知X、Y、Z、W、M均为短周期常见元素,W是形成物质种类最多的元素,X、Y同族,Z、M同族,Z原子半径在同周期最大。下列说法错误的是


| A.原子半径:Z>Y>X>M |
| B.非金属性:X>Y> W> M |
| C.X、Y、W元素形成的氢化物中沸点最高的是X的氢化物 |
| D.均由X、Y、Z、M四种元素组成常见的两种盐可以发生反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】几种短周期元素的原子半径及主要化合价如表所示:
下列叙述正确的是
| 元素代号 | X | Y | Z | W | H |
| 原子半径/pm | 160 | 143 | 99 | 75 | 74 |
| 主要化合价 | +2 | +3 | +7、-1 | +5、-3 | -2 |
| A.X、Y的最高价氧化物对应水化物的碱性:X<Y |
| B.简单离子的半径:W>H>X>Y>Z |
| C.Y与H形成的化合物能与酸反应,但不能与强碱反应 |
| D.Y与Z形成的化合物为共价化合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】现有6种短周期主族元素:X、Y、Z、M、R和Q,其原子序数依次增大。X的最高化合价和最低化合价代数和为零;Y和R位于同一主族;Z是周期表中非金属性最强的元素;M是同周期中简单离子的半径最小的元素;R的单质为淡黄色粉末,可用于杀菌消毒。下列说法不正确的是
| A.RY2的水溶液能与Q的单质发生反应 |
| B.XYQ2能与水反应产生两种酸性的气体 |
C.M、Z能形成以离子键为主的八面体构型的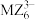 微粒 微粒 |
| D.Q单质能从R的简单氢化物中置换出R |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】W、X、Y是原子序数依次增大的同一短周期元素。W、X是金属元素,它们的最高价氧化物的水化物之间可以反应生成盐和水;Y的最外层电子数是核外电子层数的2倍,W与Y可形成化合物W2Y。下列说法正确的是
| A.Y的低价氧化物与O3漂白的原理相同 |
| B.Y的氢化物和W2Y所含化学键的类型相同 |
| C.上述三种元素形成的简单离子,X离子半径最小 |
| D.工业上常用电解相应的盐溶液制备W、X的单质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】W、X、Y、Z、M为原子序数依次增大的短周期主族元素,W为宇宙中含量最多的元素,X的内层电子数为最外层的一半,Z与M最外层电子数相同,且M的原子序数等于Y与Z的原子序数之和。下列说法正确的是
| A.W与X只能形成一种化合物 | B.第一电离能: (X)< (X)< (Z)< (Z)< (Y) (Y) |
| C.Z和M的最简单氢化物的稳定性:Z>M | D.氧化物对应水化物的酸性:X<M |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】化合物M常用作游泳池消毒剂,其结构如图所示。W、X、Y、Z为原子序数依次增大的短周期主族元素,其中Z的原子序数比Y的原子序数多9,下列说法错误的是
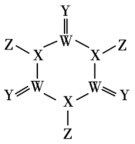

| A.W和Z可形成空间结构为正四面体的化合物 |
| B.最高价含氧酸的酸性:W<X<Z |
| C.简单离子半径:Z>Y>X |
D.X的简单氢化物与 混合后可产生白烟 混合后可产生白烟 |
您最近一年使用:0次