小明同学要测定某大理石样品中碳酸钙的质量分数,决定取一定量的大理石粉末与稀盐酸反应测量生成二氧化碳的质量来完成实验,并设计了两个实验方案(假设二氧化碳全部从溶液中逸出,不考虑盐酸挥发和水的蒸发,杂质不参与化学反应)。
【方案一】用下图装置实验可计算出生成二氧化碳的质量。
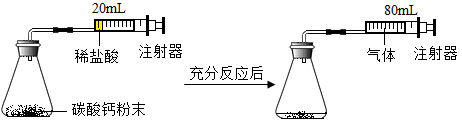
(1)在检查图装置气密性时,小明用双手捧住锥形瓶容器一段时间后再放开,若出现___________ 的现象,则证明气密性良好。
(2)针对以上方案一,下列分析正确的有___________ (填字母编号)。
A.通过测定CO2的体积可计算CO2的质量
B.共生成了80 mL CO2气体
C.注射器中收集到的是纯净的CO2气体
D.反应前后整个装置的质量不变
(3)若实验中外界大气压变大,将导致实验得到的碳酸钙的质量分数比实际值偏___________
(4)若该人理石样品中碳酸钙的质量分数为80%,则图三中天平示数m的值为多少g___________ 。(写出计算过程,CaCO3+2HCl=CaCl2+CO2↑+H2O)

【方案一】用下图装置实验可计算出生成二氧化碳的质量。

(1)在检查图装置气密性时,小明用双手捧住锥形瓶容器一段时间后再放开,若出现
(2)针对以上方案一,下列分析正确的有
A.通过测定CO2的体积可计算CO2的质量

B.共生成了80 mL CO2气体
C.注射器中收集到的是纯净的CO2气体
D.反应前后整个装置的质量不变
(3)若实验中外界大气压变大,将导致实验得到的碳酸钙的质量分数比实际值偏
(4)若该人理石样品中碳酸钙的质量分数为80%,则图三中天平示数m的值为多少g

更新时间:2021-11-07 09:34:33
|
相似题推荐
解答题
|
适中
(0.65)
【推荐1】小金欲测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品5g,把60g稀盐酸分四次加入,实验过程所得数据如下表(已知石灰石样品中含有的杂质不溶于水,也不与稀盐酸反应)。根据实验数据计算:
(1)表中x=_______________ 。
(2)求该实验中稀盐酸中溶质质量分数______________ (书写计算过程,计算结果精确到0.1%)
实验次数 | 1 | 2 | 3 | 4 |
加入稀盐酸的质量/g | 15 | 15 | 15 | 15 |
剩余固体的质量/g | 3.5 | x | 0.75 | 0.75 |
(1)表中x=
(2)求该实验中稀盐酸中溶质质量分数
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】实验室制取二氧化碳的化学方程式为:CaCO3+2HCl==CaCl2+H2O+CO2↑。150克碳酸钙与足量的盐酸反应,可生成二氧化碳多少升?消耗10%的盐酸多少克?(在该条件下,二氧化碳的密度为1.96克/升)
您最近一年使用:0次
解答题
|
适中
(0.65)
名校
【推荐3】化学兴趣小组为了测定一批石灰石样品中碳酸钙的质量分数,称取石灰石样品若干,把200g稀盐酸分4次加入样品中(样品中除碳酸钙外,其余成分不与盐酸反应,也不溶于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下:
(1)从以上数据可推知,m=_______ 。
(2)石灰石样品中碳酸钙的质量分数是_______ 。
(3)求稀盐酸中溶质的质量分数(写出计算过程,结果精确到0.1%)。_______
| 实验序号 | 稀盐酸的用量/g | 剩余固体的质量/g |
| 第一次 | 50 | 10 |
| 第二次 | 50 | 5 |
| 第三次 | 50 | 3 |
| 第四次 | 50 | m |
(2)石灰石样品中碳酸钙的质量分数是
(3)求稀盐酸中溶质的质量分数(写出计算过程,结果精确到0.1%)。
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐1】某盐酸中混有少量的MgCl2,小明为了测定该盐酸混合液中HCI的质量分数,进行如图所示的实验:


请结合图的实验数据,完成以下计算:
(1)坐标中a的数值为________;
(2)所加NaOH溶液的溶质质量分数为________;
(3)该盐酸混合液中HCl的质量分数(写出计算过程)。


请结合图的实验数据,完成以下计算:
(1)坐标中a的数值为________;
(2)所加NaOH溶液的溶质质量分数为________;
(3)该盐酸混合液中HCl的质量分数(写出计算过程)。
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】用以下实验装置进行氢气还原氧化铜,并测定某氯化铜样品的纯度(杂质不与氢气反应)。__________ 。
(2)在丙装置中加入15克氧化铜干燥样品进行实验,完全反应前后装置丙和丁的质量如表:
①小明根据装置丙减少的质量就是氧元素质量,则氧化铜的纯度为__________ 。
②小丽想根据装置丁的质量变化进行计算,请帮小丽求出氧化铜样品的纯度__________ 。(写出计算过程)
(3)比较小明和小丽的计算结果,请分析导致这一结果的原因可能是__________ 。
A.装置气密性不好
B.空气中的水分被丁处浓硫酸吸收
C.通入的氢气量不足
D.空气中的二氧化碳被丁处浓硫酸吸收

(2)在丙装置中加入15克氧化铜干燥样品进行实验,完全反应前后装置丙和丁的质量如表:
装置丙 | 装置丁 | |
反应前 | 48.8克 | 161.2克 |
反应后 | 46.5克 | 163.9克 |
②小丽想根据装置丁的质量变化进行计算,请帮小丽求出氧化铜样品的纯度
(3)比较小明和小丽的计算结果,请分析导致这一结果的原因可能是
A.装置气密性不好
B.空气中的水分被丁处浓硫酸吸收
C.通入的氢气量不足
D.空气中的二氧化碳被丁处浓硫酸吸收
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐3】实验室有一瓶敞口放置一段时间的氢氧化钠固体,为测定这瓶样品中氢氧化钠的质量分数,做如下实验:现取M克样品放入盛有足量水的烧杯中(充分溶解),向烧杯中逐滴加入200克一定溶质质量分数的稀盐酸。该过程中发生反应的化学方程式为:
Na2CO3+2HCl=2NaCl+H2O+CO2↑ NaOH+HCl=NaCl+H2O
实验数据如图所示。试分析计算回答;
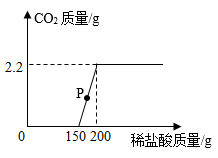
(1)与P点对应的溶液溶质是_______ 。
(2)样品中氢氧化钠的质量分数为多少?(精确到0.1%)_______
在往烧杯中逐滴加入稀盐酸的过程中,烧杯中溶液各个量随盐酸质量的变化图像如图所示,则正确的有_________ (可多选)。
A.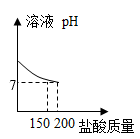 B.
B. 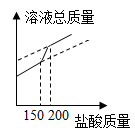
C.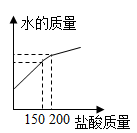 D.
D. 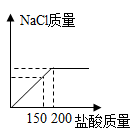
Na2CO3+2HCl=2NaCl+H2O+CO2↑ NaOH+HCl=NaCl+H2O
实验数据如图所示。试分析计算回答;

(1)与P点对应的溶液溶质是
(2)样品中氢氧化钠的质量分数为多少?(精确到0.1%)
在往烧杯中逐滴加入稀盐酸的过程中,烧杯中溶液各个量随盐酸质量的变化图像如图所示,则正确的有
A.
 B.
B. 
C.
 D.
D. 
您最近一年使用:0次



