24. 硫酸亚铁铵晶体【(NH
4)
2Fe(SO
4)
2·6H
2O】是一种重要的工业原料,易溶于水,不溶于乙醇。将硫酸亚铁溶液与硫酸铵溶液混合很容易制得硫酸亚铁铵晶体。某班级分小组拟在实验室制备硫酸亚铁铵晶体。
已知:a.FeSO
4在空气中容易被氧化为Fe
2(SO
4)
3;
b.含Fe
3+的溶液中滴加硫氮化钾(KSCN)溶液,溶液会呈现血红色;含Fe
2+的溶液中滴加硫氰化钾溶液,无明显现象。
c.相关物质的溶解度曲线如下图。

I.甲小组设计了如下流程制备硫酸亚铁铵晶体:
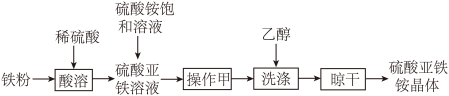
(1)加快“酸溶”速率的方法有是
________。
(2)“操作甲”应进行蒸发浓缩、冷却结晶、趁热过滤,此时“趁热过滤”适宜的温度约为
________。
(3)使用乙醇进行“洗涤”的优点有:①
_________;②
________。
Ⅱ.乙小组研究了相关资料后,设计如下实验装置制备少量硫酸亚铁铵晶体,实验步骤为:
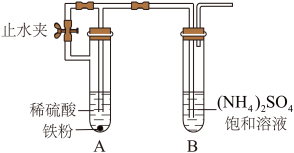
①按照图示搭好实验装置,检查装置气密性良好;
②先向B中加入一定量(NH
4)
2SO
4饱和溶液,再向A的试管中加入一定量铁粉,再迅速加入足量稀硫酸,塞好塞子,打开止水夹,B中溶液下的导管口有持续的气泡冒出;
③一段时间后,关闭止水夹,A中的浅绿色溶液经由导管进入B中,B中出现浅蓝绿色的硫酸亚铁铵晶体。
(4)步骤②,将产生的氢气向B中持续通入一段时间,其目的是
________。
(5)步骤③中,关闭止水夹后,A中的浅绿色溶液能够进入B中的原因是
________。
Ⅲ.丙小组对硫酸亚铁铵晶体进行组成检验
(6)为验证所得产品中可能含有Fe
3+,于是分别取甲、乙两小组所得晶体少许,加蒸馏水溶解后,
_________,证明甲小组所得硫酸亚铁铵晶体含Fe
3+;而乙小组的晶体溶液中没有明显现象。
(7)取乙小组所得晶体少许,加蒸馏水溶解后,分为两份。
①取其中一份,
_________,则证明晶体中含有

;
②取另一份,加入
_________,出现
________现象,则可证明晶体中含有

。