28. 铁及其化合物的广泛应用
(一)铁的广泛应用
(1)金属与人体健康息息相关,人体中的铁元素属于
_______(“常量”或“微量”)元素,作用
_______。而人体中含量最多的金属是
_______(元素名称)
(2)铁制炊具加热食物,说明铁具有的性质是
_______。
(3)某婴儿米粉中含有少量铁粉,食用后与胃酸(主要成分为盐酸)发生的化学方程式
_______,帮助补充铁元素。
(二)草酸亚铁晶体组成的测定
草酸亚铁晶体(化学式为FeC
2O
4·xH
2O)是一种淡黄色晶体粉末。
【当x=1时,
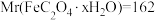
;当x=2时,
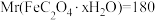
;当x=3时,

;当x=4时,
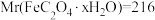
;当x=5时,
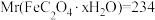
;当x=6时,
】
【查阅资料】
①白色的无水CuSO
4遇水变蓝;
②CO能与氯化钯(PdCl
2)溶液反应生成黑色的钯粉;
③FeO和Fe
3O
4都是黑色物质,FeO在空气中不稳定,易被氧化。
草酸亚铁晶体受热分解生成四种氧化物,为确定分解产物及x的值,设计了如下实验进行探究:(装置C、D、E中药品均足量)
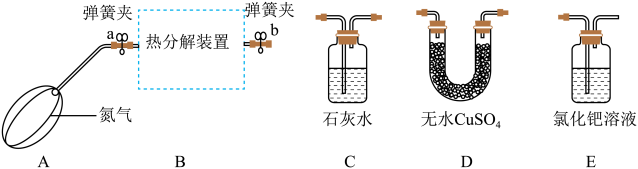
【实验步骤】
(4)①按照气流从左至右的方向,上图装置连接顺序为A→B→
_______→E,连接好装置后,
_______;
②在装置B中装入称量好的草酸亚铁晶体,打开弹簧夹a、b,鼓入一段时间氮气,称装置D的质量;
③用酒精灯加热B装置,直至晶体完全变成黑色,停止加热;
④继续通氮气至装置冷却,关闭弹簧夹a、b;
⑤再次称量装置B中固体质量、装置D的质量。
【进行实验】该小组同学按上述实验步骤进行实验,并记录了如下数据:
| 装置B中固体质量(/g) | 装置D的质量(/g) |
| 实验前 | 9.0 | 168.2 |
| 实验后 | 3.6 | 170.0 |
【实验分析及数据处理】
(5)加热前先鼓入一段时间氮气的目的是
_______。
(6)实验过程中,装置D中固体变为蓝色,说明草酸亚铁晶体分解生成了
_______,FeC
2O
4·xH
2O中x的值为
_______;实验结束后若不继续通氮气,x值
_______(填“偏大”、“不变”或“偏小”)。
(7)装置C中石灰水变浑浊,说明草酸亚铁晶体分解生成了
_______。
(8)装置E出现黑色物质,说明草酸亚铁晶体分解生成了
_______;同时装置E还具有的作用是
_______;
(9)根据上表数据,计算反应后装置B中残留黑色物质的化学式
_______。
【定量研究】
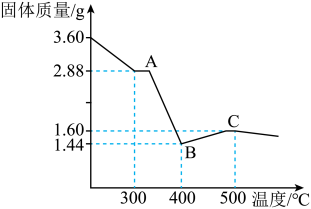
(10)取3.60g草酸亚铁晶体在坩埚中敞口充分加热,固体质量随温度变化的曲线如下图所示,写出BC段发生反应的化学方程式:
_______。