18. 硫酸亚铁是一种重要的食品和饲料添加剂,某补血剂样品【主要成分为硫酸亚铁晶体(FeSO
4•
xH
2O)】,某化学兴趣小组对其产生了兴趣并进行了探究:
【探究一】硫酸亚铁晶体(FeSO
4•
xH
2O)热分解研究
【查阅资料】
1.无水硫酸铜粉末遇水会变成蓝色的硫酸铜晶体;
2.硫酸亚铁晶体加热时,先失去结晶水,高温会继续分解产生金属氧化物和气态非金属氧化物。
3.二氧化硫能使高锰酸钾溶液褪色。
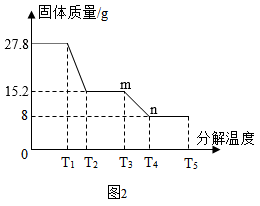
【进行实验】该兴趣小组同学称取27.8g硫酸亚铁晶体样品按图1高温加热,使其完全分解,对所得产物进行分析,并利用SDTQ600热分析仪,对硫酸亚铁晶体热分解获得相关数据,绘制成图2所示的关系图,试回答:
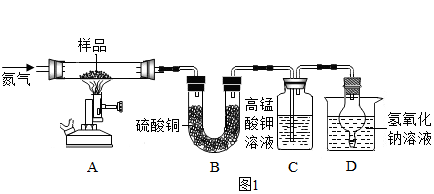
(1)装置B中硫酸铜粉末变蓝,说明产物中有
____ ,该物质的质量是
___ g;装置C中高锰酸钾溶液褪色,说明产物中还有
_____ ;硫酸亚铁晶体完全分解后,装置A中的固体呈红棕色,放入足量稀盐酸,固体全部溶解,且得到黄色溶液,则该红棕色固体与稀盐酸反应的化学方程式为
_____ 。
(2)D装置中球形干燥管的作用是
_____ 。
(3)硫酸亚铁分解生成铁的氧化物和硫的两种氧化物,请写出化学反应方程式
_____ 。
(4)根据图2中的数据,请求出FeSO
4•
xH
2O中的
x=
_____ 。(不写过程)
【交流讨论】实验中要持续通入氮气,否则测出的
x会
____ (填“偏大”、“偏小”或“不变”)。
【探究二】补血剂样品中硫酸亚铁的含量:
①取10g补血剂样品研细后溶于40g水中,研细的目的是
_____ ;
②向所配制的溶液中加氯化钡溶液至略过量,使其充分反应;
③过滤,洗涤,干燥,称量所得白色固体的质量为6.99g。
请计算出10g样品中FeSO
4的质量分数
_____ ,写出计算过程
(已知:FeSO
4+BaCl
2=BaSO
4↓+FeCl
2,有关相对分子质量:FeSO
4—152,BaSO
4—233)