北京市2017年中考化学试卷
北京
九年级
中考真题
2017-08-01
1834次
整体难度:
容易
考查范围:
化学与社会发展、物质构成的奥秘、身边的化学物质、物质的化学变化、化学实验
一、选择题 添加题型下试题
| A.分子 | B.原子 | C.离子 | D.元素 |
【知识点】 元素
| A.红磷 | B.木炭 | C.铁丝 | D.石蜡 |
| A.铁 | B.钙 | C.碘 | D.锌 |
【知识点】 人体内的微量元素——碘、铁元素解读 某些元素的缺乏症解读
| A.一氧化碳 | B.黄曲霉素 | C.甲醛 | D.水 |
【知识点】 一氧化碳的毒性及安全使用解读 对人体健康危害的物质解读
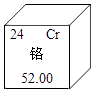
| A.原子序数是24 | B.属于非金属元素 |
| C.一个铬原子核外有28个电子 | D.相对原子质量为52.00g |
【知识点】 元素周期表及元素分类解读 元素周期表信息示意图解读
| A.氧气 | B.糖水 | C.食醋 | D.大理石 |
【知识点】 纯净物和混合物的判断解读
| A.闻气味 | B.观察颜色 |
| C.加水振荡 | D.将燃着的木条伸入集气瓶中 |
| A.2H | B.2H2 | C.H2 | D.2H2O2 |
【知识点】 化学式、分子式及涵义解读 化学符号周围数字的含义解读
| 植物 | 花生 | 苹果 | 西瓜 | 沙枣 |
| 适宜的pH范围 | 5.0~6.0 | 5.0~6.5 | 6.0~7.0 | 8.0~8.7 |
| A.花生 | B.苹果 | C.西瓜 | D.沙枣 |
【知识点】 溶液酸碱性及pH相关关系解读
12. 硅是信息技术的关键材料。高温下氢气与四氯化硅(SiCl4)反应的化学方程式为:2H2+SiCl4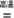 Si+4HCl,该反应属于
Si+4HCl,该反应属于
| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 |
| A.氧气可用作燃料 | B.二氧化碳可用作气体肥料 |
| C.干冰可用于人工降雨 | D.铜丝可用作导线 |
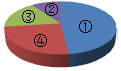
| A.① | B.② | C.③ | D.④ |
【知识点】 根据化学式计算元素质量分数解读
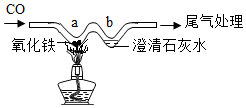
| A.a处红棕色粉末变为黑色 |
| B.a处的反应为CO +Fe2O3=2Fe+CO2 |
| C.b处澄清石灰水变浑浊证明有CO2生成 |
| D.可利用点燃的方法进行尾气处理 |
【知识点】 一氧化碳还原氧化铁实验解读
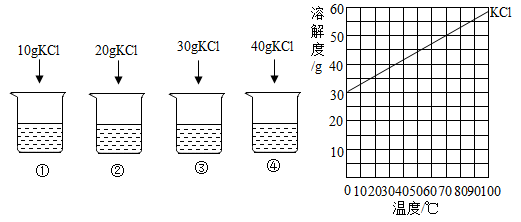
| A.10g | B.90g | C.100g | D.110g |
| A.②③④ | B.②④ | C.③④ | D.④ |
| A.升高温度 | B.加水 | C.加KCl固体 | D.倒出部分溶液 |
| A.26% | B.29% | C.35% | D.40% |

| A.反应过程中有热量放出 | B.30 s时,溶液中溶质为HCl和NaCl |
| C.该实验是将稀盐酸滴入稀NaOH溶液 | D.从20 s到40 s,溶液的温度升高,pH增大 |
二、填空与简答 添加题型下试题
(1)为使葡萄果实饱满、提高含糖量,在葡萄生长的中后期可适当施加硫酸钾、过磷酸钙等肥料,其中硫酸钾属于化学肥料中的
(2)用硫酸铜配制的农药波尔多液,可以防治葡萄生长中的病害。溶解硫酸铜时不宜用铁制容器,用化学方程式表示其原因:
(3)食用葡萄前要清洗干净,下图是一种清洗的方法。
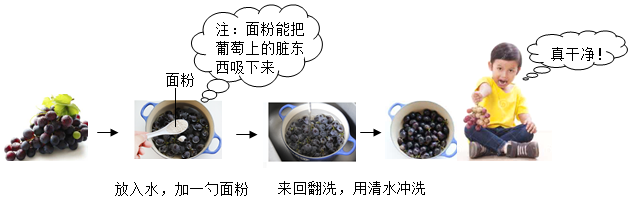
下列说法正确的是
A. 面粉有利于去除葡萄皮上的脏东西 B. 清洗干净后,建议吃葡萄不吐葡萄皮
C. 葡萄富含糖类物质,糖尿病人不宜多食
【知识点】 金属与盐溶液反应 常见化肥的种类及性质解读 糖类的组成与作用解读
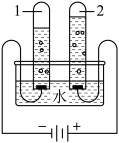
(1)试管2中生成的气体为
(2)该反应的化学方程式为
【知识点】 电解水实验的现象和结论解读 电解水生成物的验证解读
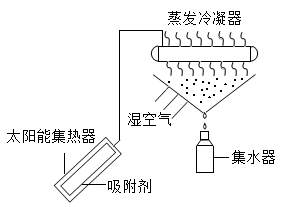
(1)蒸发冷凝器中发生的是
(2)吸附剂中主要物质为SiO和CaCl,SiO中硅元素的化合价为
(1)生活中,可以利用天然气(主要成分是甲烷)获得热量。甲烷燃烧的化学方程式为
(2)工业上,可以利用甲烷获得氢气,其反应的微观示意图如下:

①图1所示反应的化学方程式为
②在图2横线处补全相应微粒的图示
资料:在同温同压下,气体的体积之比等于分子个数之比。
(1)用微观示意图表示工作舱中空气的主要成分,下图中最合理的是
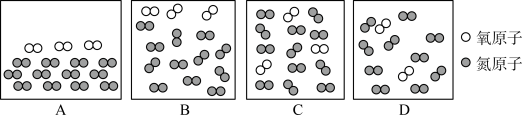
(2)宇航员呼出的CO2用氢氧化锂(LiOH)吸收,生成Li2CO3和H2O,反应的化学方程式为
(3)航天器返回地面后,用Ca(OH)2与Li2CO3发生复分解反应,使
说起二氧化硫(SO2),你可能首先想到它是空气质量播报中提及的大气污染物。其实你真的了解SO2吗?难道它只是有害物质吗?
SO2与食品工业
SO2作为防腐剂、漂白剂和抗氧化剂广泛用于食品行业。葡萄酒酿制中适量添加SO2,可防止葡萄酒在陈酿和贮藏过程中被氧化,抑制葡萄汁中微生物的活动。食糖加工过程中可使用SO2进行脱色。按照我国《食品添加剂使用标准(GB2760-2014)》,合理使用SO2不会对人体健康造成危害。
标准中部分食品SO2的最大残留量
| 食品 | 蜜饯 | 葡萄酒 | 食糖 | 水果干 | 巧克力 | 果蔬汁 |
| 最大残留量 | 0.35g/kg | 0.25g/L | 0.1g/kg | 0.1g/kg | 0.1g/kg | 0.05g/kg |
SO2与硫酸工业
硫酸是重要的化工原料,工业制硫酸的关键步骤是SO2的获取和转化。工业利用硫制硫酸的主要过程示意如下:
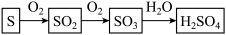
SO2与化石燃料
化石燃料中的煤通常含有硫元素,直接燃烧会产生SO2。为了减少煤燃烧产生的SO2污染空气,可以采取“提高燃煤质量,改进燃烧技术”的措施,例如,对燃煤进行脱硫、固硫处理;还可以采取“优化能源结构、减少燃煤使用”的措施,例如,北京大力推广的“煤改气、煤改电”工程,有效改善了空气质量。
现在,你对SO2一定有了新的认识,在今后的化学学习中你对SO2还会有更全面的认识!
依据文章内容回答下列问题。
(1)按照国家标准,食糖中的SO2最大残留量为
(2)葡萄酒酿制过程中SO2的作用是
(3)用硫制硫酸的主要过程中,涉及到的含硫物质有S、
(4)硫酸工业生产中,吸收尾气中SO2的物质是
(5)下列措施能减少SO2排放的是
A.将煤块粉碎 B.对燃煤进行脱硫
C.推广煤改气、煤改电 D.循环利用工业尾气中的SO2
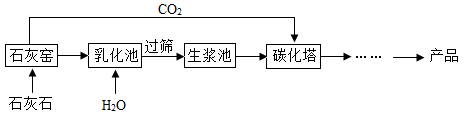
(2)乳化池中,生石灰与水发生反应,其化学方程式为
(3)过筛的目的是拦截
(4)碳化塔中反应的化学方程式为
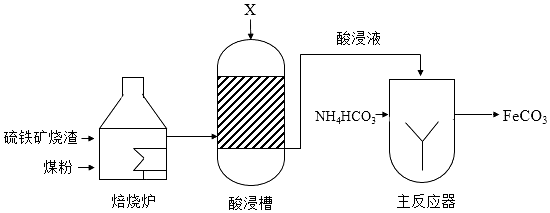
(1)焙烧炉中,发生的主要反应为:
①
 ②
② ③
③
上述反应中的各物质,碳元素呈现
(2)酸浸槽中,FeO转化为FeSO4,加入的物质X是
(3)主反应器中,生成FeCO3的反应物为

(1)认识阶梯甲
①阶梯上的5种物质中,属于氧化物的是
②攀登过程中,H2SO4与Na2CO3发生反应的化学方程式为
(2)搭建阶梯乙
请你从O2、Fe、Fe2O3、HCl、NaOH中选择4种物质,写在图中相应的台阶上,能领取奖杯。
(3)共享物质、重塑阶梯
阶梯乙搭建完成后,若在阶梯甲和阶梯乙中各选择一种物质进 行互换,也均能领取奖杯,则这两种物质是(任写一组即可)。
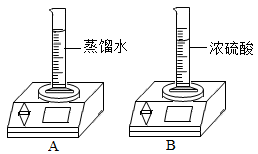
(1)A中示数变小,从微粒的角度解释其原因是
(2)B中示数
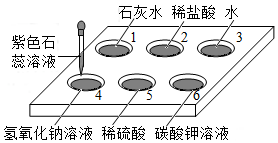
(1)孔穴6中溶液变为蓝色,说明碳酸钾溶液显
(2)溶液变为红色的孔穴有
(3)作为空白对照实验的孔穴是
(4)再向孔穴4中滴加稀硫酸,溶液变为紫色,用化学方程式解释其原因:

(1)打开K1,观察到蜡烛
(2)关闭K1、打开K2,观察到蜡烛缓慢的熄灭。蜡烛熄灭的原因是
| A用浓硫酸配制100g 9.8%的稀硫酸 | B粗盐中难溶性杂质的去除 |
| (1)实验需要5.4mL浓硫酸和90mL水。量取两种液体用到的仪器有________(填序号)。 (2)稀释时,需将浓硫酸缓慢倒入水中,并不断进行搅拌,其原因是________。 | (1)过滤需要用到的仪器有________(填序号)。 (2)蒸发过程中,需不断进行搅拌,其原因是________。 |
| 可供选择的主要仪器: ①试管 ②烧杯 ③蒸发皿 ④托盘天平 ⑤10mL量筒 ⑥100mL量筒 ⑦药匙 ⑧胶头滴管 ⑨漏斗 ⑩酒精灯 ⑪铁架台 ⑫玻璃棒 | |
【知识点】 浓溶液稀释配制一定质量分数溶液解读 粗盐提纯解读
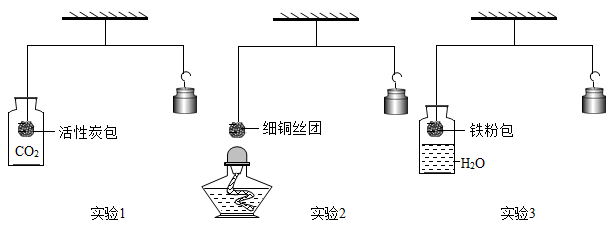
(1)实验1:通入CO2一段时间后,活性炭包下沉,原因是
(2)实验2:加热细铜丝团一段时间后移走酒精灯,观察到铜丝变为黑色(CuO),细铜丝团
(3)实验3:一段时间后,铁粉包下沉,是因为铁粉与
三、实验题 添加题型下试题
| 实验装置 | 【实验1】制备气体 | 【实验2】测定空气中氧气含量 |
 | 左管中带孔的燃烧匙盛有足量锌粒,右管盛有稀硫酸 Ⅰ.打开K1和K2,使反应发生 Ⅱ.在K1的导管口处收集气体 Ⅲ.…… | 左管中燃烧匙盛有足量白磷,右管盛有水 Ⅰ.光照引燃白磷 Ⅱ.待白磷熄灭,冷却,打开K2,至液面不再变化,右管中液体的高度为h1 |
为使反应停止,Ⅲ中的操作是
(2)实验2:打开K2,右管中液面下降,原因是
计算空气中氧气体积分数的表达式为
四、科学探究题 添加题型下试题
Ⅰ.不稳定性
(1)如下图所示进行实验,受热分解的化学方程式为,3.16g KMnO4产生O2的质量为
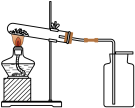
(2)用向上排空气法收集O2的原因是
Ⅱ.腐蚀性
【查阅资料】KMnO4 溶液呈中性、有腐蚀性
【进行实验】
实验1:将新鲜鸡皮在不同浓度的KMnO4溶液中浸泡相同时间,现象如下表
| KMnO4 溶液浓度 | 0.002% | 0.01% | 0.1% | 1% |
| 鸡皮的变化 | 无明显变化 | 边缘部分变为棕黄色 | 全部变为棕色 | 全部变为黑色 |
实验2:将铜片分别浸泡在4种浸泡相同时间,现象如下表。
| 编号 | ① | ② | ③ | ④ | |
| 实验 | 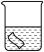 25mL0.1%KMnO4溶液 | 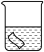 25mL0.1%KMnO4溶液+10滴浓硫酸 | 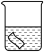 25mL蒸馏水+10滴浓硫酸 | 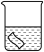 25mL1%KMnO4溶液+10滴浓硫酸 | |
| 铜片质量/g | 实验前 | 0.54 | 0.54 | 0.54 | 0.54 |
| 18小时后 | 0.54 | 0.52 | 0.54 | 0.43 | |
【解释与结论】
(3)实验1的目的是
(4)实验2中通过对比②和④,得出的结论是
(5)实验2中,欲得出“KMnO4和硫酸共同作用对铜才有腐蚀性”的结论,需要对比
(6)实验2中,铜片被腐蚀的反应如下,补全该反应的化学方程式。
5Cu+2KMnO4+8H2SO4=5CuSO4+2MnSO4+K2SO4+
试卷分析
导出试卷题型(共 35题)
试卷难度
知识点分析
细目表分析
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.85 | 绿色化学 | 单选题 |
| 2 | 0.85 | 元素 | 单选题 |
| 3 | 0.85 | 氧气助燃性及实验 铁在氧气中燃烧及其实验 木炭在氧气中燃烧及其实验 氧气与石蜡的反应 | 单选题 |
| 4 | 0.85 | 人体内的微量元素——碘、铁元素 某些元素的缺乏症 | 单选题 |
| 5 | 0.85 | 化学性质和物理性质 | 单选题 |
| 6 | 0.94 | 一氧化碳的毒性及安全使用 对人体健康危害的物质 | 单选题 |
| 7 | 0.85 | 元素周期表及元素分类 元素周期表信息示意图 | 单选题 |
| 8 | 0.85 | 纯净物和混合物的判断 | 单选题 |
| 9 | 0.94 | 氧气的物理性质及贮存 氧气助燃性及实验 二氧化碳与水的反应及实验 | 单选题 |
| 10 | 0.85 | 化学式、分子式及涵义 化学符号周围数字的含义 | 单选题 |
| 11 | 0.85 | 溶液酸碱性及pH相关关系 | 单选题 |
| 12 | 0.85 | 化合反应 分解反应 置换反应 复分解反应的定义 | 单选题 |
| 13 | 0.65 | 氧气助燃性及实验 二氧化碳的用途 金属的物理通性与用途 | 单选题 |
| 14 | 0.65 | 根据化学式计算元素质量分数 | 单选题 |
| 15 | 0.65 | 一氧化碳还原氧化铁实验 | 单选题 |
| 16-19 | 0.65 | m溶质+m溶剂=m溶液的应用 饱和溶液和不饱和溶液判断 饱和溶液和不饱和溶液的转换 溶质质量分数公式运用 | 选择题组 |
| 20 | 0.65 | 溶液酸碱性及pH相关关系 化学反应中能量变化的实际应用 | 单选题 |
| 二、填空与简答 | |||
| 21 | 0.85 | 常见盐的俗名、用途 与爆炸和燃烧有关图标的辨认 爱护水资源 | 简答题 |
| 22 | 0.94 | 常见盐的俗名、用途 油脂的来源 | 填空题 |
| 23 | 0.65 | 金属与盐溶液反应 常见化肥的种类及性质 糖类的组成与作用 | 填空题 |
| 24 | 0.65 | 电解水实验的现象和结论 电解水生成物的验证 | 填空题 |
| 25 | 0.65 | 化学变化与物理变化判断 根据化学式计算元素质量比 化合价代数和的计算与应用 | 填空题 |
| 26 | 0.65 | 化学方程式的书写 甲烷的燃烧 | 填空题 |
| 27 | 0.65 | 微粒图像的分析及应用 空气各成分及其体积分数 二氧化碳与碱的反应及实验 | 填空题 |
| 28 | 0.65 | 空气的污染与防治 常见几种燃料使用对环境的影响 空气污染及其保护 | 科普阅读题 |
| 29 | 0.65 | 化学方程式的书写 生石灰的性质及用途 碱的通性 盐类参与的反应 | 流程题 |
| 30 | 0.65 | 用质量守恒定律确定物质组成 化合价代数和的计算与应用 工业炼铁的原理及装置 盐类参与的反应 | 流程题 |
| 31 | 0.65 | 金属与氧气反应 酸的通性 碱的通性 碳酸氢钠、碳酸钠、碳酸钙 | 填空题 |
| 32 | 0.85 | 微粒的共性 微粒的观点解释现象 浓酸敞口放置的变化和现象 | 填空题 |
| 33 | 0.65 | 常见的酸碱指示剂及其变色情况 无明显现象的中和反应的判断 | 填空题 |
| 34 | 0.65 | 过氧化氢制取氧气实验 制取二氧化碳的原理 二氧化碳不可燃、不支持燃烧性质 | 填空题 |
| 35 | 0.85 | 浓溶液稀释配制一定质量分数溶液 粗盐提纯 | 填空题 |
| 36 | 0.65 | 活性炭的吸附性 金属与氧气反应 钢铁的锈蚀 | 填空题 |
| 三、实验题 | |||
| 37 | 0.65 | 化学方程式的书写 测定空气中氧气的含量实验的过程 金属与酸反应原理 | |
| 四、科学探究题 | |||
| 38 | 0.65 | 用质量守恒定律确定物质组成 不含杂质的化学方程式计算 高锰酸钾制取氧气实验 气体的收集方式 | |






