25. 过氧化氢在生产生活中有着广泛的应用。化学实验小组对过氧化氢的某些性质进行了研究。
Ⅰ、不稳定性
(1)如图所示进行实验(还测量收集的氧气体积),过氧化氢分解的化学方程式为
______,导管伸入量筒收集气体在滴加双氧水
______(前或后)。
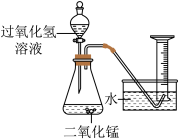
(2)能用排水法收集氧气的原因是
______。
(3)已知:常温常压下,氧气的密度为1.33g·L
-1。实验小组称量了10g溶质质量分数为6%的过氧化氢溶液进行实验,如果将该过氧化氢溶液一次性全部放入锥形瓶中,则选择规格为
______mL(选填“50”、“200”或“250”)的量筒收集氧气较为合适,图示方法测得氧气体积偏大的原因是
______。
(4)实验小组同学还探究了温度对过氧化氢分解速率的影响,相关实验数据如下表:
| 实验序号 | ① | ② | ③ |
| H2O2溶液的溶质质量分数/% | 30 | 30 | 30 |
| H2O2溶液的体积/mL | 6 | 6 | 6 |
| 温度/℃ | 20 | 35 | 35 |
| MnO2的用量/g | 0 | 0 | 0 |
| 反应时间/min | 40 | 40 | 40 |
| 收集O2的体积/mL | 0 | 1.9 | 7.8 |
由此得出的结论是
______。
Ⅱ、腐蚀性
【查阅资料】H
2O
2溶液有一定的腐蚀性。
【进行实验】将铜片分别浸泡在以下3重溶液中进行实验,实验现象如下表:
| 编号 | ① | ② | ③ |
| 实验 | 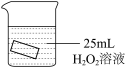 | 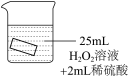 | 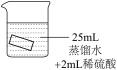 |
| 一段时间后的现象 | 无明显变化 | 溶液变蓝,缓慢产生细小气泡 | 无明显变化 |
【解释与结论】
(5)实验⑤中铜片被腐蚀的反应为Cu+H
2O+H
2SO
4=CuSO
4+
______,请补全该反应的化学方程式。
【反思交流】
(6)小红同学提出,实验⑤中除发生(5)所给的反应外,还发生了另一个反应导致有细小的气泡产生,该反应的反应物是
______。