超氧化钠(NaO2)是一种固体供氧剂,可应用于家庭急救。超氧化钠在常温下分别能与CO2、H2O、HCl发生反应,均可生成O2。为了验证CO2能跟NaO2反应生成O2,某化学小组的同学设计了下图所示实验。(已知:超氧化钠能与水反应生成氢氧化钠和氧气。)
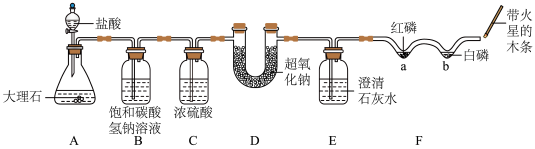
(1)超氧化钠能和二氧化碳反应,生成氧气和一种白色固体,则该白色固体可能是________ 。
a、NaCl b、NaOH c、Na2CO3 d 、NaHCO3
(2)A装置中所发生反应的化学方程式为_______ 。
(3)用化学反应方程式表示B装置中饱和NaHCO3溶液的作用________ ;表明二氧化碳没有被超氧化钠完全吸收的现象是______ ;请将C装置中导管补画完整。________
(4)F是利用W管进行微型实验的装置。实验过程中微热a、b处,观察到a处红磷不燃烧,b处白磷燃烧,由此可得出燃烧的条件之一是什么?________
(5)实验结束后,某同学取少量D中固体于试管中,加足量水,有气泡产生。为验证该水溶液中含有的氢氧化钠,他再向试管中滴加酚酞溶液,观察到溶液变红,于是该同学得出“溶液中一定含有氢氧化钠”的结论。请简述该同学的验证实验设计不合理的原因。________
(6)若要用超氧化钠与水反应来制取72g氧气,请计算理论上需要超氧化钠的质量。________

(1)超氧化钠能和二氧化碳反应,生成氧气和一种白色固体,则该白色固体可能是
a、NaCl b、NaOH c、Na2CO3 d 、NaHCO3
(2)A装置中所发生反应的化学方程式为
(3)用化学反应方程式表示B装置中饱和NaHCO3溶液的作用
(4)F是利用W管进行微型实验的装置。实验过程中微热a、b处,观察到a处红磷不燃烧,b处白磷燃烧,由此可得出燃烧的条件之一是什么?
(5)实验结束后,某同学取少量D中固体于试管中,加足量水,有气泡产生。为验证该水溶液中含有的氢氧化钠,他再向试管中滴加酚酞溶液,观察到溶液变红,于是该同学得出“溶液中一定含有氢氧化钠”的结论。请简述该同学的验证实验设计不合理的原因。
(6)若要用超氧化钠与水反应来制取72g氧气,请计算理论上需要超氧化钠的质量。
更新时间:2021-05-06 22:11:54
|
相似题推荐
实验题
|
适中
(0.65)
解题方法
【推荐1】以下是实验室制取气体的常用仪器,回答列问题。
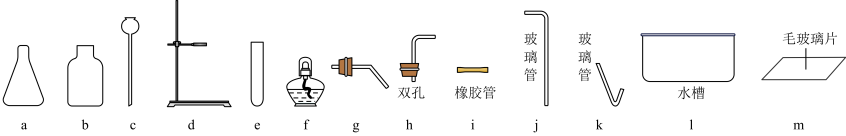
(1)从标号为a、b、e的仪器中任意选择一种,写出它的名称是________ ,简要说出它的一种用途______ ;
(2)用2KMnO4 K2MnO4 + MnO2 + O2↑制取O2,并用向上排空气法收集。
K2MnO4 + MnO2 + O2↑制取O2,并用向上排空气法收集。
①若制取1.6g O2,理论上至少需要KMnO4________ g;
②收集O2时,图中有2个玻璃管:玻璃管1和玻璃管2,你选择_______ ;
(3)用大理石和稀盐酸反应制取CO2,并用排空气法收集;
①该反应的化学方程式为________ ;
②组装制取装置时,需选择上图中的a、b、h、j、m和_______ 、_______ 。
③收集一瓶二氧化碳气体:当收集一段时间后,将燃着的木条放在集气瓶口,若观察到火焰熄灭,则接下来应进行的操作是_________ 。

(1)从标号为a、b、e的仪器中任意选择一种,写出它的名称是
(2)用2KMnO4
 K2MnO4 + MnO2 + O2↑制取O2,并用向上排空气法收集。
K2MnO4 + MnO2 + O2↑制取O2,并用向上排空气法收集。①若制取1.6g O2,理论上至少需要KMnO4
②收集O2时,图中有2个玻璃管:玻璃管1和玻璃管2,你选择
(3)用大理石和稀盐酸反应制取CO2,并用排空气法收集;
①该反应的化学方程式为
②组装制取装置时,需选择上图中的a、b、h、j、m和
③收集一瓶二氧化碳气体:当收集一段时间后,将燃着的木条放在集气瓶口,若观察到火焰熄灭,则接下来应进行的操作是
您最近半年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】某校化学兴趣小组学习了气体的制取和收集后,对相关知识进行总结,请你一起参与,并完成下面题目内容:

(1)写出下列仪器名称:a_____ ,b_____ .
(2)装置B可用于制取氢气,实验室制取氢气的化学方程式为_____ .
(3)若用D装置收集二氧化碳,则二氧化碳应从_____ 口通入(填”c”或“d”).
(4)若用装置E测量生成CO2气体的体积是不准确的,原因是_____ ,要用装置E准确测量生成CO2气体的体积的措施有_____ .
(5)利用如图装置,分别用氯酸钾或过氧化氢制取氧气,都需要加入少量二氧化锰,二氧化锰的作用是_____ ;若未加入二氧化锰,则反应_____ (选填“不能发生”或“明显减慢”),若实验室要制取48g氧气,至少需要氯酸钾__________ 克?(计算题)

(1)写出下列仪器名称:a
(2)装置B可用于制取氢气,实验室制取氢气的化学方程式为
(3)若用D装置收集二氧化碳,则二氧化碳应从
(4)若用装置E测量生成CO2气体的体积是不准确的,原因是
(5)利用如图装置,分别用氯酸钾或过氧化氢制取氧气,都需要加入少量二氧化锰,二氧化锰的作用是
您最近半年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】金属材料的使用与生产、生活和社会发展密切相关。请回答下列问题:
I. 金属的应用
(1)共享单车颇受年轻人的喜爱。车上的钢丝网篓属于________ (填“纯净物”或“混合物”)。
(2)2023年5月28日国产C919大飞机完成了商业首航。C919飞机制造过程中使用了锂铝合金,说明其具有________ (填字母)优点。
Ⅱ.炼铁过程的探究。
实验室利用如图装置可制得铁。
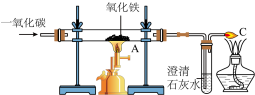
(3)A处玻璃管内所发生反应的化学方程式是_________________________ 。
(4)装置B中的实验现象是_____ 。
(5)C处酒精灯的作用是__________ 。
Ⅲ.金属的活动性顺序判断
(6)将一定量的硫酸铜溶液加入锌和铁的混合物中,反应的示意图如下图。
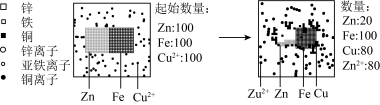
由上可知,实验中发生反应的化学方程式为________ 可得结论:_________ 。
(7)在(6)中反应结束后的混合物中继续滴加硫酸铜溶液,当微粒种类和数量呈现__ 的变化情况时,可得结论:金属活动性Zn>Fe>Cu。
Ⅳ. 定量计算
(8)某化工厂产生的废液中含有硫酸亚铁和硫酸铜(不考虑其它物质),为回收铜和硫酸亚铁,研究人员设计出“用铁处理”的方案。取200g上述废液,向其中加入5.6g铁粉,恰好完全反应,测得反应后溶液中溶质的质量分数为15%,试计算可回收得到硫酸亚铁的质量是__ g(写出计算过程,结果保留小数点后一位)。
I. 金属的应用
(1)共享单车颇受年轻人的喜爱。车上的钢丝网篓属于
(2)2023年5月28日国产C919大飞机完成了商业首航。C919飞机制造过程中使用了锂铝合金,说明其具有
| A.硬度大 | B.密度小 | C.易导电 | D.耐腐蚀 |
Ⅱ.炼铁过程的探究。
实验室利用如图装置可制得铁。

(3)A处玻璃管内所发生反应的化学方程式是
(4)装置B中的实验现象是
(5)C处酒精灯的作用是
Ⅲ.金属的活动性顺序判断
(6)将一定量的硫酸铜溶液加入锌和铁的混合物中,反应的示意图如下图。

由上可知,实验中发生反应的化学方程式为
(7)在(6)中反应结束后的混合物中继续滴加硫酸铜溶液,当微粒种类和数量呈现
Ⅳ. 定量计算
(8)某化工厂产生的废液中含有硫酸亚铁和硫酸铜(不考虑其它物质),为回收铜和硫酸亚铁,研究人员设计出“用铁处理”的方案。取200g上述废液,向其中加入5.6g铁粉,恰好完全反应,测得反应后溶液中溶质的质量分数为15%,试计算可回收得到硫酸亚铁的质量是
您最近半年使用:0次
实验题
|
适中
(0.65)
【推荐1】实验室制取气体时需要的一些装置如图所示,请回答下列问题。

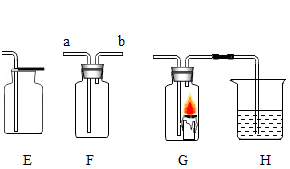
(1)写出标有序号的仪器名称:①_____ ,② _____ 。
(2)实验室制取氧气和二氧化碳的发生装置都可选用 B 装置的原因是_____ ,装置中使用分液漏斗的优点是 _____ 。
(3)若要得到干燥的氧气,最好用_____ 法收集。
(4)用F装置收集二氧化碳,气体从_____ 端通入(填字母)。
(5)某兴趣小组的同学连接 B、G、H 装置进行实验。若实验时 G 装置中蜡烛燃烧更剧烈,H 装置中溶液变浑浊,则 B 装置中反应的化学方程式为_____ 。


(1)写出标有序号的仪器名称:①
(2)实验室制取氧气和二氧化碳的发生装置都可选用 B 装置的原因是
(3)若要得到干燥的氧气,最好用
(4)用F装置收集二氧化碳,气体从
(5)某兴趣小组的同学连接 B、G、H 装置进行实验。若实验时 G 装置中蜡烛燃烧更剧烈,H 装置中溶液变浑浊,则 B 装置中反应的化学方程式为
您最近半年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】根据下列实验装置图回答问题:

(1)写出图中仪器a的名称:__________ 。
(2)若实验室用加热KMnO4制取氧气,选择的装置组合是______ (填字母序号),写出该反应的化学方程式_______ 。若用E装置来收集氧气,集满气体的集气瓶移出水面后应_____ (填“正放”或“倒放”)在桌面上。
(3)通常将产生的二氧化碳通入装置F,目的是__________ 。
(4)若用G装置来去除CO中混有的少量CO2,则该装置中最好加入下列哪种试剂_______ (填字母序号),混合气体应从_________ (填“M”或“N”)端导管口进入。
A 浓硫酸 B 紫色石蕊溶液 C 氢氧化钠溶液

(1)写出图中仪器a的名称:
(2)若实验室用加热KMnO4制取氧气,选择的装置组合是
(3)通常将产生的二氧化碳通入装置F,目的是
(4)若用G装置来去除CO中混有的少量CO2,则该装置中最好加入下列哪种试剂
A 浓硫酸 B 紫色石蕊溶液 C 氢氧化钠溶液
您最近半年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】实验室制取某些气体的装置如下:
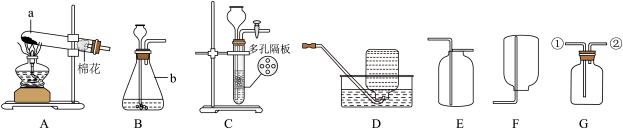
(1)仪器b的名称为______ 。
(2)实验时要根据酒精灯_______ (填“内焰”或“外焰”)调整试管的高度,并固定在铁架台上。
(3)写出实验室用A装置制氧气的文字表达式______ ,试管口放棉花的目的是_______ 。
(4)若收集的氧气用来做蜡烛燃烧实验,并验证蜡烛燃烧的产物,最好选择_______ 装置收集(从A—F中选取)。
(5)实验室制取二氧化碳的文字表达式_______ 。选用发生装置时,选用C装置相对B装置的优点是_______ 。
(6)用G装置收集二氧化碳时,证明集满的方法是______ (方法、现象,结论)。

(1)仪器b的名称为
(2)实验时要根据酒精灯
(3)写出实验室用A装置制氧气的文字表达式
(4)若收集的氧气用来做蜡烛燃烧实验,并验证蜡烛燃烧的产物,最好选择
(5)实验室制取二氧化碳的文字表达式
(6)用G装置收集二氧化碳时,证明集满的方法是
您最近半年使用:0次
实验题
|
适中
(0.65)
【推荐1】已知白磷化学式为P4,结构如图1所示,着火点是40℃;红磷以P4四面体的单键形成链或环的高聚合结构,结构如图2所示,着火点是240℃。如图3实验,三支试管里面充满氮气,初始温度25℃,升温至60℃后,用注射器同时向②③试管中迅速注入足量氧气。请回答下列问题。
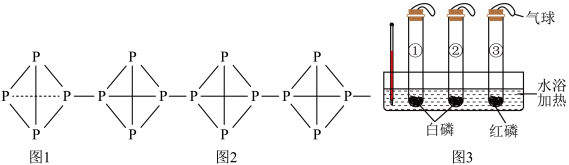
(1)白磷、红磷物理性质存在明显差异的原因是__________ 。
(2)观察到试管__________ (填试管编号)中物质燃烧,反应的化学方程式为__________ 。
(3)根据图3实验得出燃烧需要的条件是 (填序号)。

(1)白磷、红磷物理性质存在明显差异的原因是
(2)观察到试管
(3)根据图3实验得出燃烧需要的条件是 (填序号)。
| A.可燃物 | B.温度达到着火点 | C.需要氧气参与 |
您最近半年使用:0次
实验题
|
适中
(0.65)
名校
【推荐2】在化学学习中,很多结论都是通过对比实验获得的,如下图所示

(1)利用对比实验可探究燃烧条件,如图 1 所示。请根据实验回答下列问题。
①铜片在实验中起到的作用是_____ ,请写出图 1 所示实验中的实验现象_____ 。
②小冬在进行图 1 所示实验时,对乒乓球的材质产生了极大兴趣,于是他查阅了资料,发现该实验所用的乒乓球是有“赛璐珞”——硝化纤维塑料制成,该赛璐珞属于_____ 材料。
(2)根据图 2 所示实验回答下列问题:试管C 中放入氯化钙的作用_____ , 对比A 和B 实验得到的结论是_____ ;金属资源是 不可再生的,防止金属锈蚀是保护金属资源的方法之一,请你再写出一种保护金属资源的方法_____ 。
(3)请你设计实验证明Fe 和Cu 的金属活动性顺序,并完成实验报告。

(1)利用对比实验可探究燃烧条件,如图 1 所示。请根据实验回答下列问题。
①铜片在实验中起到的作用是
②小冬在进行图 1 所示实验时,对乒乓球的材质产生了极大兴趣,于是他查阅了资料,发现该实验所用的乒乓球是有“赛璐珞”——硝化纤维塑料制成,该赛璐珞属于
(2)根据图 2 所示实验回答下列问题:试管C 中放入氯化钙的作用
(3)请你设计实验证明Fe 和Cu 的金属活动性顺序,并完成实验报告。
| 实验步骤 | 实验现象 | 实验结论 |
您最近半年使用:0次
实验题
|
适中
(0.65)
【推荐1】下图是实验室常用气体制备装置,据图回答问题:
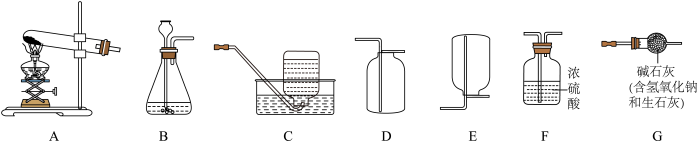
(1)用A装置制取氧气的化学方程式是_____ 。选择D装置收集氧气是因为_____ 。实验室制取二氧化碳的化学方程式是_____ ,选用的发生装置是_____ 。
(2)实验室制取氨气的反应原理是Ca(OH)2(固)+2NH4Cl(固) CaCl2(固)+2H2O+2NH3↑。要制取并收集干燥的氨气,所选装置正确的连接顺序是
CaCl2(固)+2H2O+2NH3↑。要制取并收集干燥的氨气,所选装置正确的连接顺序是_____ (填代号)。

(1)用A装置制取氧气的化学方程式是
(2)实验室制取氨气的反应原理是Ca(OH)2(固)+2NH4Cl(固)
 CaCl2(固)+2H2O+2NH3↑。要制取并收集干燥的氨气,所选装置正确的连接顺序是
CaCl2(固)+2H2O+2NH3↑。要制取并收集干燥的氨气,所选装置正确的连接顺序是
您最近半年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】根据下列实验装置图回答问题。
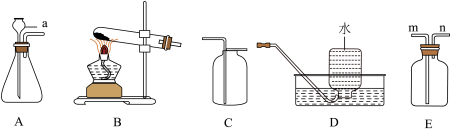
(1)仪器a的名称是______ 。
(2)实验室用过氧化氢溶液和二氧化锰制取氧气。
①应选择的发生装置为______ (填序号),反应的化学方程式为______ 。
②若用C装置收集氧气,检验氧气已经收集满的方法是______ 。
③如图是用D装置收集氧气,集满后移出集气瓶的操作,该错误操作会导致的后果为______ 。
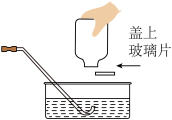
④70g过氧化氢溶液完全反应后生成1.6g氧气。则参加反应的过氧化氢质量为______ g。过氧化氢溶液中溶质质量分数为______ (精确至0.1%)。
(3)E装置可以进行许多实验。当气体从m口进入时,下列实验设计方案中可行的是______ (填序号)。
①E中盛澄清石灰水时,可以检验二氧化碳气体
②E中盛烧碱溶液时,可以除去CO中混有的CO2
③E中盛浓硫酸时,可以除去氧气中的水蒸气
④E中盛冷水和红磷(着火点240℃),可验证可燃物燃烧的条件

(1)仪器a的名称是
(2)实验室用过氧化氢溶液和二氧化锰制取氧气。
①应选择的发生装置为
②若用C装置收集氧气,检验氧气已经收集满的方法是
③如图是用D装置收集氧气,集满后移出集气瓶的操作,该错误操作会导致的后果为

④70g过氧化氢溶液完全反应后生成1.6g氧气。则参加反应的过氧化氢质量为
(3)E装置可以进行许多实验。当气体从m口进入时,下列实验设计方案中可行的是
①E中盛澄清石灰水时,可以检验二氧化碳气体
②E中盛烧碱溶液时,可以除去CO中混有的CO2
③E中盛浓硫酸时,可以除去氧气中的水蒸气
④E中盛冷水和红磷(着火点240℃),可验证可燃物燃烧的条件
您最近半年使用:0次
【推荐3】气体制备、收集是初中化学的重要知识,请你结合如图,回答有关问题。

(1)写出图中仪器b的名称:_______________ 。
(2)实验室用氯酸钾制取氧气应选择的发生装置是_____________ ( 填字母),写出氯酸钾制取氧气的化学方程式_____________________ 。
(3)实验室可用装置C代替装置B制取二氧化碳,装置C比B的优点是_____________ ;用E装置收集二氧化碳,则气体应从____________ (填“①”或“②”)端进入。
(4)若要用D装置干燥氢气,可将气体通入装有____________ (填试剂名称)的D装置中。

(1)写出图中仪器b的名称:
(2)实验室用氯酸钾制取氧气应选择的发生装置是
(3)实验室可用装置C代替装置B制取二氧化碳,装置C比B的优点是
(4)若要用D装置干燥氢气,可将气体通入装有
您最近半年使用:0次




