高氯酸钠可以用于制备火箭推进剂高氯酸铵。以粗盐为原料制备高氯酸钠晶体(NaClO4·H2O)的流程如下:
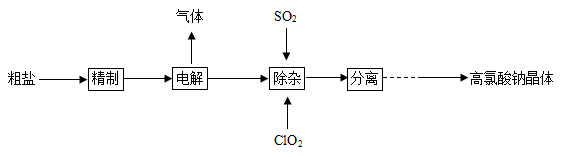
(1)“精制”中,由粗盐(含Ca2+、Mg2+、 等杂质)制备精制盐水时需用到NaOH、BaCl2、Na2CO3等试剂。加入Na2CO3溶液的作用
等杂质)制备精制盐水时需用到NaOH、BaCl2、Na2CO3等试剂。加入Na2CO3溶液的作用_______ 。“电解”分两步进行,其反应分别为NaCl+3H2O NaClO3+3H2↑、NaClO3+H2O
NaClO3+3H2↑、NaClO3+H2O NaClO4+H2↑。
NaClO4+H2↑。
(2)“除杂”的目的是除去少量未被电解的NaClO3,该反应的化学方程式为_______ 。
(3)“分离”的操作分别是加热浓缩、_______ 、过滤、洗涤、干燥。(各物质的溶解度如图所示)
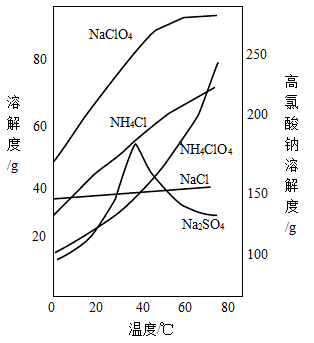
(4)为确定所得高氯酸钠晶体的纯度(含有少量Na2SO4杂质),进行如下实验:①准确称取3.00g样品加水充分溶解配制成100 mL溶液。②量取25.00mL溶液,加入足量的KI溶液充分反应(NaClO4+8KI+4H2O=4I2+8KOH+NaCl),再滴加Na2S2O3溶液进行反应(反应为I2+2Na2S2O3=2NaI+Na2S4O6),恰好消耗40.00 g15.8%Na2S2O3溶液。根据以上数据计算样品中高氯酸钠晶体纯度_____ (写出计算过程,保留2位小数)。

(1)“精制”中,由粗盐(含Ca2+、Mg2+、
 等杂质)制备精制盐水时需用到NaOH、BaCl2、Na2CO3等试剂。加入Na2CO3溶液的作用
等杂质)制备精制盐水时需用到NaOH、BaCl2、Na2CO3等试剂。加入Na2CO3溶液的作用 NaClO3+3H2↑、NaClO3+H2O
NaClO3+3H2↑、NaClO3+H2O NaClO4+H2↑。
NaClO4+H2↑。(2)“除杂”的目的是除去少量未被电解的NaClO3,该反应的化学方程式为
(3)“分离”的操作分别是加热浓缩、

(4)为确定所得高氯酸钠晶体的纯度(含有少量Na2SO4杂质),进行如下实验:①准确称取3.00g样品加水充分溶解配制成100 mL溶液。②量取25.00mL溶液,加入足量的KI溶液充分反应(NaClO4+8KI+4H2O=4I2+8KOH+NaCl),再滴加Na2S2O3溶液进行反应(反应为I2+2Na2S2O3=2NaI+Na2S4O6),恰好消耗40.00 g15.8%Na2S2O3溶液。根据以上数据计算样品中高氯酸钠晶体纯度
更新时间:2021-10-10 15:15:16
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】2022年2月4日,举世瞩目的第24届北京冬季奥林匹克运动会向全世界传递了绿色奥运的理念,回答下列问题。
(1)冬奥火炬“飞扬”采用氢气作燃料。氢气燃烧的化学方程式为_____ ;关闭燃气开关,使火炬熄灭,采用的灭火原理是_____ 。
(2)冬奥速滑场馆“冰丝带”采用CO2跨临界直冷制冰,碳排放值趋近于零,可减缓_____ 效应。
(3)冬奥村为了给运动员补充营养,准备了丰富多样的食物。一位运动员自助选择了米饭、水煮鱼片、红烧肉、麻婆豆腐,从均衡膳食角度看,你认为他还需要补充的营养物质是_____ 。
(4)滑雪大跳台主体为钢结构,生铁和钢的性能不同的主要原因是_____ 。裁判塔采用的是耐候钢,该钢材自带防腐功能。而铁制品易锈蚀是铁与空气中的_____ 共同作用的结果。
(5)冬奥会国家速滑馆“冰丝带”采用面向未来的单层双向正交马鞍形索网结构,减少屋顶所用钢材2800吨。某钢铁厂每天需消耗2500t含Fe2O376%的赤铁矿石,该厂理论上可日产含Fe98%的生铁的质量是_____ t(结果精确到0.1)。
(6)现有不纯的氧化铜样品16g,所含杂质可能是氧化铝、氧化镁、木炭粉、氯化钠。向其中加入200g溶质质量分数为9.8%的稀硫酸,恰好完全反应,没有固体剩余。反应生成水的质量是_____ g。
(1)冬奥火炬“飞扬”采用氢气作燃料。氢气燃烧的化学方程式为
(2)冬奥速滑场馆“冰丝带”采用CO2跨临界直冷制冰,碳排放值趋近于零,可减缓
(3)冬奥村为了给运动员补充营养,准备了丰富多样的食物。一位运动员自助选择了米饭、水煮鱼片、红烧肉、麻婆豆腐,从均衡膳食角度看,你认为他还需要补充的营养物质是
(4)滑雪大跳台主体为钢结构,生铁和钢的性能不同的主要原因是
(5)冬奥会国家速滑馆“冰丝带”采用面向未来的单层双向正交马鞍形索网结构,减少屋顶所用钢材2800吨。某钢铁厂每天需消耗2500t含Fe2O376%的赤铁矿石,该厂理论上可日产含Fe98%的生铁的质量是
(6)现有不纯的氧化铜样品16g,所含杂质可能是氧化铝、氧化镁、木炭粉、氯化钠。向其中加入200g溶质质量分数为9.8%的稀硫酸,恰好完全反应,没有固体剩余。反应生成水的质量是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
真题
解题方法
【推荐2】过氧化钙晶体(CaO2·8H2O)较稳定,呈白色,微溶于水,广泛应用于环境杀菌、消毒。以贝壳为原料制备CaO2流程如下:

(1)气体X是CO2,其名称是__________ ;将过氧化钙晶体与溶液分离的方法是_____ 。
(2)反应Y需控制温度在0~5℃,可将反应容器放在__________ 中,该反应是化合反应,反应产物是CaO2·8H2O,请写出化学方程式______________________ 。获得的过氧化钙晶体中常含有Ca(OH)2杂质,原因是_________________________ 。
(3)CaO2的相对分子质量为______ ,过氧化钙晶体(CaO2·8H2O)中H、O元素的质量比为________ 。
(4)为测定制得的过氧化钙晶体中CaO2·8H2O的质量分数,设计的实验如下:称取晶体样品50g,加热到220℃充分反应(方程式为 ,杂质不发生变化),测得生成氧气的质量为3.2g,请计算样品中CaO2·8H2O的质量分数
,杂质不发生变化),测得生成氧气的质量为3.2g,请计算样品中CaO2·8H2O的质量分数________ (CaO2·8H2O相对分子质量为216),写出必要的计算过程。

(1)气体X是CO2,其名称是
(2)反应Y需控制温度在0~5℃,可将反应容器放在
(3)CaO2的相对分子质量为
(4)为测定制得的过氧化钙晶体中CaO2·8H2O的质量分数,设计的实验如下:称取晶体样品50g,加热到220℃充分反应(方程式为
 ,杂质不发生变化),测得生成氧气的质量为3.2g,请计算样品中CaO2·8H2O的质量分数
,杂质不发生变化),测得生成氧气的质量为3.2g,请计算样品中CaO2·8H2O的质量分数
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】锶有“金属味精”之称。以天青石(主要含有SrSO4和少量Fe2O3、MgO杂质)生产氢氧化锶的工艺如图:
已知氢氧化锶在水中的溶解度:

(1)隔绝空气焙烧时SrSO4只被还原成SrS,化学方程式为______ 。
(2)盐酸酸浸是将SrS溶解、脱硫,溶解过程中SrS与盐酸发生复分解反应生成SrCl2,并将硫元素以气体的形式脱去,该含硫气体的化学式为______ 。
(3)除杂时采取“趁热过滤”的目的是______ 。从趁热过滤后的滤液中获取氢氧化锶的步骤是:______ 、过滤、洗涤、干燥。证明洗涤干净的方法是______ 。
(4)取100g天青石样品,样品中含有质量分数为5%的杂质,酸浸步骤中有80%的Sr溶解,其他步骤均100%转化没有损耗,理论上可以获取纯净的氢氧化锶质量为____ 。(只列计算式)
(5)Sr和Ca的化学性质比较类似,推测SrO与水发生反应的化学方程式______ 。
已知氢氧化锶在水中的溶解度:

| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
| 溶解度(g) | 0.91 | 1.22 | 1.77 | 2.64 | 3.95 | 8.42 | 20.2 | 44.5 | 91.2 |
(2)盐酸酸浸是将SrS溶解、脱硫,溶解过程中SrS与盐酸发生复分解反应生成SrCl2,并将硫元素以气体的形式脱去,该含硫气体的化学式为
(3)除杂时采取“趁热过滤”的目的是
(4)取100g天青石样品,样品中含有质量分数为5%的杂质,酸浸步骤中有80%的Sr溶解,其他步骤均100%转化没有损耗,理论上可以获取纯净的氢氧化锶质量为
(5)Sr和Ca的化学性质比较类似,推测SrO与水发生反应的化学方程式
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐2】同学们在实验室废液桶中收集了含有大量FeSO4和CuSO4的废水,为防止废水直接排放到下水道造成重金属污染和浪费,设计了如下回收硫酸亚铁晶体和铜的实验方案:

(1)所加物质X是__________ 。加入溶液Y后发生反应的化学方程式为_________ 。
(2)根据流程可知,硫酸亚铁的溶解度随温度的升高而_________ 。
(3)某同学通过实验验证Ag、Fe、Cu三种金属的活动性顺序,下列所选试剂不可行的是________ 。
①Cu、Ag、FeSO4溶液
②Fe、Ag、CuSO4溶液
③Cu、FeSO4溶液、AgNO3溶液
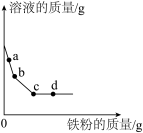
(4)向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Fe,溶液质量与加入Fe的质量关系如图所示,下列说法不正确的是_______。

(1)所加物质X是
(2)根据流程可知,硫酸亚铁的溶解度随温度的升高而
(3)某同学通过实验验证Ag、Fe、Cu三种金属的活动性顺序,下列所选试剂不可行的是
①Cu、Ag、FeSO4溶液
②Fe、Ag、CuSO4溶液
③Cu、FeSO4溶液、AgNO3溶液
(4)向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Fe,溶液质量与加入Fe的质量关系如图所示,下列说法不正确的是_______。

| A.a点溶液中的溶质有2种 |
| B.在b-c段溶液中,没有硝酸银剩余 |
| C.取d点的固体,加入稀盐酸,有气泡产生 |
| D.从该图像可以判断Fe、Cu、Ag金属的活动性顺序 |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
【推荐3】如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,回答下列问题。
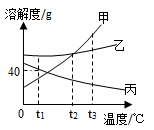
①t3℃ 时,物质甲、乙、丙的溶解度由小到大的是____ 。
②t1℃时,将25g丙加入到50g水中充分溶解后所得溶液的质量为____ 。
③甲中含有少量的乙,欲提纯甲应采用的方法是____ 。
④将100g10%的甲溶液稀释到4%需加入____ 水。
⑤t3℃时,将甲、乙、丙三种物质的饱和溶液降温至t1℃时,这时三种溶液的溶质质量分数由大到小是___________ 。

①t3℃ 时,物质甲、乙、丙的溶解度由小到大的是
②t1℃时,将25g丙加入到50g水中充分溶解后所得溶液的质量为
③甲中含有少量的乙,欲提纯甲应采用的方法是
④将100g10%的甲溶液稀释到4%需加入
⑤t3℃时,将甲、乙、丙三种物质的饱和溶液降温至t1℃时,这时三种溶液的溶质质量分数由大到小是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐1】NaCl、KNO3的部分溶解度数据见下表。
(1)20℃时,硝酸钾的溶解度是___________ 。
(2)氯化钠和硝酸钾在___________ 温度范围内可能溶解度相等。
(3)20℃时,称取60g硝酸钾固体加入100g水中,充分溶解后得到___________ (选填“饱和”或“不饱和”)溶液,溶液质量为___________ 。将此溶液升温至60℃,所得溶液的溶质质量分数是___________ 。
(4)从含有84.5g硝酸钾和19g氯化钠的混合物中提纯硝酸钾,进行如下实验。(实验中不考虑各种损耗)
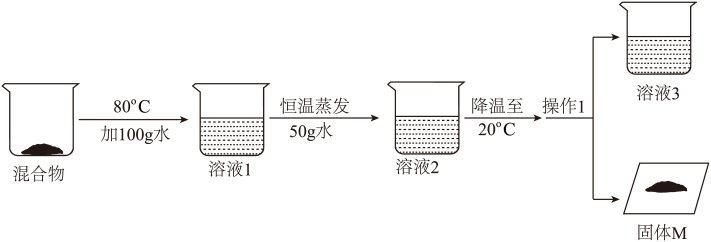
I、操作1的名称___________ 。
II、溶液1、2、3中关于溶质硝酸钾的溶质质量分数大小关系___________ (用“1”、“2”、“3”表示)。
III、固体M的成分___________ 及质量是___________ 。
IV、对整个实验过程分析正确的是___________ 。
A.60℃~80℃开始析出晶体
B.硝酸钾在整个过程中一直保持饱和状态
C.上述方法能将氯化钠和硝酸钾完全分离
D.若溶液1直接降温至20℃,析出硝酸钾的质量变少
| 温度 | 10 | 20 | 30 | 40 | 60 | 80 | 100 | |
| 溶解度 (g/100g) | 硝酸钾 | 20.9 | 31.6 | 45.8 | 64 | 110 | 169 | 246 |
| 氯化钠 | 35.8 | 36 | 36.3 | 36.4 | 37 | 38.4 | 39.8 |
(1)20℃时,硝酸钾的溶解度是
(2)氯化钠和硝酸钾在
(3)20℃时,称取60g硝酸钾固体加入100g水中,充分溶解后得到
(4)从含有84.5g硝酸钾和19g氯化钠的混合物中提纯硝酸钾,进行如下实验。(实验中不考虑各种损耗)

I、操作1的名称
II、溶液1、2、3中关于溶质硝酸钾的溶质质量分数大小关系
III、固体M的成分
IV、对整个实验过程分析正确的是
A.60℃~80℃开始析出晶体
B.硝酸钾在整个过程中一直保持饱和状态
C.上述方法能将氯化钠和硝酸钾完全分离
D.若溶液1直接降温至20℃,析出硝酸钾的质量变少
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐2】如表为两种物质在不同温度时的溶解度,请回答
(1)60℃时,100g 水中最多可溶解_______ gKCl 即可达到饱和
(2)40℃时,将 30gKCl加入到 50g 水中,充分溶解后所得溶液是_______ 溶液(填写“饱和”或“不饱和”);
(3)从表中信息可知,在______ 温度范围内 KNO3 和 KCl 的溶解度相等
(4)将 20℃时 KNO3 和 KCl 的两种饱和溶液升温至 60℃,则两种溶液的溶质质量分数大小关系是:KNO3_________________________ KCl(填写“>”、“<”或“=”).
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | KCl | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 | 56.7 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
(2)40℃时,将 30gKCl加入到 50g 水中,充分溶解后所得溶液是
(3)从表中信息可知,在
(4)将 20℃时 KNO3 和 KCl 的两种饱和溶液升温至 60℃,则两种溶液的溶质质量分数大小关系是:KNO3
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐1】某兴趣小组利用废镍材料(含有金属Ni及少量Fe、Ag)探究相关物质的性质并回收镍,设计流程如图1所示(部分产物略去)。
查阅资料:
a.H2O2溶液可将Fe2+转化为Fe3+。
b. Fe3+、Ni2+转化为对应的氢氧化物沉淀时溶液pH如图2。

(1)步骤Ⅰ的操作名称为_____ 。
(2)步骤Ⅱ中反应后铁元素的化合价______ (选填“升高”或“降低”或“不变”)。
(3)滤液②中有Ni2+、无Fe3+,则滤液②pH可能为_______(填序号)。
(4)Ni、Fe、Ag三种金属的活动性由强到弱的顺序为______ 。
查阅资料:
a.H2O2溶液可将Fe2+转化为Fe3+。
b. Fe3+、Ni2+转化为对应的氢氧化物沉淀时溶液pH如图2。

(1)步骤Ⅰ的操作名称为
(2)步骤Ⅱ中反应后铁元素的化合价
(3)滤液②中有Ni2+、无Fe3+,则滤液②pH可能为_______(填序号)。
| A.pH=2 | B.pH=4 | C.pH=6 | D.pH=10 |
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐2】为了除去NaCl溶液中含有少量的MgCl2、CaCl2和Na2SO4等杂质,某小组同学选用Na2CO3溶液、稀盐酸、Ba(OH)2溶液三种试剂,按一定的顺序进行如图所示的实验。
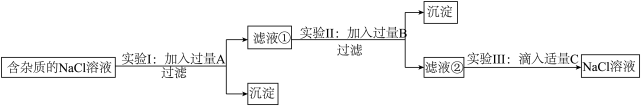
回答下列问题:
(1)实验Ⅰ中加入试剂A除去的杂质是_________ 。
(2)实验Ⅱ中加入的试剂B是_________ 溶液;加入过量B的目的是__________ 。
(3)滤液②中除Na+和Cl-外,还含有的离子是__________ (填离子符号)。
(4)实验Ⅲ中发生的中和反应的化学方程式__________ 。
(5)由所得NaCl溶液制成氯化钠晶体,所需操作为_________ 。

回答下列问题:
(1)实验Ⅰ中加入试剂A除去的杂质是
(2)实验Ⅱ中加入的试剂B是
(3)滤液②中除Na+和Cl-外,还含有的离子是
(4)实验Ⅲ中发生的中和反应的化学方程式
(5)由所得NaCl溶液制成氯化钠晶体,所需操作为
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
真题
解题方法
【推荐3】构建知识网络是学习化学的重要方法,下图是不同物质间相互转化关系图。其中 A、B、C、D属于不同类别的物质,且都含有铜元素,B为黑色粉末,C为红色粉末。“→”表示一种物质一步转化成另一种物质(部分反应物、生成物及反应条件未标出),请回答问题:
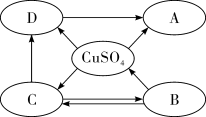
(1)C的化学式____________ , A的化学式____________ ;
(2)写出由B生成硫酸铜的化学方程式_______________ ;
(3)在该知识网络所涉及的化学反应中,可以归纳出能与盐发生反应的物质类别有______ 。
A.单质
B.氧化物
C.酸
D.碱
E.盐

(1)C的化学式
(2)写出由B生成硫酸铜的化学方程式
(3)在该知识网络所涉及的化学反应中,可以归纳出能与盐发生反应的物质类别有
A.单质
B.氧化物
C.酸
D.碱
E.盐
您最近一年使用:0次





