根据提供的实验装置回答问题。
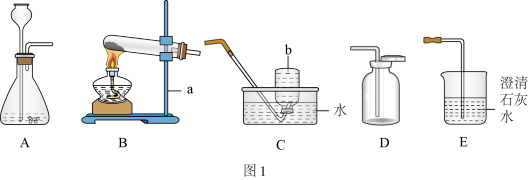
(1)写出实验仪器名称:a为_____ 。
(2)实验室制取、收集CO2的发生和收集装置是_____ (填字母序号),实验室制取CO2的化学方程式是_____ 。
(3)CO2能与NaOH发生反应。
【实验过程】检查装置气密性。如图2所示连接好装置。进行实验。
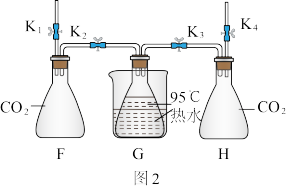
【实验分析】锥形瓶G中热水剧烈沸腾的原因是_____ 。
【实验反思】有观点认为只需要进行实验操作Ⅱ,即可说明CO2与NaOH发生反应。你对该观点的看法及理由是_____ 。
(4)实验室用B装置制取O2,发生反应的化学方程式为_____ 。
【查阅资料】KMnO4溶液呈中性、有腐蚀性
【进行实验】
实验1:将新鲜鸡皮在不同浓度的KMnO4溶液中浸泡相同时间,现象如表
实验2:将铜片分别浸泡在4种浸泡相同时间,现象如下表。
【解释与结论】
(5)实验1的目的是_____ 。
(6)实验2中,欲得出“KMnO4和硫酸共同作用对铜才有腐蚀性”的结论,需要对比_____ (填编号)。
(7)实验2中,铜片被腐蚀的反应如下,补全该反应的化学方程式。5Cu+2KMnO4+8H2SO4=5CuSO4+2MnSO4+K2SO4+_____ 。

(1)写出实验仪器名称:a为
(2)实验室制取、收集CO2的发生和收集装置是
(3)CO2能与NaOH发生反应。
【实验过程】检查装置气密性。如图2所示连接好装置。进行实验。

| 序号 | 操作步骤 | 实验现象 |
| I | 打开弹簧夹K1,关闭弹簧夹K2、K3、K4,将20mL水注入锥形瓶F中,关闭弹簧夹K1,振荡瓶F,打开弹簧夹K2 | 无明显现象 |
| II | 关闭弹簧夹K2,打开弹簧夹K4,将20mLNaOH溶液注入锥形瓶H中,关闭弹簧夹K4,振荡瓶H,打开弹簧夹K3 | 锥形瓶G中的热水剧烈沸腾 |
【实验反思】有观点认为只需要进行实验操作Ⅱ,即可说明CO2与NaOH发生反应。你对该观点的看法及理由是
(4)实验室用B装置制取O2,发生反应的化学方程式为
【查阅资料】KMnO4溶液呈中性、有腐蚀性
【进行实验】
实验1:将新鲜鸡皮在不同浓度的KMnO4溶液中浸泡相同时间,现象如表
| KMnO4溶液浓度 | 0.002% | 0.01% | 0.1% | 1% |
| 鸡皮的变化 | 无明显变化 | 边缘部分变为棕黄色 | 全部变为棕色 | 全部变为黑色 |
| 编号 | ① | ② | ③ | ④ | |
| 实验 | 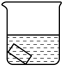 25mL0.1%KMnO4溶液 | 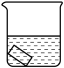 25mL0.1%KMnO4溶液+10滴浓硫酸 | 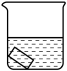 25mL蒸馏水+10滴浓硫酸 | 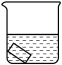 25mL1%KMnO4溶液+10滴浓硫酸 | |
| 铜片 质量/g | 实验前 | 0.54 | 0.54 | 0.54 | 0.54 |
| 18小时后 | 0.54 | 0.52 | 0.54 | 0.43 | |
(5)实验1的目的是
(6)实验2中,欲得出“KMnO4和硫酸共同作用对铜才有腐蚀性”的结论,需要对比
(7)实验2中,铜片被腐蚀的反应如下,补全该反应的化学方程式。5Cu+2KMnO4+8H2SO4=5CuSO4+2MnSO4+K2SO4+
更新时间:2021-01-01 22:36:28
|
相似题推荐
综合应用题
|
适中
(0.65)
【推荐1】中国古代四大发明之一的“黑火药”是由木炭(C)、硫粉(S)和硝酸钾(KNO3)按一定比例混合而成。
(1)“黑火药”爆炸时发生的主要反应是:S+2KNO3+3C═K2S+3CO2↑+______ ↑。
(2)古代曾用硝土[含有Ca(NO3)2、少量NaCl等]和草木灰(含有K2CO3)作原料制取KNO3。某化学兴趣小组设计了如下实验流程:
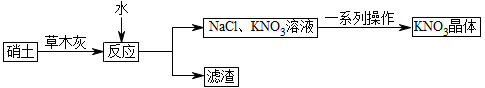
“反应”过程中的化学方程式为______ 。
(3)现代国防、开矿等使用的烈性炸药,主要成分为硝化甘油(C3H5O9N3)。硝化甘油在人体内能缓慢氧化生成一种氮的氧化物,用于治疗心绞痛。合成硝化甘油的化学方程式为C3H8O3+3HNO3═C3H5O9N3+3H2O。现用100g质量分数为37.8%硝酸和足量甘油反应,理论上可以生成多少硝化甘油?______ (写出计算过程)
(1)“黑火药”爆炸时发生的主要反应是:S+2KNO3+3C═K2S+3CO2↑+
(2)古代曾用硝土[含有Ca(NO3)2、少量NaCl等]和草木灰(含有K2CO3)作原料制取KNO3。某化学兴趣小组设计了如下实验流程:

“反应”过程中的化学方程式为
(3)现代国防、开矿等使用的烈性炸药,主要成分为硝化甘油(C3H5O9N3)。硝化甘油在人体内能缓慢氧化生成一种氮的氧化物,用于治疗心绞痛。合成硝化甘油的化学方程式为C3H8O3+3HNO3═C3H5O9N3+3H2O。现用100g质量分数为37.8%硝酸和足量甘油反应,理论上可以生成多少硝化甘油?
您最近一年使用:0次
【推荐2】2021年3月22日是“世界水日”。请根据下列情况回答问题。
(1)下图是自来水生产流程的简化图:
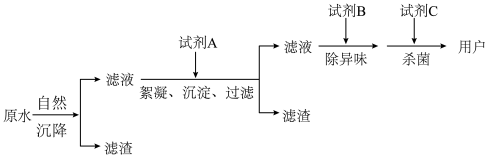
①流程中起到絮凝作用的试剂A常用______ (填物质名称)。
②流程中的“过滤”在实验室中常用的玻璃仪器有:烧杯、玻璃棒和______ 。过滤时,玻璃棒的作用是______ 。
③检验净化后的水是软水或硬水的方法是______ (填序号)。
A.用肥皂水 B.加热煮沸 C.蒸馏
④自来水中含有少量碳酸氢钙【化学式为Ca(HCO3)2】等可溶性化合物,烧水时碳酸氢钙发生分解反应,Ca(HCO3)2 CaCO3↓+X+CO2↑,这就是壶中出现水垢的原因之一、请写X的化学式
CaCO3↓+X+CO2↑,这就是壶中出现水垢的原因之一、请写X的化学式______ 。
(2)如图是电解水的使用装置图。回答下列问题。

①气体a可用______ 检验。
②该实验进行时,a、b之间的装置(漏斗)内的液面______ (填“上升”或“下降”)。
③写出电解水的化学方程式______ ,通过该实验可以得出水由______ 组成。
(1)下图是自来水生产流程的简化图:

①流程中起到絮凝作用的试剂A常用
②流程中的“过滤”在实验室中常用的玻璃仪器有:烧杯、玻璃棒和
③检验净化后的水是软水或硬水的方法是
A.用肥皂水 B.加热煮沸 C.蒸馏
④自来水中含有少量碳酸氢钙【化学式为Ca(HCO3)2】等可溶性化合物,烧水时碳酸氢钙发生分解反应,Ca(HCO3)2
 CaCO3↓+X+CO2↑,这就是壶中出现水垢的原因之一、请写X的化学式
CaCO3↓+X+CO2↑,这就是壶中出现水垢的原因之一、请写X的化学式(2)如图是电解水的使用装置图。回答下列问题。

①气体a可用
②该实验进行时,a、b之间的装置(漏斗)内的液面
③写出电解水的化学方程式
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐3】2023年6月,中国航天捷报频传,神舟十六号顺利升天,神舟十五号成功返回,航天梦,照亮中国科技兴国路,请回答下列问题:
(1)下表为航天器所用的燃料和氧化剂,请回答:
①上述所有物质中属于混合物的有________ (填名称),属于单质的有________ (填化学式)。
②标出高氯酸铵(NH4ClO4)中氯元素的化合价________ 。
③火箭中偏二甲肼(C2H8N2)与四氧化二氮(N2O4)点燃后,反应生成空气中最多气体和另外两种氧化物,并放出大量的热,请写出其化学方程式为:________ 。
(2)宇宙飞船所用的新型材料里其中应用了镁锂合金,请回答下列问题:
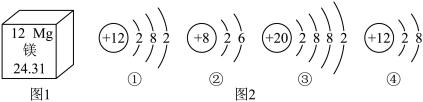
①图1为镁在元素周期表中的部分信息,则镁的相对原子质量为________ 。
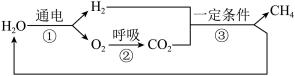
②图2为几种粒子的结构示意图,其中属于同种元素的是________ (填序号,下同),与镁元素化学性质相似的是________ 。
(3)天宫空间站中水气整合系统简易流程如图,该过程中,可循环利用的化合物是________ (填化学式),请写出反应③的化学方程式________ ,空间站内所需要的氧气来自水的电解,若实验室用10%的NaOH溶液配制200g4%的NaOH溶液用于电解实验,则需要10%的NaOH溶液________ g。
(4)航天员出舱需携带高压氧气罐,并将氧气罐集成到舱外航天服上,氧气可以压缩储存在氧气罐中的微观实质是________ ,此外,在航天服生命保障系统中还常用过氧化钠吸收航天员呼出的CO2,反应原理为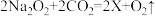 则X的化学式
则X的化学式________ ,若一定时间内航天员所排出CO2的质量为110g,若将其完全吸收,则同时产生氧气的体积为________ 升(通常状况下的氧气密度约为1.4g/L,计算结果精确到0.1),航天员在空间站内不需要穿笨重的航天服也能正常地生活和工作,则空间站为航天员提供的必要条件是________ 。
A.适宜的温度B.纯氧环境 C.饮用水 D.与地球相仿的气压
(5)神舟号载人飞船返回舱返回时,与大气剧烈摩擦,舱表面会产生数千度的高温,此时,舱表面的“烧蚀层”会汽化燃烧保护返回舱不因高温而烧毁。从燃烧的条件解释返回舱不会被烧毁的原因可能是________ ,返回舱的返回动力来自液氢和液氧,在即将着陆前要迅速释放剩余的燃料,这样做的目的是________ 。(答一点即可)
(1)下表为航天器所用的燃料和氧化剂,请回答:
| 一级火箭 | 二级火箭 | 三级火箭 | 固体燃料 | |
| 燃料 | 煤油 | 液氢 | 偏二甲肼(液态) | 铝粉 |
| 氧化剂 | 液氧 | 液氧 | 四氧化二氮(液态) | 高氯酸铵 |
②标出高氯酸铵(NH4ClO4)中氯元素的化合价
③火箭中偏二甲肼(C2H8N2)与四氧化二氮(N2O4)点燃后,反应生成空气中最多气体和另外两种氧化物,并放出大量的热,请写出其化学方程式为:
(2)宇宙飞船所用的新型材料里其中应用了镁锂合金,请回答下列问题:


①图1为镁在元素周期表中的部分信息,则镁的相对原子质量为
②图2为几种粒子的结构示意图,其中属于同种元素的是
(3)天宫空间站中水气整合系统简易流程如图,该过程中,可循环利用的化合物是
(4)航天员出舱需携带高压氧气罐,并将氧气罐集成到舱外航天服上,氧气可以压缩储存在氧气罐中的微观实质是
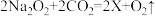 则X的化学式
则X的化学式A.适宜的温度B.纯氧环境 C.饮用水 D.与地球相仿的气压
(5)神舟号载人飞船返回舱返回时,与大气剧烈摩擦,舱表面会产生数千度的高温,此时,舱表面的“烧蚀层”会汽化燃烧保护返回舱不因高温而烧毁。从燃烧的条件解释返回舱不会被烧毁的原因可能是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】某课外兴趣小组用以下装置对二氧化碳的制取和性质进行探究。
(1)制取纯净、干燥的二氧化碳。
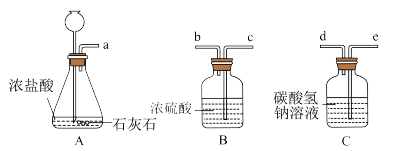
图中装置导管接口正确的连接顺序为:a接______ 、______ 接______ 。写出装置A发生反应的化学方程式______ 。
(2)若用下图装置收集二氧化碳(从n口进),将装置中导管补画完整。
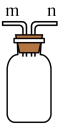
(3)二氧化碳性质的探究
利用图3装置研究CO2与NaOH的反应。用等体积的氢氧化钠溶液和蒸馏水分别进行实验,测得一段时间内压强的变化为图4所示。

①写出NaOH与CO2反应的化学方程式______ 。
②曲线______ (填“Ⅰ”或“Ⅱ")说明NaOH与CO2发生了反应,依据是______ 。
③请设计实验探究NaOH与CO2反应后溶液中溶质的成分______ 。(写出实验的操作、现象和结论)
(4)CO2和NH3在一定条件下反应生成尿素【CO(NH2)2】和水,该方法既可以生产尿素,又可以减少CO2的排放。若用该方法生产90t尿素,理论上可减少排放CO2的质量是多少?
(1)制取纯净、干燥的二氧化碳。

图中装置导管接口正确的连接顺序为:a接
(2)若用下图装置收集二氧化碳(从n口进),将装置中导管补画完整。

(3)二氧化碳性质的探究
利用图3装置研究CO2与NaOH的反应。用等体积的氢氧化钠溶液和蒸馏水分别进行实验,测得一段时间内压强的变化为图4所示。

①写出NaOH与CO2反应的化学方程式
②曲线
③请设计实验探究NaOH与CO2反应后溶液中溶质的成分
(4)CO2和NH3在一定条件下反应生成尿素【CO(NH2)2】和水,该方法既可以生产尿素,又可以减少CO2的排放。若用该方法生产90t尿素,理论上可减少排放CO2的质量是多少?
您最近一年使用:0次
【推荐2】到2060年,我国要实现“碳中和”,梦天化学兴趣小组以“简易吸碳机的制作”为项目开展探究,请你一起参与:
任务一:“捕风”——制作简易吸风机
兴趣小组成员自制捕风装置——简易吸风机(如图1),左侧是利用负压吸风动力装置,右侧是滤网,接通电后,吸风机风扇旋转产生内外压强差将空气自右向左吸进简易吸风机,完成捕风任务。
任务二:“捉碳”——探寻适宜的 吸收剂
吸收剂
兴趣小组向装有 气体的塑料瓶内倒入不同种类的吸收剂,实验数据及现象如下:
气体的塑料瓶内倒入不同种类的吸收剂,实验数据及现象如下:
采用振荡吸收法比较不同吸收剂的吸收效果
(1)30mL水这一组实验的作用是_____ 。
(2)写出用澄清石灰水做吸收剂时反应的化学方程式_____ 。
(3)从上述实验得到的结论是_____ 。
(4)将吸风机过滤网倒扣在石灰乳中,蘸取一定量的石灰乳后,通电后发现吸风效果变差,其原因是_____ 。
兴趣小组在老师的帮助下,查阅相关资料如下:
资料1:20℃时,几种常见物质的溶解度
资料2:碳酸盐能与 、
、 反应
反应
(5)你认为哪种物质最不适合作为 吸收剂?
吸收剂?_____ ,说明理由:_____ 。
经实验探究,氢氧化钾更适合用于简易吸碳机。
任务三:“释碳”——吸收剂再生与碳释放再利用
兴趣小组设计了吸收并释放 方案,其流程如图2所示:
方案,其流程如图2所示:_____ 种氧化物。
(7)请你设计实验证明滤液中不含 ,实验方案:
,实验方案:_____ 。
(8)除通过“碳捕集”实现碳中和外,请你再提出一条能实现碳中和的合理方案_____ 。
任务一:“捕风”——制作简易吸风机
兴趣小组成员自制捕风装置——简易吸风机(如图1),左侧是利用负压吸风动力装置,右侧是滤网,接通电后,吸风机风扇旋转产生内外压强差将空气自右向左吸进简易吸风机,完成捕风任务。

任务二:“捉碳”——探寻适宜的
 吸收剂
吸收剂兴趣小组向装有
 气体的塑料瓶内倒入不同种类的吸收剂,实验数据及现象如下:
气体的塑料瓶内倒入不同种类的吸收剂,实验数据及现象如下:采用振荡吸收法比较不同吸收剂的吸收效果
| 水 | 澄清石灰水 | 石灰乳 |  固体 固体 |
|
 |
 |
 固体 固体 |
(1)30mL水这一组实验的作用是
(2)写出用澄清石灰水做吸收剂时反应的化学方程式
(3)从上述实验得到的结论是
(4)将吸风机过滤网倒扣在石灰乳中,蘸取一定量的石灰乳后,通电后发现吸风效果变差,其原因是
兴趣小组在老师的帮助下,查阅相关资料如下:
资料1:20℃时,几种常见物质的溶解度
| 物质 | NaOH | KOH |  |  |  |
| 溶解度/g | 109 | 112 | 3.89 | 21.8 | 111 |
 、
、 反应
反应(5)你认为哪种物质最不适合作为
 吸收剂?
吸收剂?经实验探究,氢氧化钾更适合用于简易吸碳机。
任务三:“释碳”——吸收剂再生与碳释放再利用
兴趣小组设计了吸收并释放
 方案,其流程如图2所示:
方案,其流程如图2所示: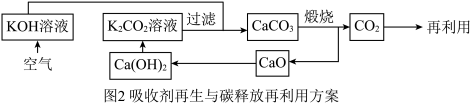
(7)请你设计实验证明滤液中不含
 ,实验方案:
,实验方案:(8)除通过“碳捕集”实现碳中和外,请你再提出一条能实现碳中和的合理方案
您最近一年使用:0次
【推荐3】酸、碱、盐在生活、生产中有着广泛的应用。
(1)在实验室中常用浓硫酸作干燥剂,是利用了浓硫酸的_____ (填字母)。
a.腐蚀性 b.吸水性 c.氧化性 d.酸性
(2)用稀盐酸除铁锈的化学方程式为_____ 。
(3)如图1所示,向充满CO2气体的烧瓶中,注入100mL饱和氢氧化钠溶液,关闭活塞;连接压强传感器,观察到烧瓶内气压变化图像如图2所示。

①用文字描述烧瓶内压强减小的原因:_____ 。
②如何确定反应后烧瓶中溶液是否还含有NaOH:_____ 。(请叙述操作、现象、结论)
(4)从海水得到的粗盐中往往含有泥沙和氯化钙、氯化镁、硫酸钠等杂质,某化学兴趣小组取少量粗盐样品在实验室进行了如下实验:

①操作②中用到的玻璃仪器有玻璃棒、_____ 、烧杯。
②按照上图所示实验流程,加入过量的碳酸钠的目的是:_____ 。
③写出加入稀盐酸后所发生的反应的化学方程式:_____ 。(写出一个即可)
(5)食用碱的主要成分是碳酸钠,其中含少量氯化钠。取一定质量某品牌食用碱样品投入烧杯中,加入足量的水,搅拌后加入200g溶质质量分数为11.1%的氯化钙溶液,二者恰好完全反应,则该品牌食用碱样品中碳酸钠的质量为多少?
(1)在实验室中常用浓硫酸作干燥剂,是利用了浓硫酸的
a.腐蚀性 b.吸水性 c.氧化性 d.酸性
(2)用稀盐酸除铁锈的化学方程式为
(3)如图1所示,向充满CO2气体的烧瓶中,注入100mL饱和氢氧化钠溶液,关闭活塞;连接压强传感器,观察到烧瓶内气压变化图像如图2所示。

①用文字描述烧瓶内压强减小的原因:
②如何确定反应后烧瓶中溶液是否还含有NaOH:
(4)从海水得到的粗盐中往往含有泥沙和氯化钙、氯化镁、硫酸钠等杂质,某化学兴趣小组取少量粗盐样品在实验室进行了如下实验:

①操作②中用到的玻璃仪器有玻璃棒、
②按照上图所示实验流程,加入过量的碳酸钠的目的是:
③写出加入稀盐酸后所发生的反应的化学方程式:
(5)食用碱的主要成分是碳酸钠,其中含少量氯化钠。取一定质量某品牌食用碱样品投入烧杯中,加入足量的水,搅拌后加入200g溶质质量分数为11.1%的氯化钙溶液,二者恰好完全反应,则该品牌食用碱样品中碳酸钠的质量为多少?
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
解题方法
【推荐1】根据如图装置,结合所学化学知识,回答下列问题。
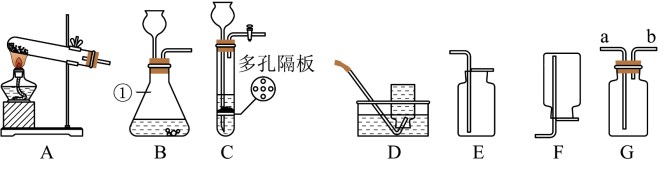
(1)写出仪器①的名称为___________ 。
(2)若用A装置制取氧气,反应的化学方程式为_________ 。
(3)实验室制取二氧化碳的发生装置可选用装置B。
①请在如图中将装置B补充完整_______ ;
②如何检查装置B的气密性_______ ?
③若用装置C制取二氧化碳,与装置B相比,其优点是什么_______ ?
(4)已知:氨气是一种具有刺激性气味的无色气体,密度比空气小,极易溶于水,实验室常用加热氯化铵和熟石灰的固体混合物来制取氨气,请你从图中选择制取一瓶氨气所需要的发生装置与收集装置_____ (填标号),若用G装置收集气体,进气端口为_____ 。
(5)化学兴趣小组取30g石灰石样品(杂质不参加反应,也不溶于水)放在烧杯中,向其中加入90g稀盐酸,恰好完全反应,反应后烧杯中物质的总质量为109g,计算石灰石中碳酸钙的质量_____ 。

(1)写出仪器①的名称为
(2)若用A装置制取氧气,反应的化学方程式为
(3)实验室制取二氧化碳的发生装置可选用装置B。
①请在如图中将装置B补充完整

②如何检查装置B的气密性
③若用装置C制取二氧化碳,与装置B相比,其优点是什么
(4)已知:氨气是一种具有刺激性气味的无色气体,密度比空气小,极易溶于水,实验室常用加热氯化铵和熟石灰的固体混合物来制取氨气,请你从图中选择制取一瓶氨气所需要的发生装置与收集装置
(5)化学兴趣小组取30g石灰石样品(杂质不参加反应,也不溶于水)放在烧杯中,向其中加入90g稀盐酸,恰好完全反应,反应后烧杯中物质的总质量为109g,计算石灰石中碳酸钙的质量
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】实验室常用如图装置制取气体,回答问题:
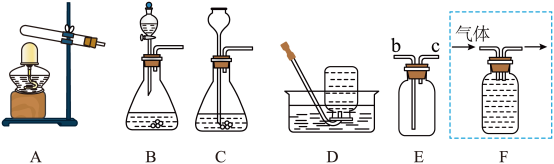
(1)若用AD装置制取并收集氧气,发现收集氧气时,水槽中的水有点发红,原因是_______ ,请写出有关反应的化学方程式_______ 。
(2)用BC装置均可以制取氧气,与C装置相比B装置的优点是_______ ,若用E装置收集氧气应该怎样验满?_______ 。
(3)若制取的O2用F装置采用排水法收集,请将图F补画完整____ 。
(4)实验室加热熟石灰和氯化铵制取氨气,写出应选用的发生装置的序号为_______ ,并说明其原因_______ 。
(5)实验室加热氯酸钾(KClO3)和二氧化锰的固体混合物28.0g制取氧气,完全反应后,剩余固体质量为18.4g。请计算原固体混合物中氯酸钾的质量____ 。

(1)若用AD装置制取并收集氧气,发现收集氧气时,水槽中的水有点发红,原因是
(2)用BC装置均可以制取氧气,与C装置相比B装置的优点是
(3)若制取的O2用F装置采用排水法收集,请将图F补画完整
(4)实验室加热熟石灰和氯化铵制取氨气,写出应选用的发生装置的序号为
(5)实验室加热氯酸钾(KClO3)和二氧化锰的固体混合物28.0g制取氧气,完全反应后,剩余固体质量为18.4g。请计算原固体混合物中氯酸钾的质量
您最近一年使用:0次
【推荐3】实验室制取气体是化学学习者必备的技能。
(1)在实验室用氯酸钾、二氧化锰制取氧气,要选择下图仪器中的_______ (填仪器编号),反应的化学方程式是_______ 。

(2)某种气体可用下图所示装置进行制备。下列有关推测,合理的是 。(填编号)

(3)影响过氧化氢分解速率的因素有很多,升温或者加入MnO2、CuSO4都能加快其分解;但NaC1、Na2SO4对其分解无影响。某小组测得70°C时,不同条件下H2O2的质量分数随时间的变化结果如下图所示。
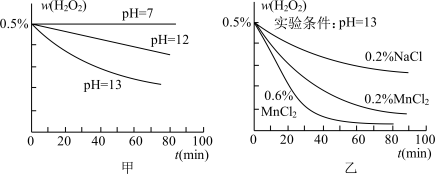
请回答以下问题:
①图甲表明,其他条件不变时,溶液的pH越_______ ,H2O2分解越快。
②图乙表明,碱性条件下,_______ (填离子符号)对H2O2分解速率的影响大。
③综合以上信息推测,下列物质可加快H2O2分解的是_______ (填编号)。
A.KOH B.KCl C.HCl D.MnSO4
(1)在实验室用氯酸钾、二氧化锰制取氧气,要选择下图仪器中的

(2)某种气体可用下图所示装置进行制备。下列有关推测,合理的是 。(填编号)

| A.反应有水生成 | B.反应需要加热才能进行 |
| C.该气体的密度比空气大 | D.该气体易溶于水 |
| E.该气体能与NaOH溶液反应 | |
(3)影响过氧化氢分解速率的因素有很多,升温或者加入MnO2、CuSO4都能加快其分解;但NaC1、Na2SO4对其分解无影响。某小组测得70°C时,不同条件下H2O2的质量分数随时间的变化结果如下图所示。

请回答以下问题:
①图甲表明,其他条件不变时,溶液的pH越
②图乙表明,碱性条件下,
③综合以上信息推测,下列物质可加快H2O2分解的是
A.KOH B.KCl C.HCl D.MnSO4
您最近一年使用:0次
【推荐1】二氧化碳是碳循环中的重要物质。
(1)实验室可用如图所示的装置制备二氧化碳,反应的化学方程式是_______ 。长颈漏斗的末端要伸入多孔隔板下的原因是_______ 。装置中弹簧夹的作用是_______ 。

(2)为研究二氧化碳与氢氧化钙溶液、氢氧化钠溶液的反应情况,社团同学进行如下图所示实验(装置气密性良好)。
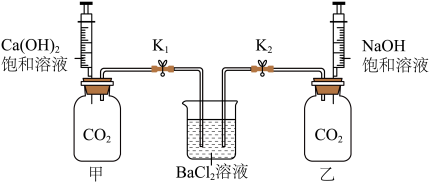
(3)社团同学最后对制取二氧化碳后的废液中是否含有盐酸进行了检验,其中可选择的试剂是_______。
(1)实验室可用如图所示的装置制备二氧化碳,反应的化学方程式是

(2)为研究二氧化碳与氢氧化钙溶液、氢氧化钠溶液的反应情况,社团同学进行如下图所示实验(装置气密性良好)。

| 实验步骤 | 现象 | |
| 甲装置 | 乙装置 | |
| ①分别向充满CO2的甲乙两个等体积集气瓶中,注入等体积的Ca(OH)2饱和溶液和NaOH饱和溶液 | 无明显现象 | |
| ②稍后打开弹簧夹K1、K2 | 烧杯中少量液体倒流入甲中 | |
| 结论:I.证明CO2能与NaOH发生反应,该反应的化学方程式是 Ⅱ.相同条件下, | ||
(3)社团同学最后对制取二氧化碳后的废液中是否含有盐酸进行了检验,其中可选择的试剂是_______。
| A.Zn粒 | B.AgNO3溶液 | C.酚酞 | D.Na2CO3固体 |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐2】“实验创新”又一化学核心素养。
用“W”型玻璃管进行微型实验模拟冶铁,如图所示:
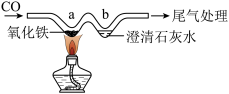
(1)实验时一定要先通气一会再加热,理由是_____
(2)a处可观察红棕色粉末变为黑色,在b处发生的有关反应方程式的;_____
(3)若用如图装置收集与处理尾气,正确的导管接口连接顺序是______

经资料查阅,一氧化碳还可以用氯化亚铜溶液吸收生成复合物也可防止一氧化碳污染空气。
请回答:两种吸收设计中图2较图1的最大优点是______
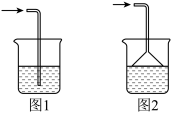
(4)若实验前后测得红棕色粉末的质量减少了1.6g,则生成二氧化碳的质量是___
(5)若在清洗实验“W”型玻璃管前,从左端滴入一定量的硝酸银溶液于a处,还可完成金属的性质实验之一,有关化学反应方程式______
用“W”型玻璃管进行微型实验模拟冶铁,如图所示:

(1)实验时一定要先通气一会再加热,理由是
(2)a处可观察红棕色粉末变为黑色,在b处发生的有关反应方程式的;
(3)若用如图装置收集与处理尾气,正确的导管接口连接顺序是

经资料查阅,一氧化碳还可以用氯化亚铜溶液吸收生成复合物也可防止一氧化碳污染空气。
请回答:两种吸收设计中图2较图1的最大优点是

(4)若实验前后测得红棕色粉末的质量减少了1.6g,则生成二氧化碳的质量是
(5)若在清洗实验“W”型玻璃管前,从左端滴入一定量的硝酸银溶液于a处,还可完成金属的性质实验之一,有关化学反应方程式
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐3】某兴趣小组利用下列装置进行氧气的制取实验,请回答下列问题。
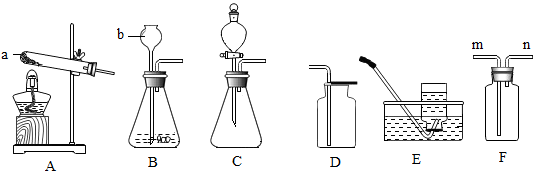
①写出标号a仪器的名称________ ;标号b仪器的名称 ______ 。
②用氯酸钾和二氧化锰制取较纯氧气的装置组合是______ (填字母);用D装置收集氧气,检验氧气集满的方法是 ________ (写明操作、现象、结论)。
③用过氧化氢溶液制备氧气可用装置B和C,指出用装置C制备氧气的优点____ 。
④若用装置F收集氧气(从n端进入),该如何操作?_________ 。
⑤含溶质0.2mol的过氧化氢溶液在二氧化锰的催化作用下,完全分解能生成氧气几____ mol(根据化学方程式列式计算)?
⑥化学兴趣小组借助数字化实验手段用装置C探究“外界条件对过氧化氢分解速率的影响”,按下表分组进行实验1,在同一温度下通过压强传感器得到的数据如下图所示。
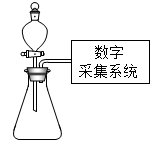
Ⅰ.经过分组实验,同学们从实验1中得出结论:在其他条件相同的情况下, ______ 作催化剂的催化效果最好。
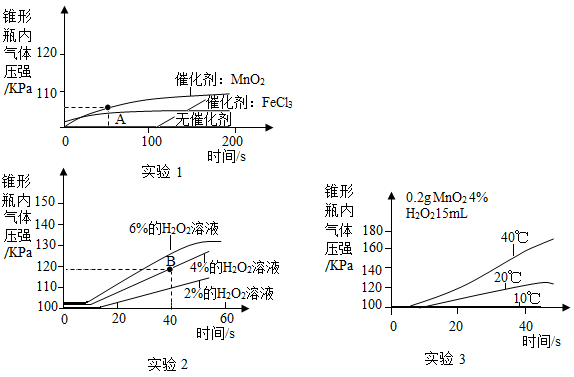
Ⅱ.选用0.2g的MnO2粉末作催化剂,同学们又分别做了实验2和实验3,得到的数据图表如上,你认为影响该反应速率的外界因素除催化剂外,还有_______ 。
Ⅲ.实验1与实验2中4%的过氧化氢溶液与0.2gMnO2粉末混合后产生的气体压强有明显不同(见实验1图中A点和实验2图中B点),你认为可能的原因是_________ 。

①写出标号a仪器的名称
②用氯酸钾和二氧化锰制取较纯氧气的装置组合是
③用过氧化氢溶液制备氧气可用装置B和C,指出用装置C制备氧气的优点
④若用装置F收集氧气(从n端进入),该如何操作?
⑤含溶质0.2mol的过氧化氢溶液在二氧化锰的催化作用下,完全分解能生成氧气几
⑥化学兴趣小组借助数字化实验手段用装置C探究“外界条件对过氧化氢分解速率的影响”,按下表分组进行实验1,在同一温度下通过压强传感器得到的数据如下图所示。

| 实验1 | 药品 |
| 第一组 | 4%H2O2溶液15ml |
| 第二组 | 4%H2O2溶液15ml0.2gMnO2粉末 |
| 第三组 | 4%H2O2溶液15ml0.2gFeCl3粉末 |

Ⅱ.选用0.2g的MnO2粉末作催化剂,同学们又分别做了实验2和实验3,得到的数据图表如上,你认为影响该反应速率的外界因素除催化剂外,还有
Ⅲ.实验1与实验2中4%的过氧化氢溶液与0.2gMnO2粉末混合后产生的气体压强有明显不同(见实验1图中A点和实验2图中B点),你认为可能的原因是
您最近一年使用:0次