根据下图中A、B、C三种物质的溶解度曲线,回答下列问题
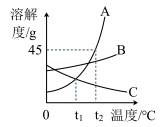
(1)现有A、B、C三种物质的浓溶液,适用海水晒盐原理结晶的是_____ ;
(2)t2℃时A、B、C三种物质的饱和溶液中溶质质量分数的大小顺序为_____ 。将这三种饱和溶液分别从t2℃降温到t1℃时,溶液中溶质质量分数最小的是(填物质的序号) _____ 。
(3)在t2℃时把50克A物质加入的100克水中,得到的溶液的总质量是_____ 克。
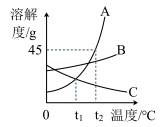
(1)现有A、B、C三种物质的浓溶液,适用海水晒盐原理结晶的是
(2)t2℃时A、B、C三种物质的饱和溶液中溶质质量分数的大小顺序为
(3)在t2℃时把50克A物质加入的100克水中,得到的溶液的总质量是
12-13九年级下·湖北宜昌·期中 查看更多[2]
更新时间:2016-11-28 11:27:28
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
【推荐1】如图是氯化钠与硝酸钾的溶解度曲线,回答下列问题。

(1)配制200g 0.9%的医用生理盐水,需要NaCl的质量为_________ g。
(2)由图可知,t1℃时,硝酸钾的溶解度_________ (填“>”、“<”或“=”)氯化钠的溶解度;欲提纯混有少量氯化钠的硝酸钾固体,应采用的方法是________ 。
(3)t2℃时,将50g硝酸钾固体完全溶于50g水,形成溶液的质量是__________ 。

(1)配制200g 0.9%的医用生理盐水,需要NaCl的质量为
(2)由图可知,t1℃时,硝酸钾的溶解度
(3)t2℃时,将50g硝酸钾固体完全溶于50g水,形成溶液的质量是
您最近半年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
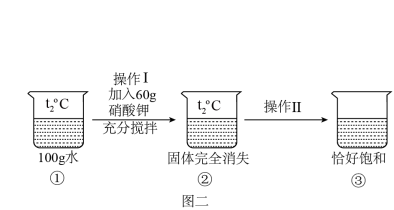
【推荐2】甲、乙两种固体的溶解度曲线如图一所示:

(1)t1℃时,乙的溶解度是_______ 。
(2)t2℃时,配制90g甲物质的饱和溶液,需称量甲的质量_______ 。
(3)甲的饱和溶液中含有少量的乙,要提纯甲,采用的方法是_______ 。
(4)由图二推测硝酸钾是图一中的_______ (填“甲”或“乙”)物质。
(5)图二操作Ⅱ前后的溶液状态变化过程,可以在图一中表示为_______(填字母)。


(1)t1℃时,乙的溶解度是
(2)t2℃时,配制90g甲物质的饱和溶液,需称量甲的质量
(3)甲的饱和溶液中含有少量的乙,要提纯甲,采用的方法是
(4)由图二推测硝酸钾是图一中的
(5)图二操作Ⅱ前后的溶液状态变化过程,可以在图一中表示为_______(填字母)。
| A.c点→a点 | B.c点→b 点 | C.c点→d点 | D.b点→a点 |
您最近半年使用:0次
【推荐3】根据NaCl和KNO3的部分溶解度数据,回答下列问题:
(1)0℃时,NaCl的溶解度为______ g 可得影响溶解度的因素有______ (任写一点即可)。
(2)KNO3中混有少量NaCl时,提纯硝酸钾的方法是______ 。
(3)按照下图进行实验,各步操作均已充分溶解,实验过程中溶剂的挥发不计

①a和b中溶质的质量分数:a______ b(用“<”“>”“=”填空,下同);a和d中溶剂质量:a______ d;如c和f上层清液溶质质量分数相等,则t℃的最小范围是______ 。
②e中溶质质量分数为______ ,b中是否是该温度下硝酸钾的饱和溶液?______ (填“是”“否”“不一定”)。
温度/℃ | 0 | 20 | 40 | |
溶解度g /100g水 | NaCl | 35.7 | 36.0 | 36.6 |
KNO3 | 13.3 | 31.6 | 63.9 | |
(1)0℃时,NaCl的溶解度为
(2)KNO3中混有少量NaCl时,提纯硝酸钾的方法是
(3)按照下图进行实验,各步操作均已充分溶解,实验过程中溶剂的挥发不计

①a和b中溶质的质量分数:a
②e中溶质质量分数为
您最近半年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】如图是A、B、C三种物质的溶解度曲线,回答下列问题:
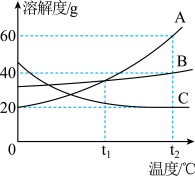
(1)欲将t2℃ 时B物质的不饱和溶液转化为该温度下的饱和溶液,可采取的方法是
时B物质的不饱和溶液转化为该温度下的饱和溶液,可采取的方法是___________ (填一种)。
(2)氧气的溶解度随温度变化的规律与图中的___________ (填A、B、C)相似。
(3)A中混有少量B,提纯A的方法是___________ 。
(4)t2℃时,100g20%的B溶液再加____________ gB可以恰好配成饱和溶液。
(5)t2℃时,将三种物质各ag分别加入100g水中,充分溶解后,若只有一种物质能形成饱和溶液则a的取值范围是___________ 。

(1)欲将t2℃
 时B物质的不饱和溶液转化为该温度下的饱和溶液,可采取的方法是
时B物质的不饱和溶液转化为该温度下的饱和溶液,可采取的方法是(2)氧气的溶解度随温度变化的规律与图中的
(3)A中混有少量B,提纯A的方法是
(4)t2℃时,100g20%的B溶液再加
(5)t2℃时,将三种物质各ag分别加入100g水中,充分溶解后,若只有一种物质能形成饱和溶液则a的取值范围是
您最近半年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】甲、乙两种物质的溶解度曲线如图所示。
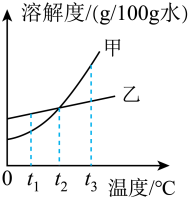
①_____ ℃时,甲、乙的溶解度相等。
②若甲中含有少量乙,提纯甲可采用的方法是_____ 。
③将t1℃时等质量的甲、乙饱和溶液升温至t2℃,若采用加溶质的方法使两者重新达到饱和,则_____ 物质所加的量多。
④t1℃时,向一只盛有15g甲的烧杯中加入50g水,充分搅拌后烧杯底部仍有未溶解的固体。下列相关叙述不正确的是_____

①
②若甲中含有少量乙,提纯甲可采用的方法是
③将t1℃时等质量的甲、乙饱和溶液升温至t2℃,若采用加溶质的方法使两者重新达到饱和,则
④t1℃时,向一只盛有15g甲的烧杯中加入50g水,充分搅拌后烧杯底部仍有未溶解的固体。下列相关叙述不正确的是
| A.t1℃时,甲的溶解度为30 g/100g水 |
| B.烧杯中溶液的质量小于65g |
| C.降温后烧杯中溶液总质量不变 |
| D.取烧杯中上层清液加热变为不饱和溶液 |
您最近半年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐3】下图是A、B、C三种固体的溶解度曲线,请据图回答下列问题:

(1)d点所表示的意义是_______ ,t1°C时,A、B、C三种物质的溶解度大小顺序为 _____
(2)t3°C时,30gA物质加入到50 g水中不断搅拌,所得溶液溶质质量分数为_____ (保留到0.1%)
(3)t3℃时,相同质量的A、B、C三种物质的饱和溶液降温至t1°C,析出晶体最多的是_____ ,此时三种物质的溶液的溶质质量分数由大到小的顺序是 ________ 。
(4)如图所示,试管内装有A、B、C三种物质之一的饱和溶液,向烧杯中的水中加入氢氧化钠固体,试管中有晶体析出。由此判断试管内的溶液是________ (填字母序号)物质的溶液。
(5)某同学在实验室用固体B和蒸馏水配制50 g质量分数为6%的B溶液时,涉及以下实验步骤:① 溶解② 称量和量取③ 计算④ 装入试剂瓶贴好标签。配制上述溶液正确的实验步骤顺序是____________ (填序号)。

(1)d点所表示的意义是
(2)t3°C时,30gA物质加入到50 g水中不断搅拌,所得溶液溶质质量分数为
(3)t3℃时,相同质量的A、B、C三种物质的饱和溶液降温至t1°C,析出晶体最多的是
(4)如图所示,试管内装有A、B、C三种物质之一的饱和溶液,向烧杯中的水中加入氢氧化钠固体,试管中有晶体析出。由此判断试管内的溶液是
(5)某同学在实验室用固体B和蒸馏水配制50 g质量分数为6%的B溶液时,涉及以下实验步骤:① 溶解② 称量和量取③ 计算④ 装入试剂瓶贴好标签。配制上述溶液正确的实验步骤顺序是
您最近半年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】如图是a、b、c三种固体物质(均不含结晶水)的溶解度曲线图。请根据图示回答下列问题:

(1)20℃时,溶解度最大的是__ (填序号);
(2)欲将c物质的饱和溶液变为不饱和溶液,可采用的方法是___ (填“降低”或“升高”)温度;
(3)若a中混有少量的c,提纯a的最佳方法是___ (填“降温结晶”或“蒸发结晶”);
(4)20℃时,向30g物质a中加入50g水,充分溶解并恢复到原温度,所得溶液中溶质的质量为__ g;

(1)20℃时,溶解度最大的是
(2)欲将c物质的饱和溶液变为不饱和溶液,可采用的方法是
(3)若a中混有少量的c,提纯a的最佳方法是
(4)20℃时,向30g物质a中加入50g水,充分溶解并恢复到原温度,所得溶液中溶质的质量为
您最近半年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】图1是a、b两种固体物质(不含结晶水)的溶解度曲线。t1℃时,分别向盛有10g水的A、B两支试管中加入等质量的a、b两种固体物质,使其充分溶解,现象如图2所示。
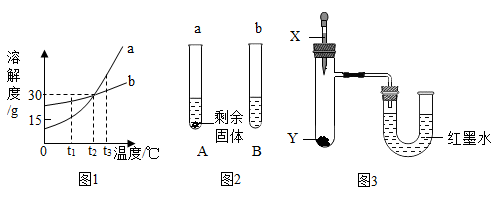
(1)t1℃时______ (填“ A”或“B”)试管中的溶液一定是饱和溶液。
(2)t2℃时,向100 g水中加入35 g a固体,发现固体全部溶解,一段时间后又有部分a的固体析出,则析出固体的质量是______ 。
(3)将t3℃时a,b两种物质的饱和溶液降温到t1℃,所得溶液中溶质的质量分数大小关系为a______ (填“>”、“<”或“=”)b。
(4)按图3所示装置,将液体x滴入装有固体y的试管中,会导致U形管中右端液面升高,则可能的组合是______ (填序号)。

(1)t1℃时
(2)t2℃时,向100 g水中加入35 g a固体,发现固体全部溶解,一段时间后又有部分a的固体析出,则析出固体的质量是
(3)将t3℃时a,b两种物质的饱和溶液降温到t1℃,所得溶液中溶质的质量分数大小关系为a
(4)按图3所示装置,将液体x滴入装有固体y的试管中,会导致U形管中右端液面升高,则可能的组合是
| 选项 | ① | ② | ③ | ④ |
| x | 水 | 水 | 水 | 水 |
| y | 氧化钙 | 硝酸铵 | 氯化钠 | 氢氧化钠 |
您最近半年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】下图是A、B、C三种物质的溶解度曲线。

(1)20°C时,A、B、C三种物质溶解度由大到小的顺序是_____________ 。
(2)B溶液中有少量的A,提纯B物质的方法是_____________ 。
(3)35℃时,A、B、C的饱和溶液各wg,均冷却至20°℃时,析出晶体最多的是_____________ ,没有晶体析出的是_____________ 。
(4)30°C时,把30gA物质加入50g水中,所得A溶液的质量分数溶液是_____________ 。

(1)20°C时,A、B、C三种物质溶解度由大到小的顺序是
(2)B溶液中有少量的A,提纯B物质的方法是
(3)35℃时,A、B、C的饱和溶液各wg,均冷却至20°℃时,析出晶体最多的是
(4)30°C时,把30gA物质加入50g水中,所得A溶液的质量分数溶液是
您最近半年使用:0次
【推荐1】请回答下列问题。
(1)齐鲁晚报报道2021年春节,为响应“就地过年”号召,济莱高铁建设项目部向全线2786名建设者达成共识,选择值守项目,为济莱建设做出贡献。


①如图高铁车头的玻璃是用无机玻璃、树脂、塑料等粘合而成,能耐受强大的撞击力,这种玻璃属于_______ 材料。
②高铁建设需要消耗大量的铝、铁等金属.工业上常用电解氧化铝的方法冶炼金属铝,写出该反应的化学方程式_______ ,该反应属于_______ (填字母序号)。
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
(2)1926年我国化学家侯德榜创立了“侯氏制碱法”,是原料氯化钠的利用率从70%提高到96%,也使得原来的副产物氯化钙转化成化肥NH4Cl,Na2CO3和NaCl的溶解度曲线如图所示,请回答。
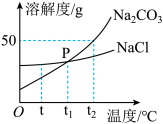
①P点的意义是_______ 。
②t2℃时,向盛有30gNa2CO3固体的烧杯中加入50g水,所得溶液中溶质的质量分数是_______ 。(精确到0.1%)
③t℃时,将相同质量的Na2CO3和NaCl的饱和溶液都升温至t2℃后(水分不蒸发),所得溶液的质量关系为Na2CO3 溶液_______ NaCl溶液。(填“大于 ”“小于”“等于”之一)
(1)齐鲁晚报报道2021年春节,为响应“就地过年”号召,济莱高铁建设项目部向全线2786名建设者达成共识,选择值守项目,为济莱建设做出贡献。


①如图高铁车头的玻璃是用无机玻璃、树脂、塑料等粘合而成,能耐受强大的撞击力,这种玻璃属于
②高铁建设需要消耗大量的铝、铁等金属.工业上常用电解氧化铝的方法冶炼金属铝,写出该反应的化学方程式
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
(2)1926年我国化学家侯德榜创立了“侯氏制碱法”,是原料氯化钠的利用率从70%提高到96%,也使得原来的副产物氯化钙转化成化肥NH4Cl,Na2CO3和NaCl的溶解度曲线如图所示,请回答。

①P点的意义是
②t2℃时,向盛有30gNa2CO3固体的烧杯中加入50g水,所得溶液中溶质的质量分数是
③t℃时,将相同质量的Na2CO3和NaCl的饱和溶液都升温至t2℃后(水分不蒸发),所得溶液的质量关系为Na2CO3 溶液
您最近半年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】如图为A、B、C三种物质的溶解度曲线,试根据图回答:
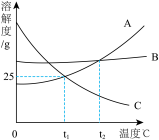
(1)______ ℃时,A和C两物质的溶解度相等。
(2)当温度大于 ℃时,三种物质的溶解度由小到大依次为
℃时,三种物质的溶解度由小到大依次为_______ 。
(3)若将C物质的饱和溶液转化为不饱和溶液,可采用的方法为_______ 。
(4)A的溶液中混有少量的B,提纯A通常采用_______ 结晶的方法。
(5) ℃时,将20g固体A加入50g水中,充分搅拌后,得到
℃时,将20g固体A加入50g水中,充分搅拌后,得到_______ g溶液。
(6) ℃时A、B、C的三种饱和溶液,升温到
℃时A、B、C的三种饱和溶液,升温到 ℃时,三种溶液的溶质质量分数由大到小是
℃时,三种溶液的溶质质量分数由大到小是_______ 。

(1)
(2)当温度大于
 ℃时,三种物质的溶解度由小到大依次为
℃时,三种物质的溶解度由小到大依次为(3)若将C物质的饱和溶液转化为不饱和溶液,可采用的方法为
(4)A的溶液中混有少量的B,提纯A通常采用
(5)
 ℃时,将20g固体A加入50g水中,充分搅拌后,得到
℃时,将20g固体A加入50g水中,充分搅拌后,得到(6)
 ℃时A、B、C的三种饱和溶液,升温到
℃时A、B、C的三种饱和溶液,升温到 ℃时,三种溶液的溶质质量分数由大到小是
℃时,三种溶液的溶质质量分数由大到小是
您最近半年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】如图是a、b、c三种物质的溶解度曲线,请结合图示回答问题:
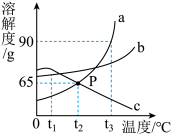
(1)P点的含义是t2℃时,a、c溶解度都为________ 。
(2)t3 ℃时,50 g a放入50 g水中形成的溶液中溶质和溶剂的质量比为________ 。若再加10g、t3℃的水,此时该溶液为__________ (选填“饱和”或“不饱和”)溶液
(3)下列说法正确的是________ 。
①t2 ℃时,b的溶液中溶质的质量分数一定比a、c的溶液中溶质的质量分数大;
②将t3 ℃时,a、c的饱和溶液分别降温至t2 ℃,此时两溶液中溶质的质量分数相等;
③当a中混有少量b时,可用降温结晶的方法提纯a
④在t1 ℃时,把等质量的a、b、c三种物质分别配制成饱和溶液,所得溶液质量由大到小的顺序为a>b>c
⑤将t3 ℃时,a、b的饱和溶液分别降温至t1℃,析出晶体的质量a>b

(1)P点的含义是t2℃时,a、c溶解度都为
(2)t3 ℃时,50 g a放入50 g水中形成的溶液中溶质和溶剂的质量比为
(3)下列说法正确的是
①t2 ℃时,b的溶液中溶质的质量分数一定比a、c的溶液中溶质的质量分数大;
②将t3 ℃时,a、c的饱和溶液分别降温至t2 ℃,此时两溶液中溶质的质量分数相等;
③当a中混有少量b时,可用降温结晶的方法提纯a
④在t1 ℃时,把等质量的a、b、c三种物质分别配制成饱和溶液,所得溶液质量由大到小的顺序为a>b>c
⑤将t3 ℃时,a、b的饱和溶液分别降温至t1℃,析出晶体的质量a>b
您最近半年使用:0次



