请根据图中甲、乙三种固体的溶解度曲线,回答下列问题:__________________ 。
(2)在t2℃时,向盛有25g甲物质的烧杯中加入50g水,充分溶解后,所得溶液的质量为__ g。
(3)若乙物质中混有少量甲物质,最好采用____ (填“降温结晶”或“蒸发结晶”)的方法提纯乙。
(4)t2℃时,甲、乙两种物质的饱和溶液同时降温至t1℃,所得溶液中溶质质量分数大小关系为___ 。
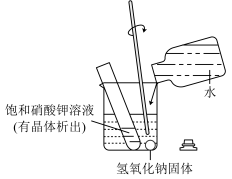
(5)如图中,当向盛有氢氧化钠的烧杯中缓慢倒入水时,试管中观察到的现象是_____ 。

(2)在t2℃时,向盛有25g甲物质的烧杯中加入50g水,充分溶解后,所得溶液的质量为
(3)若乙物质中混有少量甲物质,最好采用
(4)t2℃时,甲、乙两种物质的饱和溶液同时降温至t1℃,所得溶液中溶质质量分数大小关系为
(5)如图中,当向盛有氢氧化钠的烧杯中缓慢倒入水时,试管中观察到的现象是
更新时间:2022-07-07 12:28:11
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】化学与生产、生活息息相关。请用所学知识回答下列问题:
(1)把磨好的豆浆倒在纱布袋中将渣和浆分离,相当于化学实验中的______ 中操作。
(2)新车内放几包活性炭可减少异味,这是利用了活性炭的________ 。
(3)“杂交水稻之父”袁隆平培育出的某种水稻中富含硒,这里的“硒”指的是________ 。
(4)共享单车(自行车)成为人们的代步工具,这种方式践行了低碳理念。“低碳”就是较低的________ (填化学式)排放。
(5)做饭时锅被熏黑,产生这种现象的原因是________ 。
(6)化学兴趣小组在实验室开展“自制简易冰袋”的探究活动,在药品氢氧化钠、硝酸铵、氯化钠固体物质中,用来制作冰袋最佳的固体物质是_______ 。
(1)把磨好的豆浆倒在纱布袋中将渣和浆分离,相当于化学实验中的
(2)新车内放几包活性炭可减少异味,这是利用了活性炭的
(3)“杂交水稻之父”袁隆平培育出的某种水稻中富含硒,这里的“硒”指的是
(4)共享单车(自行车)成为人们的代步工具,这种方式践行了低碳理念。“低碳”就是较低的
(5)做饭时锅被熏黑,产生这种现象的原因是
(6)化学兴趣小组在实验室开展“自制简易冰袋”的探究活动,在药品氢氧化钠、硝酸铵、氯化钠固体物质中,用来制作冰袋最佳的固体物质是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
【推荐2】用化学用语填空:
(1)导电性最好的金属_____ ;
(2)能充入飞艇,又很安全的气体_____
(3)标出NH4ClO4中氯元素的化合价_____
(4)溶解于水后溶液温度会明显下降的物质_____
(5)写出能直接反映出铝的活动性强于铁的化学方程式_____
(1)导电性最好的金属
(2)能充入飞艇,又很安全的气体
(3)标出NH4ClO4中氯元素的化合价
(4)溶解于水后溶液温度会明显下降的物质
(5)写出能直接反映出铝的活动性强于铁的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】溶液的广泛应用极大地服务了人们的生活。某小组以“溶液”为主题开展项目式学习。
【溶液的形成】
(1)分别向水中加入少量下列物质,充分搅拌。其中,不能形成溶液的是______ (填字母序号,后同),溶解过程中温度明显降低的是______ 。
A.氯化钠 B.硝酸铵 C.浓硫酸 D.面粉
【探究溶液浓度的变化】
(2)探究某盐酸敞口放置一段时间后浓度的变化情况,有同学猜想浓度增大,并设计如下方案进行验证。
如图1所示,用胶头滴管向盛有敞口放置后盐酸的试管中滴入足量碳酸钠溶液,观察到U形管内液面的最终变化情况是______ 。其他条件相同时,将敞口放置后的盐酸换为等体积新配制的盐酸,重复上述实验。
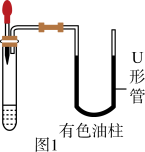
①两次实验最终U形管右侧液面高度的大小关系为______ ,说明猜想成立。
②上述实验中反应的化学方程式为______ ,
【探究溶液的导电性】
(3)查阅文献:a.其他条件相同时,同种离子,离子浓度越大,溶液的导电性越强,电导率越大。
b.碳酸钙与二氧化碳、水反应生成可溶于水的碳酸氢钙[ Ca(HCO3)2]。。
c.Ca(OH)2在水中会解离出Ca2+、OH-;Ca(HCO3)2在水中会解离出Ca2+、 。
。
如图2所示,向盛有饱和Ca(OH)2溶液(用氧化钙新配制)的烧杯中持续通入纯净的CO2,测得实验过程中溶液的电导率如图3所示。
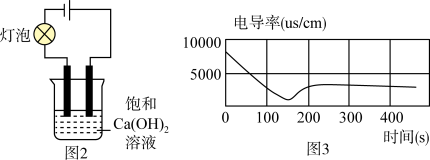
①通入二氧化碳前灯泡发光,通入二氧化碳后可观察到灯泡发光情况为______ 。
②分析最终溶液电导率远低于起始电导率的原因______ 。
【溶液的形成】
(1)分别向水中加入少量下列物质,充分搅拌。其中,不能形成溶液的是
A.氯化钠 B.硝酸铵 C.浓硫酸 D.面粉
【探究溶液浓度的变化】
(2)探究某盐酸敞口放置一段时间后浓度的变化情况,有同学猜想浓度增大,并设计如下方案进行验证。
如图1所示,用胶头滴管向盛有敞口放置后盐酸的试管中滴入足量碳酸钠溶液,观察到U形管内液面的最终变化情况是

①两次实验最终U形管右侧液面高度的大小关系为
②上述实验中反应的化学方程式为
【探究溶液的导电性】
(3)查阅文献:a.其他条件相同时,同种离子,离子浓度越大,溶液的导电性越强,电导率越大。
b.碳酸钙与二氧化碳、水反应生成可溶于水的碳酸氢钙[ Ca(HCO3)2]。。
c.Ca(OH)2在水中会解离出Ca2+、OH-;Ca(HCO3)2在水中会解离出Ca2+、
 。
。如图2所示,向盛有饱和Ca(OH)2溶液(用氧化钙新配制)的烧杯中持续通入纯净的CO2,测得实验过程中溶液的电导率如图3所示。

①通入二氧化碳前灯泡发光,通入二氧化碳后可观察到灯泡发光情况为
②分析最终溶液电导率远低于起始电导率的原因
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】下图甲是A、B、C三种固体物质的溶解度曲线图。

(1)甲图中,t2℃时,A、B、C三种物质中,溶解度最大的是______ 。P点所表示的含义为______ 。
(2)t2℃时,将B物质的不饱和溶液转变成饱和溶液可采取的方法是______ 。(写一种).
(3)要从含A、B、C的混合物中分离出A,最好采用_________ 法。
(4)如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5mL稀盐酸,立即产生大量的气泡,同时烧杯中出现浑浊,则X可能为A、B、C三种固体物质中的哪一种?_______ 。

(1)甲图中,t2℃时,A、B、C三种物质中,溶解度最大的是
(2)t2℃时,将B物质的不饱和溶液转变成饱和溶液可采取的方法是
(3)要从含A、B、C的混合物中分离出A,最好采用
(4)如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5mL稀盐酸,立即产生大量的气泡,同时烧杯中出现浑浊,则X可能为A、B、C三种固体物质中的哪一种?
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】如图是甲、乙、丙三种物质的溶解度曲线。据此回答下列问题:

(1)图中P点的含义是_________ 。
(2)将等质量的甲、乙、丙三种物质,分别配制成t1℃时的饱和溶液,需要水的质量最少的是____ 。
(3)将丙的饱和溶液变为不饱和溶液,在不改变溶液质量的前提下,宜采用的方法是_____ 。
(4)将t2℃时,甲、乙、丙三种物质等质量的饱和溶液降温到t1℃,所得三种溶液的质量由大到小的顺序是______ (用甲、乙、丙表示)。

(1)图中P点的含义是
(2)将等质量的甲、乙、丙三种物质,分别配制成t1℃时的饱和溶液,需要水的质量最少的是
(3)将丙的饱和溶液变为不饱和溶液,在不改变溶液质量的前提下,宜采用的方法是
(4)将t2℃时,甲、乙、丙三种物质等质量的饱和溶液降温到t1℃,所得三种溶液的质量由大到小的顺序是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氯化钾是低钠盐的主要添加剂,从海水晒盐后的苦卤中可以获取氯化钾。
(1)物理方法提取
苦卤的主要成分是氯化镁和氯化钠,其次是硫酸镁和氯化钾。它们的溶解度曲线如图1所示,提取过程如下:

①将苦卤在较高温度下______ (选填“降温结晶”或“蒸发结晶”)析出氯化钠和硫酸镁。
②将①中所得混合物进行______ 操作得到母液。
③将母液降温,氯化钾和氯化镁析出。在较低温度下用水洗涤,即可获得较纯净的氯化钾。
(2)化学方法提纯
工业生产的氯化钾中含有少量硫酸镁杂质,不能满足科研的需要,实验室提纯过程如图2所示:

①提纯过程所用试剂X、Y分别是(写溶质化学式)______ 、______ 。
②写出步骤Ⅱ中发生反应的化学方程式______ 。
③步骤Ⅳ中实际参加反应的离子有______ (写离子符号)。
(1)物理方法提取
苦卤的主要成分是氯化镁和氯化钠,其次是硫酸镁和氯化钾。它们的溶解度曲线如图1所示,提取过程如下:

①将苦卤在较高温度下
②将①中所得混合物进行
③将母液降温,氯化钾和氯化镁析出。在较低温度下用水洗涤,即可获得较纯净的氯化钾。
(2)化学方法提纯
工业生产的氯化钾中含有少量硫酸镁杂质,不能满足科研的需要,实验室提纯过程如图2所示:

①提纯过程所用试剂X、Y分别是(写溶质化学式)
②写出步骤Ⅱ中发生反应的化学方程式
③步骤Ⅳ中实际参加反应的离子有
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】甲、乙、丙三种固体物质的溶解度曲线如图所示。
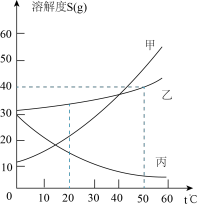
(1)50℃时,乙物质的溶解度是____________ 。
(2)20℃时,使甲物质的饱和溶液变成不饱和溶液,除加水外的另一种方法是____________ 。
(3)50℃时,将甲、乙、丙三种物质的饱和溶液降温至20℃时,溶液溶质质量分数由大到小的顺序是____________ 。
(4)若甲物质中混有少量的乙物质,提纯甲物质可采用的方法是____________ 。

(1)50℃时,乙物质的溶解度是
(2)20℃时,使甲物质的饱和溶液变成不饱和溶液,除加水外的另一种方法是
(3)50℃时,将甲、乙、丙三种物质的饱和溶液降温至20℃时,溶液溶质质量分数由大到小的顺序是
(4)若甲物质中混有少量的乙物质,提纯甲物质可采用的方法是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
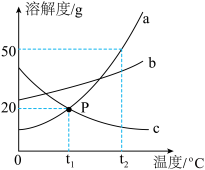
【推荐2】如图是a、b、c三种物质(均不含结晶水)的溶解度曲线,根据右图回答下列问题。______ 。
(2)t2°C时,a、b、c三种物质的溶解度由大到小的顺序是______ 。
(3)t1℃时,将25ga物质加入到100g水中,充分搅拌溶解后恢复到原温度,所得溶液中溶质与溶剂的质量比是______ (最简整数比)。
(4)t2℃时,将a、b、c三种物质的等质量的饱和溶液降温至t1℃,下列说法正确的是______ 。
A都是饱和溶液 B溶质质量分数大小关系是:b>a>c C析出晶体质量最多的是a
(2)t2°C时,a、b、c三种物质的溶解度由大到小的顺序是
(3)t1℃时,将25ga物质加入到100g水中,充分搅拌溶解后恢复到原温度,所得溶液中溶质与溶剂的质量比是
(4)t2℃时,将a、b、c三种物质的等质量的饱和溶液降温至t1℃,下列说法正确的是
A都是饱和溶液 B溶质质量分数大小关系是:b>a>c C析出晶体质量最多的是a
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
【推荐3】甲、乙、丙三种固体物质在水中的溶解度曲线如图所示。请回答:
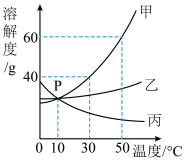
(1)图中P点的意义是____________________________ 。
(2)若甲中混有少量的乙,最好采用_______________ 的方法提纯甲。
(3)使30℃接近饱和的甲溶液变成该温度下的饱和溶液,可采用的一种方法是___ 。
(4)使50℃甲、乙、丙三种物质的饱和溶液降温到10℃,则其溶质质量分数不变的是_________ 。
(5)向100g 50℃的水中加入65g甲固体,发现全部溶解,一段时间后又有部分甲的晶体析出。你认为“全部溶解”的原因可能是__________________________ 。

(1)图中P点的意义是
(2)若甲中混有少量的乙,最好采用
(3)使30℃接近饱和的甲溶液变成该温度下的饱和溶液,可采用的一种方法是
(4)使50℃甲、乙、丙三种物质的饱和溶液降温到10℃,则其溶质质量分数不变的是
(5)向100g 50℃的水中加入65g甲固体,发现全部溶解,一段时间后又有部分甲的晶体析出。你认为“全部溶解”的原因可能是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】下表是氯化钠和硝酸钾在不同温度时的溶解度,根据此表回答:
(1)60℃时,氯化钠的溶解度为________________
(2)在30℃时,100g水中加入50g硝酸钾,充分搅拌后得到的溶液质量为____________
(3)由表中数据分析可知,硝酸钾和氯化钠在某一温度时具有相同的溶解度x,则x的取值范围是_________________
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
(2)在30℃时,100g水中加入50g硝酸钾,充分搅拌后得到的溶液质量为
(3)由表中数据分析可知,硝酸钾和氯化钠在某一温度时具有相同的溶解度x,则x的取值范围是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】t2℃时,将甲,乙各80g分别放到盛有100g水的两个烧杯中,充分溶解后,恢复到t2℃,现象如图一、甲和乙的溶解度曲线如图二、请结合图示回答下列问题:

(1)固体甲对应的溶解度曲线是___________ (填“a”或“b”)。
(2)向烧杯①的溶液中继续加入15g甲物质,充分搅拌,发现固体先全部溶解,一段时间后又有部分固体甲析出。此时(t2℃)溶液的溶质质量分数是___________ (结果精确到0.1%)。你认为“全部溶解”的原因是___________ 。
(3)将t2℃等质量的甲、乙饱和溶液分别降温到t1℃时,所得溶液的有关说法不正确的是___________ (填序号)。
a甲溶液仍为饱和溶液
b两溶液质量:甲<乙
c两溶液中溶剂质量:甲=乙
d两溶液溶质质量分数:甲=乙
e两溶质溶解度:甲>乙

(1)固体甲对应的溶解度曲线是
(2)向烧杯①的溶液中继续加入15g甲物质,充分搅拌,发现固体先全部溶解,一段时间后又有部分固体甲析出。此时(t2℃)溶液的溶质质量分数是
(3)将t2℃等质量的甲、乙饱和溶液分别降温到t1℃时,所得溶液的有关说法不正确的是
a甲溶液仍为饱和溶液
b两溶液质量:甲<乙
c两溶液中溶剂质量:甲=乙
d两溶液溶质质量分数:甲=乙
e两溶质溶解度:甲>乙
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】硫酸镁在工农业及医疗上有广泛的应用,其在一定温度范围内的溶解度如下表所示。
(1)50℃时,硫酸镁饱和溶液中溶质和溶剂的质量比为_______ 。
(2)要配制溶质质量分数最大的硫酸镁饱和溶液,温度要控制在_______ ℃。
(3)90℃时取150.0g硫酸镁溶液,进行如图所示操作(析出的晶体为无水硫酸镁):
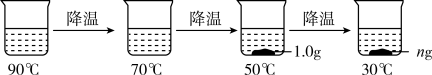
上述90℃的硫酸镁溶液是_______ (填“饱和”或“不饱和”)溶液。图中n的值为_______ 。
| 温度/℃ | 10 | 30 | 50 | 70 | 90 |
| 溶解度/g | 27.7 | 39.3 | 49.0 | 54.1 | 51.1 |
(2)要配制溶质质量分数最大的硫酸镁饱和溶液,温度要控制在
(3)90℃时取150.0g硫酸镁溶液,进行如图所示操作(析出的晶体为无水硫酸镁):

上述90℃的硫酸镁溶液是
您最近一年使用:0次



