溶液与人类生产、生活密切相关。
(1)如图是甲、乙、丙三种固体物质的溶解度曲线。按要求回答问题:
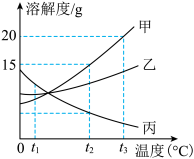
①t3℃时,甲、乙、丙三种物质溶解度由大到小的顺序是______ 。
②t2℃时,将 20g 甲加入 100g 水中,充分溶解,所得溶液的质量为______ g。
③t3℃时,将丙物质的不饱和溶液变成该温度下的饱和溶液,可采用的方法是______ 。
④将 t2℃时三种物质的饱和溶液降温到 t1℃,此时三种溶液的溶质的质量分数由大到小的顺序是______ 。
(2)化学实验中经常用到一定溶质质量分数的溶液。请回答:(水的密度1g/cm)。
若用质量分数为 20%的氯化钠溶液来配制 50g 质量分数为 6%的氯化钠溶液。
①需要 20%的氯化钠溶液______ g
②该溶液配制过程中除用到量筒、烧杯和胶头滴管外,还需要的玻璃仪器是______
(1)如图是甲、乙、丙三种固体物质的溶解度曲线。按要求回答问题:

①t3℃时,甲、乙、丙三种物质溶解度由大到小的顺序是
②t2℃时,将 20g 甲加入 100g 水中,充分溶解,所得溶液的质量为
③t3℃时,将丙物质的不饱和溶液变成该温度下的饱和溶液,可采用的方法是
④将 t2℃时三种物质的饱和溶液降温到 t1℃,此时三种溶液的溶质的质量分数由大到小的顺序是
(2)化学实验中经常用到一定溶质质量分数的溶液。请回答:(水的密度1g/cm)。
若用质量分数为 20%的氯化钠溶液来配制 50g 质量分数为 6%的氯化钠溶液。
①需要 20%的氯化钠溶液
②该溶液配制过程中除用到量筒、烧杯和胶头滴管外,还需要的玻璃仪器是
更新时间:2022-12-31 21:39:43
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】溶液在生产、生活中起着十分重要的作用。请回答下列问题:

(1)如图1是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。
①t1℃时,甲的溶解度为______ g。
②t2℃时,将20g甲加入100g水中,充分搅拌后所得甲溶液是______ (填“饱和”或“不饱和”)的,可以用图中______ (填“a”“b”或“c”)点表示。
③将t1℃的甲、乙、丙饱和溶液升温至t2℃,其溶质的质量分数由大到小顺序为______ 。
(2)不同温度下,氧气的溶解度随压强的变化如图2所示,图中t1对应的温度为40℃,则t2对应的温度______ (填字母编号)。
A.大于40℃ B.小于40℃ C.无法确定

(1)如图1是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。
①t1℃时,甲的溶解度为
②t2℃时,将20g甲加入100g水中,充分搅拌后所得甲溶液是
③将t1℃的甲、乙、丙饱和溶液升温至t2℃,其溶质的质量分数由大到小顺序为
(2)不同温度下,氧气的溶解度随压强的变化如图2所示,图中t1对应的温度为40℃,则t2对应的温度
A.大于40℃ B.小于40℃ C.无法确定
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐2】溶液在生产、生活中起着十分重要的作用。请回答下列问题。
(1)可以作为溶质的是_____ (填字母序号)。
A 只有固体 B 只有液体
C 只有气体 D 气体、液体、固体都可以
(2)配制 100 g质量分数为 16%的氯化钠溶液,所需水的体积为_____ mL(水的密度 为 1 g/cm3)。
(3)如图所示为 X、Y、Z 三种固体物质(不含结晶水)的溶解度曲线,请回答下列问题:

①t2℃时,三种物质的溶解度的大小关系是_____ 。
②t3℃时,在 100gX 的饱和溶液中加入 10g 水,为使溶液 重新达到饱和,需加入 X 固体_____ g。
③t3℃时,将 80gX 的饱和溶液降温到 t1℃,析出晶体质量是_____ g。
(1)可以作为溶质的是
A 只有固体 B 只有液体
C 只有气体 D 气体、液体、固体都可以
(2)配制 100 g质量分数为 16%的氯化钠溶液,所需水的体积为
(3)如图所示为 X、Y、Z 三种固体物质(不含结晶水)的溶解度曲线,请回答下列问题:

①t2℃时,三种物质的溶解度的大小关系是
②t3℃时,在 100gX 的饱和溶液中加入 10g 水,为使溶液 重新达到饱和,需加入 X 固体
③t3℃时,将 80gX 的饱和溶液降温到 t1℃,析出晶体质量是
您最近一年使用:0次
【推荐3】硝酸钾在不同温度时的溶解度见下表:
(1)下图A、B、C、D四个烧杯中分别盛有100g水,分别向其中加入110g、 86g、 64g、32g硝酸钾,充分溶解后得到40℃时的溶液。
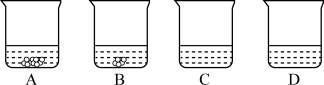
①______ 中的液体是饱和溶液(选填字母),D烧杯中溶液的溶质质量分数为______ 。
②将一瓶接近饱和的硝酸钾溶液变成饱和溶液的方法是______ (任写一种)。
③40℃时,向B烧杯中加适量的水得到的饱和溶液最大质量为______ g(精确到0.1)。
(2)硝酸钾和氯化铵的溶解度曲线如图1所示,某化学兴趣小组同学进行了如图2所示实验。

①t1℃时,氯化铵的溶解度为______ g。
②t2℃时,硝酸钾和氯化铵的溶解度大小关系是______ 。
③t2℃时,将80gKNO3加入到l00g水中,充分搅拌溶解后恢复到原温度,所得溶液中溶质与溶剂的质量比是______ 。
④下列关于图2中烧杯内物质的说法正确的是______ (填字母)。
A.烧杯Ⅱ中溶液的质量是160g
B.烧杯Ⅰ、Ⅱ、Ⅲ中,只有Ⅱ中上层清液是饱和溶液
C.若使烧杯Ⅲ中的固体溶解,可采用加水或升温的方法
D.烧杯Ⅲ的上层清液中溶质质量分数一定比Ⅰ的溶液中溶质质量分数大
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| 溶解度/g | 21 | 32 | 46 | 64 | 86 | 110 | 138 |
(1)下图A、B、C、D四个烧杯中分别盛有100g水,分别向其中加入110g、 86g、 64g、32g硝酸钾,充分溶解后得到40℃时的溶液。

①
②将一瓶接近饱和的硝酸钾溶液变成饱和溶液的方法是
③40℃时,向B烧杯中加适量的水得到的饱和溶液最大质量为
(2)硝酸钾和氯化铵的溶解度曲线如图1所示,某化学兴趣小组同学进行了如图2所示实验。

①t1℃时,氯化铵的溶解度为
②t2℃时,硝酸钾和氯化铵的溶解度大小关系是
③t2℃时,将80gKNO3加入到l00g水中,充分搅拌溶解后恢复到原温度,所得溶液中溶质与溶剂的质量比是
④下列关于图2中烧杯内物质的说法正确的是
A.烧杯Ⅱ中溶液的质量是160g
B.烧杯Ⅰ、Ⅱ、Ⅲ中,只有Ⅱ中上层清液是饱和溶液
C.若使烧杯Ⅲ中的固体溶解,可采用加水或升温的方法
D.烧杯Ⅲ的上层清液中溶质质量分数一定比Ⅰ的溶液中溶质质量分数大
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐1】如图为NH4Cl、NaCl、NaHCO3三种物质的溶解度曲线。

(1)60℃时,氯化铵的溶解度是______ 。
(2)60℃时,从含有少量氯化钠的氯化铵溶液中得到氯化铵晶体的操作:加热浓缩、______ 、过滤、洗涤、干燥。
(3)将60℃时氯化铵和氯化钠的饱和溶液各100g分别蒸发掉10g水,然后降温至t℃,过滤,得到溶液甲和溶液乙,则溶液中溶质的质量关系:甲______ 乙(填“>”或“<”或“=”)。
(4)下列说法正确的是______。

(1)60℃时,氯化铵的溶解度是
(2)60℃时,从含有少量氯化钠的氯化铵溶液中得到氯化铵晶体的操作:加热浓缩、
(3)将60℃时氯化铵和氯化钠的饱和溶液各100g分别蒸发掉10g水,然后降温至t℃,过滤,得到溶液甲和溶液乙,则溶液中溶质的质量关系:甲
(4)下列说法正确的是______。
| A.碳酸氢钠的溶解度最小 |
| B.t℃时,氯化铵溶液和氯化钠溶液的溶质质量分数不一定相等 |
| C.60℃时,三种物质的饱和溶液的质量关系是:氯化铵>氯化钠>碳酸氢钠 |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】如图所示,是A、B、C三种固体物质的溶解度曲线,请据图回答下列问题:
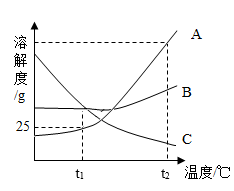
(1)t1℃时,A物质饱和溶液的溶质质量分数为___________ 。
(2)t2℃时,A 、B、C三种物质的溶解度最大的是___________ 。
(3)要从B物质的饱和溶液中得到B物质的晶体,一般采用___________ 的方法,这是因为___________ 。
(4)将t1℃时C物质的不饱和溶液,可以通过减少溶剂、增加溶质或___________ ,可使其变为饱和溶液。
(5)从t2℃降低到t1℃时,等质量的A 、B、C三种物质的饱和溶液,析出晶体最多的是___________ 物质。

(1)t1℃时,A物质饱和溶液的溶质质量分数为
(2)t2℃时,A 、B、C三种物质的溶解度最大的是
(3)要从B物质的饱和溶液中得到B物质的晶体,一般采用
(4)将t1℃时C物质的不饱和溶液,可以通过减少溶剂、增加溶质或
(5)从t2℃降低到t1℃时,等质量的A 、B、C三种物质的饱和溶液,析出晶体最多的是
您最近一年使用:0次
【推荐3】硝酸钾在不同温度下的溶解度如下表所示,据此画出不同温度下硝酸钾在溶解时恰好达到饱和状态时溶质质量与溶剂质量的关系。
(1)图像中,t2℃对应的温度是______________ ℃。
(2)80℃时,将80g硝酸钾放入50g水中,得到的溶液为该温度下硝酸钾的_____________ (填“饱和”或“不饱和”)溶液。
(3)若要使B点对应的溶液转化到C点对应的溶液,应加入硝酸钾的质量为______________ g。
(4)A、B、C三点对应的溶液,溶质质量分数的大小关系为______________ 。

| 温度/℃ | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 31.6 | 63.9 | 110 | 169 | 240 |
(2)80℃时,将80g硝酸钾放入50g水中,得到的溶液为该温度下硝酸钾的
(3)若要使B点对应的溶液转化到C点对应的溶液,应加入硝酸钾的质量为
(4)A、B、C三点对应的溶液,溶质质量分数的大小关系为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】水和溶液在生产,生活中具有广泛的用途。
(1)下列物质属于溶液的是 (填字母)。
(2)在实验室配制100g质量分数为8%的氢氧化钠溶液。
①计算:需要氢氧化钠固体的质量为_____ g,水的体积为_____ ml(水的密度近似看作1g/cm3)。
②称量:调节托盘天平平衡,将一个烧杯放在托盘天平的左盘,称量其质量,然后_____ (按操作的先后顺序选填字母),直至天平平衡。
A.将氢氧化钠固体加入烧杯中
B.按需要添加砝码、移动游码
该步骤中不把氢氧化钠放在纸上称量的原因是_____ 。
③量取:用量筒量取所需的水。
④溶解:将量取的水,倒入盛有氢氧化钠固体的烧杯里搅拌,使其溶解,并冷却至室温。
⑤把配好的溶液装入试剂瓶,塞好橡皮塞并贴上标签。
(3)以下操作会导致所得氢氧化钠溶液的溶质质量分数偏小的是 (填字母)。
(4)甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示。_____ 溶液(填“饱和”或“不饱和”)。
②t2℃时,将等质量的甲、乙两种物质饱和溶液降温至t1℃,下列说法正确的是_____ (填字母)。
A.得到的都是饱和溶液
B.所得溶液的溶质质量分数大小关系是:甲 > 乙
C.析出晶体质量多的是甲
D.所得甲、乙两种物质的溶液质量相等
(5)某工厂利用废铁屑与废硫酸反应制取硫酸亚铁。现有废硫酸9.8t(硫酸的质量分数为20%)与足量的废铁屑反应,可生产FeSO4的质量是多少?
(1)下列物质属于溶液的是 (填字母)。
| A.医用酒精 | B.碘酒 | C.碳酸饮料 | D.泥浆水 |
(2)在实验室配制100g质量分数为8%的氢氧化钠溶液。
①计算:需要氢氧化钠固体的质量为
②称量:调节托盘天平平衡,将一个烧杯放在托盘天平的左盘,称量其质量,然后
A.将氢氧化钠固体加入烧杯中
B.按需要添加砝码、移动游码
该步骤中不把氢氧化钠放在纸上称量的原因是
③量取:用量筒量取所需的水。
④溶解:将量取的水,倒入盛有氢氧化钠固体的烧杯里搅拌,使其溶解,并冷却至室温。
⑤把配好的溶液装入试剂瓶,塞好橡皮塞并贴上标签。
(3)以下操作会导致所得氢氧化钠溶液的溶质质量分数偏小的是 (填字母)。
| A.用托盘天平称量氢氧化钠,敞口放置一段时间后,加水溶解 |
| B.用量筒量取水时仰视读数,并将水全部倒入上述烧杯中 |
| C.将配制好的氢氧化钠溶液装入试剂瓶中时,有部分溶液洒出 |
| D.盛装配制好的氢氧化钠溶液的试剂瓶没有干燥,残留少量蒸馏水 |
(4)甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示。

②t2℃时,将等质量的甲、乙两种物质饱和溶液降温至t1℃,下列说法正确的是
A.得到的都是饱和溶液
B.所得溶液的溶质质量分数大小关系是:甲 > 乙
C.析出晶体质量多的是甲
D.所得甲、乙两种物质的溶液质量相等
(5)某工厂利用废铁屑与废硫酸反应制取硫酸亚铁。现有废硫酸9.8t(硫酸的质量分数为20%)与足量的废铁屑反应,可生产FeSO4的质量是多少?
您最近一年使用:0次
【推荐2】在t℃时,分别取甲、乙两固体物质的溶液,恒温蒸发水分,得到析出晶体质量与蒸发水的质量的关系如图所示(析出晶体不含结晶水)。

(1)蒸发水之前,甲形成的溶液是______ 溶液(填“饱和”或“不饱和”)。
(2)t℃时,甲、乙的溶解度大小关系为:甲______ 乙(填“<”、“>”或“=”)。
(3)P点时,乙溶液的溶质质量分数是______ 。
(4)下列说法不正确的是______(填字母)。
(5)工业上电解饱和食盐水制得NaOH、H2和Cl2,写出该反应的化学方程式______ ,该反应中Cl元素的化合价由______ 价变为0价。
(6)侯氏制碱的原理为:NaCl+H2O+NH3+CO2=NaHCO3↓+NH4Cl;2NaHCO3 Na2CO3+CO2↑+H2O。结合如图回答下列问题:
Na2CO3+CO2↑+H2O。结合如图回答下列问题:

①NH4Cl溶液中混有少量NaCl,可用______ 方法提纯NH4Cl。
②60℃后,NaHCO3的溶解度无数据的原因可能是______ 。
(7)如图是配制50g质量分数为10%的氯化钠溶液的操作过程示意图,试回答:

①请指出图中两个明显的错误处,请填写错误操作序号______ 。
②若将错误更正后,进行实验,应称量氯化钠的质量是______ g;如果向托盘上加氯化钠时,指针偏向分度盘的右边,应进行的操作是______ 。
③量取水时,应选用______ 的量筒(从10mL,100mL中选择);量水读数时,量筒必须平放,视线要跟量筒内______ 处保持水平。
④若将错误更正后重新配制溶液,测得溶液中溶质质量分数小于10%。请你分析可能的原因有______ (填字母)。
A.用量筒量取水时俯视读数
B.配制溶液的烧杯用少量蒸馏水润洗
C.氯化钠晶体不纯
D.盛装溶液的试剂瓶用蒸馏水润洗
E.C操作中发现一部分氯化钠撒在烧杯外边
⑤若用溶质质量分数为20%NaCl溶液配制上述溶液,应取20%NaCl溶液______ g。

(1)蒸发水之前,甲形成的溶液是
(2)t℃时,甲、乙的溶解度大小关系为:甲
(3)P点时,乙溶液的溶质质量分数是
(4)下列说法不正确的是______(填字母)。
| A.甲中含有少量乙时,可用降温结晶的方法提纯乙 |
| B.t℃时,等质量的甲、乙饱和溶液,降温到相同温度,析出甲的质量小于乙 |
| C.用固体乙配制50g 6%的乙溶液,主要实验步骤是:计算、称量、混匀 |
| D.P点表示t℃时甲和乙的溶解度相等 |
(6)侯氏制碱的原理为:NaCl+H2O+NH3+CO2=NaHCO3↓+NH4Cl;2NaHCO3
 Na2CO3+CO2↑+H2O。结合如图回答下列问题:
Na2CO3+CO2↑+H2O。结合如图回答下列问题:
①NH4Cl溶液中混有少量NaCl,可用
②60℃后,NaHCO3的溶解度无数据的原因可能是
(7)如图是配制50g质量分数为10%的氯化钠溶液的操作过程示意图,试回答:

①请指出图中两个明显的错误处,请填写错误操作序号
②若将错误更正后,进行实验,应称量氯化钠的质量是
③量取水时,应选用
④若将错误更正后重新配制溶液,测得溶液中溶质质量分数小于10%。请你分析可能的原因有
A.用量筒量取水时俯视读数
B.配制溶液的烧杯用少量蒸馏水润洗
C.氯化钠晶体不纯
D.盛装溶液的试剂瓶用蒸馏水润洗
E.C操作中发现一部分氯化钠撒在烧杯外边
⑤若用溶质质量分数为20%NaCl溶液配制上述溶液,应取20%NaCl溶液
您最近一年使用:0次
【推荐3】为测定某含杂质3.5%的锌铜粉末(杂质不溶于水且不参加反应)中锌的纯度,进行右图实验:

(1)上述实验中发生反应的化学方程式为___________ ;
(2)求解样品中参加反应的物质质量(x)的比例式为______________ ;
(3)配制实验中所用的硫酸铜溶液,需要16%的硫酸铜溶液的质量为___________ ;
(4)该粉末样品中锌的质量分数为______________ ;
(5)由C→D需蒸发水的体积为__________________ mL;
(6)冶炼398t与上述B中固体纯度相同的铜,需要含杂质的赤铜(Cu2O)的质量为___________ 。

(1)上述实验中发生反应的化学方程式为
(2)求解样品中参加反应的物质质量(x)的比例式为
(3)配制实验中所用的硫酸铜溶液,需要16%的硫酸铜溶液的质量为
(4)该粉末样品中锌的质量分数为
(5)由C→D需蒸发水的体积为
(6)冶炼398t与上述B中固体纯度相同的铜,需要含杂质的赤铜(Cu2O)的质量为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐1】为测定某工厂废铁屑(杂质不溶于水不与酸反应且不含铁元素)中铁的含量,某化学兴趣小组,进行如下实验:

(1)上述实验过程中发生反应的化学方程式为___________ 。
(2)根据已知条件列出求解参加反应铁质量(x)的比例式___________ 。
(3)用36.5%的浓盐酸配制上述实验稀盐酸,需要浓盐酸的质量为___________ 。
(4)废铁屑中铁的含量为___________ 。
(5)若要使滤液质量分数变为12.7%,需蒸发水的质量___________ 。

(1)上述实验过程中发生反应的化学方程式为
(2)根据已知条件列出求解参加反应铁质量(x)的比例式
(3)用36.5%的浓盐酸配制上述实验稀盐酸,需要浓盐酸的质量为
(4)废铁屑中铁的含量为
(5)若要使滤液质量分数变为12.7%,需蒸发水的质量
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】硝酸钾、氯化钾的溶解度曲线如图甲所示,回答下列问题:

(1)t1℃时KNO3的溶解度___________ KCl溶解度(填“>”“<”或“=”)。
(2)t3℃时,将60gKCl放入___________ g水中,完全溶解后,可得到恰好饱和的溶液。
(3)如图乙是有关硝酸钾溶液的实验操作及变化情况,下列说法正确的是___________。
(4)用40%的硝酸钾溶液配制l00g10%的硝酸钾溶液,需要加入水的体积是___________ 。

(1)t1℃时KNO3的溶解度
(2)t3℃时,将60gKCl放入
(3)如图乙是有关硝酸钾溶液的实验操作及变化情况,下列说法正确的是___________。
| A.①与②的溶质质量可能相等 |
| B.②与③的溶质质量分数一定相等 |
| C.若将等温度等质量的硝酸钾和氯化钾饱和溶液,恒温蒸发等质量的水,析出的晶体质量:硝酸钾>氯化钾 |
| D.若将等温度等质量的硝酸钾和氯化钾的饱和溶液,降低相同的温度,析出的晶体的质量:硝酸钾>氯化钾 |
(4)用40%的硝酸钾溶液配制l00g10%的硝酸钾溶液,需要加入水的体积是
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐3】某化学兴趣小组的同学在老师的指导下,进行如下实验活动。
I.用98%的浓硫酸(p=1.84g/cm3)配制100g10%的硫酸,所需浓硫酸的体积为___ mL(计算结果精确到0.1);量取浓硫酸时,若仰视读数(其他操作均正确),则所配硫酸的质量分数__ 10%(填“>”“<”或“=”)。
Ⅱ.有一包固体粉末,可能含有硝酸钾、氯化钠、碳酸钠、硫酸钠、硫酸铜中的一种或几种为探究该固体粉末的组成,小组同学取50g样品按如下流程进行实验:

根据上述实验现象及数据,回答下列问题:
(1)由上述实验现象及数据分析,原固体粉末中一定不含有__ (填化学式),一定含有___ (填化学式)。
(2)滤液D中共含有___ (填数字)种溶质。
(3)原固体粉末中含量最少的物质的质量为___ g。
I.用98%的浓硫酸(p=1.84g/cm3)配制100g10%的硫酸,所需浓硫酸的体积为
Ⅱ.有一包固体粉末,可能含有硝酸钾、氯化钠、碳酸钠、硫酸钠、硫酸铜中的一种或几种为探究该固体粉末的组成,小组同学取50g样品按如下流程进行实验:

根据上述实验现象及数据,回答下列问题:
(1)由上述实验现象及数据分析,原固体粉末中一定不含有
(2)滤液D中共含有
(3)原固体粉末中含量最少的物质的质量为
您最近一年使用:0次



