阅读下面科普短文。
中国是世界上最早发现和利用茶树的国家。
茶树适宜生长在pH为4.5~6.5的土壤中。茶叶有效成分主要含有的三类物质分别为茶多酚、氨基酸、咖啡碱。咖啡碱(化学式为C8H10N4O2)能使人体中枢神经产生兴奋,喝茶能提神解乏。茶多酚是茶叶所含多酚类物质的总称,是形成茶叶色香味的主要成分,也是茶叶中有保健功能的主要成分。

泡茶前一般要洗茶,可以唤醒茶叶的活性,冲泡时香气可以得到最大程度的散发,口感更加醇厚,另外茶叶在加工、储存过程中会有浮尘附着,洗茶,喝着更放心。
泡茶时水的温度不同,影响着茶水中茶多酚的浓度。温度过高,茶所具有的有益物质遭受破坏,温度过低,不能使茶叶中的有效成分充分浸出,其滋味淡薄。而且,不同种类的茶需要不同温度的水冲泡,才能达到茶的最佳保健效果。
以龙井茶(绿茶)为例进行研究,如图2为水温及浸泡时间对茶多酚溶解率的影响。

除了控制水温和浸泡时间外,多次浸泡也可提高茶多酚的溶解率。
(1)茶树适宜生长在_________ (填“酸性”“碱性”或“中性”)土壤。
(2)结合题中图1,把茶叶和茶水分离的操作是_________ 。
(3)咖啡碱中含有_________ 种元素。
(4)下列说法正确的是 (填序号)。
(5)保存茶叶时需要注意防潮,茶叶包装中常放入一小袋干燥剂,其成分为生石灰,写出生石灰与水反应的化学方程式__________ 。
中国是世界上最早发现和利用茶树的国家。
茶树适宜生长在pH为4.5~6.5的土壤中。茶叶有效成分主要含有的三类物质分别为茶多酚、氨基酸、咖啡碱。咖啡碱(化学式为C8H10N4O2)能使人体中枢神经产生兴奋,喝茶能提神解乏。茶多酚是茶叶所含多酚类物质的总称,是形成茶叶色香味的主要成分,也是茶叶中有保健功能的主要成分。

泡茶前一般要洗茶,可以唤醒茶叶的活性,冲泡时香气可以得到最大程度的散发,口感更加醇厚,另外茶叶在加工、储存过程中会有浮尘附着,洗茶,喝着更放心。
泡茶时水的温度不同,影响着茶水中茶多酚的浓度。温度过高,茶所具有的有益物质遭受破坏,温度过低,不能使茶叶中的有效成分充分浸出,其滋味淡薄。而且,不同种类的茶需要不同温度的水冲泡,才能达到茶的最佳保健效果。
以龙井茶(绿茶)为例进行研究,如图2为水温及浸泡时间对茶多酚溶解率的影响。

除了控制水温和浸泡时间外,多次浸泡也可提高茶多酚的溶解率。
(1)茶树适宜生长在
(2)结合题中图1,把茶叶和茶水分离的操作是
(3)咖啡碱中含有
(4)下列说法正确的是 (填序号)。
| A.结合图2为减少茶多酚流失,洗龙井茶时水的温度适宜在50℃左右 |
| B.冲泡龙井茶时,水温、浸泡时间影响茶多酚的溶解率大小 |
| C.生活中,各种茶都要用100℃的水冲泡 |
2023·北京·一模 查看更多[1]
更新时间:2023-04-29 00:19:10
|
相似题推荐
综合应用题
|
适中
(0.65)
【推荐1】无土栽培是一种农业高新技术,它可以显著提高农作物的产量和质量。现有西红柿无土栽培营养液中,含硝酸钾(KNO3)的溶质质量分数为5%,请填空:
(1)硝酸钾由_____ 种元素组成,其中氮、氧两种元素质量比为(最简整数比) _____ ;
(2)某同学练习配制该无土栽培营养液80g,需KNO3_______ g.
下图是该同学配制的实验操作示意图:

(3)量取所需要的水应选择____ (选填“10mL”“50mL”或“100mL”)量筒.用上述图示的序号表示配制溶液的操作顺序: ____ ;
(4)要使该溶液的质量分数增大一倍,可以采用增加溶质和____ 等方法。请你选取其中一种方法通过计算说明(要有解题过程和必要的文字说明;所选方法如有小数,请保留小数点后两位数)
(1)硝酸钾由
(2)某同学练习配制该无土栽培营养液80g,需KNO3
下图是该同学配制的实验操作示意图:

(3)量取所需要的水应选择
(4)要使该溶液的质量分数增大一倍,可以采用增加溶质和
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】阅读科普短文,回答相关问题。
二氧化碳的综合开发利用越来越受到人们的关注。
甲醇(CH3OH)是一种基础有机化工原料,广泛应用于有机合成、医药、农药、染料、高分子等化工生产领域,其消费量在有机原料中仅次于乙烯、丙烯和苯,位居第四位。甲醇将成为21世纪具有竞争力的清洁燃料之一、可以单独或与汽油混合作为汽车燃料。目前,我国则是以煤和重渣油为主要原料,这些原料都日渐减少,人们正在积极寻找新的碳源来合成甲醇。如果用含二氧化碳的工业废气为碳源合成甲醇,既可为减少二氧化碳的排放提供一种好的解决方法,又可为甲醇的合成提供一条绿色合成的新途径,是十分有意义的。

(1)下列有关甲醇(CH3OH)的说法正确的是_____。
(2)二氧化碳在常温下可加压转化成超临界二氧化碳流体,此变化属于_____ 变化,转化过程中_____ (“释放”或“吸收”)放出热量。
(3)工业生产甲醇,选用H2与CO2体积比为_____ ,工业选用温度为320℃的原因:_____ 。
二氧化碳的综合开发利用越来越受到人们的关注。
甲醇(CH3OH)是一种基础有机化工原料,广泛应用于有机合成、医药、农药、染料、高分子等化工生产领域,其消费量在有机原料中仅次于乙烯、丙烯和苯,位居第四位。甲醇将成为21世纪具有竞争力的清洁燃料之一、可以单独或与汽油混合作为汽车燃料。目前,我国则是以煤和重渣油为主要原料,这些原料都日渐减少,人们正在积极寻找新的碳源来合成甲醇。如果用含二氧化碳的工业废气为碳源合成甲醇,既可为减少二氧化碳的排放提供一种好的解决方法,又可为甲醇的合成提供一条绿色合成的新途径,是十分有意义的。

(1)下列有关甲醇(CH3OH)的说法正确的是_____。
| A.由1个碳原子、4个氢原子、1个氧原子构成 |
| B.甲醇完全燃烧只生成二氧化碳和水,并放出能量 |
| C.二氧化碳与氢气在催化下,通过化合反应可生成甲醇 |
| D.甲醇属于有机高分子化合物 |
| E.甲醇中氢元素质量分数最大 |
(3)工业生产甲醇,选用H2与CO2体积比为
您最近一年使用:0次
【推荐3】实验室制取气体常用到下列装置,根据给出的装置回答下列问题:

(1)写出图中a仪器的名称:______ 。
(2)实验室用A装置制取氧气的文字表达式为______ ,若收集一瓶纯净的氧气作为铁丝燃烧的实验,应选择装置______ 收集,理由是______ 。
(3)某同学利用C装置收集氧气时,发现收集的氧气不纯,请分析原因:_______ 。(写出一条即可)
(4)若用如图2装置采用排空气法收集氧气,请在图中补画完整______ 。
(5)人体缺乏维生素C(简写成Vc)易患坏血病,如图是某品牌Vc片说明书的一部分(只写计算结果)。
①Vc分子中碳、氢、氧原子个数比______ 。
②Vc中碳和氢元素的质量比______ 。
③Vc的相对分子质量为______ 。
④若成人每天对Vc的最低需要量为60mg,每天服用该品牌维生素C片______ 次。

(1)写出图中a仪器的名称:
(2)实验室用A装置制取氧气的文字表达式为
(3)某同学利用C装置收集氧气时,发现收集的氧气不纯,请分析原因:
(4)若用如图2装置采用排空气法收集氧气,请在图中补画完整
(5)人体缺乏维生素C(简写成Vc)易患坏血病,如图是某品牌Vc片说明书的一部分(只写计算结果)。
| 维生素C(白色) 化学式:  每片100mg,含Vc10% 一日**次,每次2片 |
②Vc中碳和氢元素的质量比
③Vc的相对分子质量为
④若成人每天对Vc的最低需要量为60mg,每天服用该品牌维生素C片
您最近一年使用:0次
【推荐1】我国的北斗卫星导航系统标志是北斗星和司南的结合。
(1)我国“长三乙”火箭将第55颗北斗卫星送入预定轨道,完成了北斗卫星导航系统的组网。该火箭的推进剂是液氢和液氧,二者发生的反应属于______ 反应(填基本反应类型)。
(2)“司南之杓,投之于地,其柢指南”中“杓”的主要成分是Fe3O4,其中铁元素的质量分数为______ (结果精确到0.1%)。
(3)如图“北斗七星”代表7种初中化学常见的物质,“—”表示相邻的物质间能发生反应,“→”表示能一步实现的物质转化方向。已知A、C的元素组成相同且常温下均为液体,D可作食品干燥剂,F是农业生产中常用的气体肥料。

①写出A的名称:______ 。
②B在空气中的体积分数约为______ 。“铁丝在氧气中燃烧实验”中C的作用是_____________ 。
③写出D→E的化学方程式:_________________ 。
④写出F的另一种用途:___________ 。若G能与血红蛋白结合导致人体中毒,则其化学式为______ 。
(1)我国“长三乙”火箭将第55颗北斗卫星送入预定轨道,完成了北斗卫星导航系统的组网。该火箭的推进剂是液氢和液氧,二者发生的反应属于
(2)“司南之杓,投之于地,其柢指南”中“杓”的主要成分是Fe3O4,其中铁元素的质量分数为
(3)如图“北斗七星”代表7种初中化学常见的物质,“—”表示相邻的物质间能发生反应,“→”表示能一步实现的物质转化方向。已知A、C的元素组成相同且常温下均为液体,D可作食品干燥剂,F是农业生产中常用的气体肥料。

①写出A的名称:
②B在空气中的体积分数约为
③写出D→E的化学方程式:
④写出F的另一种用途:
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】流程与推断。
(1)工业上,常将煤气化,煤气化示意图如下。回答下列问题。
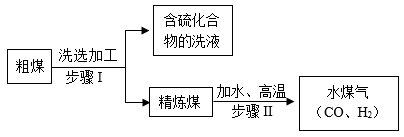
①煤属于_____ (填“混合物”或“纯净物”)。
②步骤Ⅰ分离操作的名称是_____ 。
③该工艺没有直接把粗煤作为燃料,而经过系列加工转化为生产生活中的重要燃料水煤气,主要原因是_____ (一点即可)。
(2)A、B、C、D、E是初中化学常见的物质,A是石灰石的主要成分,E是能与血红蛋白结合的有毒气体,如图表示它们的转化关系。回答下列问题。
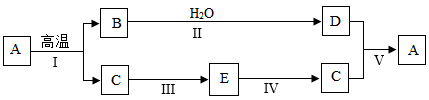
①反应Ⅰ用于工业制取二氧化碳,化学反应方程式为_____ 。
②属于放热反应的是_____ (填写“Ⅱ”或“Ⅲ”或“Ⅱ和Ⅲ”)
③E物质虽然有毒,但也是重要的化工原料,填写E物质的一种用途_____ 。
④反应Ⅴ的化学反应方程式为_____ 。
(1)工业上,常将煤气化,煤气化示意图如下。回答下列问题。

①煤属于
②步骤Ⅰ分离操作的名称是
③该工艺没有直接把粗煤作为燃料,而经过系列加工转化为生产生活中的重要燃料水煤气,主要原因是
(2)A、B、C、D、E是初中化学常见的物质,A是石灰石的主要成分,E是能与血红蛋白结合的有毒气体,如图表示它们的转化关系。回答下列问题。

①反应Ⅰ用于工业制取二氧化碳,化学反应方程式为
②属于放热反应的是
③E物质虽然有毒,但也是重要的化工原料,填写E物质的一种用途
④反应Ⅴ的化学反应方程式为
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐3】《石灰吟》是明代文学家于谦创作的一首七言绝句,全诗内容如下:“千锤万凿出深山,烈火焚烧若等闲。粉骨碎身浑不怕,要留清白在人间。”全诗所涉及的化学反应用流程图表示如下:

(1)过程①所发生的反应属于_______ 反应(填“化合”“分解”“置换”“复分解”之一)。
(2)写出过程③的化学方程式________________ 。
(3)上述过程所涉及的物质中经常用作干燥剂的是________ (填化学式)。
(4)为制取氢氧化钠,取一定质量的步骤②所得石灰乳,向其中滴入质量分数为10.6%的Na2CO3溶液,使其充分反应。加入Na2CO3溶液的质量和所得沉淀的质量关系如下图所示:

①当滴入10.6%的碳酸钠溶液至图中B点时,溶液中的溶质有______________ (填化学式)。
②计算恰好完全反应(至图中A点)时所得氢氧化钠的质量。(计算结果精确至0.1 g)____

(1)过程①所发生的反应属于
(2)写出过程③的化学方程式
(3)上述过程所涉及的物质中经常用作干燥剂的是
(4)为制取氢氧化钠,取一定质量的步骤②所得石灰乳,向其中滴入质量分数为10.6%的Na2CO3溶液,使其充分反应。加入Na2CO3溶液的质量和所得沉淀的质量关系如下图所示:

①当滴入10.6%的碳酸钠溶液至图中B点时,溶液中的溶质有
②计算恰好完全反应(至图中A点)时所得氢氧化钠的质量。(计算结果精确至0.1 g)
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
解题方法
【推荐1】中和反应是一类重要的化学反应。某同学利用图1装置探究相同浓度的稀盐酸与氢氧化钠溶液反应的过程,并用pH计和温度传感器测量反应过程中相关量的变化情况,得到图2和图3。
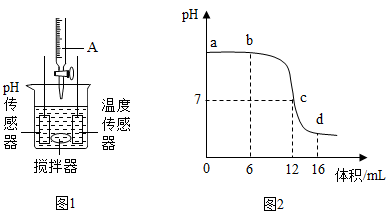

(1)烧杯中发生反应的化学方程式为______ 。
(2)图2中c点所示溶液的溶质是______ ;由图2可知,图1中向烧杯里滴加的是______ (填名称):小雨同学发现随着反应的进行,溶液pH在逐渐减小,于是得出结论:酸和碱能发生反应。你认为需测得溶液的pH______ 7(填“<”或“≤”)时才能证明酸和碱能发生反应。
(3)图3中V的数值最接近图2中的体积数值是______ (填“6”、“12”或“16”):
(4)通过图3可知,中和反应是______ 反应(填“放热”或“吸热”)。
(5)实验结束后,同学们对烧杯中反应后的溶质成分产生兴趣,并对其成分进行猜想:
【猜想与假设】猜想一:NaCl:
猜想二:NaCl、NaOH
猜想三:______ 。
猜想四:NaCl、HCl、NaOH
小王同学认为猜想四肯定不合理,理由是______ ;
【实验与验证】
【评价与反思】
I、小彤同学认为向步骤Ⅱ的试管中加入其它试剂也能得出相同的结论,下列试剂可以选用的是______ 。
A.无色酚酞试液 B.锌粒 C.硝酸银溶液 D.紫色石蕊试液
Ⅱ、小丽同学总结出在对反应后所得溶液的溶质成分进行猜想时,除了考虑生成物外还要考虑______ 。


(1)烧杯中发生反应的化学方程式为
(2)图2中c点所示溶液的溶质是
(3)图3中V的数值最接近图2中的体积数值是
(4)通过图3可知,中和反应是
(5)实验结束后,同学们对烧杯中反应后的溶质成分产生兴趣,并对其成分进行猜想:
【猜想与假设】猜想一:NaCl:
猜想二:NaCl、NaOH
猜想三:
猜想四:NaCl、HCl、NaOH
小王同学认为猜想四肯定不合理,理由是
【实验与验证】
| 步骤 | 现象 | 结论 |
| 步骤I:取烧杯中的溶液少许于试管中,滴入硫酸铜溶液 | 猜想二不成立 | |
| 步骤Ⅱ:另取烧杯中的溶液少许于试管中,滴入碳酸钠溶液 | 有气泡产生 | 猜想三成立 |
I、小彤同学认为向步骤Ⅱ的试管中加入其它试剂也能得出相同的结论,下列试剂可以选用的是
A.无色酚酞试液 B.锌粒 C.硝酸银溶液 D.紫色石蕊试液
Ⅱ、小丽同学总结出在对反应后所得溶液的溶质成分进行猜想时,除了考虑生成物外还要考虑
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】新型材料纳米级铁粉是指其颗粒大小达到纳米级的单质铁,具有广泛的用途。
(一)纳米铁粉的制备与性质图1为某种制备纳米级铁粉的流程:

(1)请以化学方程式表示该种制备原理_______ ,N2的作用是______ 。
(2)纳米级铁粉在氧气中更容易自燃成黑色固体(Fe3O4),请写出反应的化学方程式_______ ;而铁丝在氧气中需要引燃方能燃烧。由此,你对可燃物着火点的认识是_______ 。
(3)该方法制得的纳米级铁粉样品中常混有少量的FeCl2杂质。为除去样品中的杂质,可在无氧环境下,先加__________ 试剂溶解,再_________ (填一种操作名称)、洗涤、烘干。
(二)纳米铁粉的用途
纳米铁粉对处理酸性废水中的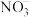 有较好的效果。
有较好的效果。

(4)废水中的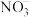 在含纳米铁粉的水处理剂表面的变化如图2,上述变化过程中,化合价降低的元素是
在含纳米铁粉的水处理剂表面的变化如图2,上述变化过程中,化合价降低的元素是________ 。
(5)研究发现:
①纳米铁粉较普通铁粉去除 的速率快得多,其原因是
的速率快得多,其原因是_______ 。
②已知当溶液的pH为7.6时,Fe2+开始沉淀。纳米铁粉在酸性条件下对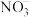 的去除效果要好于中性和碱性条件,其原因是
的去除效果要好于中性和碱性条件,其原因是________ 。
③废水中溶解氧会对 的去除产生一定影响。在其它条件相同情况下,有氧与无氧条件下
的去除产生一定影响。在其它条件相同情况下,有氧与无氧条件下 的去除率随反应时间的变化如图3所示。1~3h时,有氧条件下
的去除率随反应时间的变化如图3所示。1~3h时,有氧条件下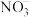 去除率低于无氧条件下,其可能原因是
去除率低于无氧条件下,其可能原因是_______ 。
(一)纳米铁粉的制备与性质图1为某种制备纳米级铁粉的流程:

(1)请以化学方程式表示该种制备原理
(2)纳米级铁粉在氧气中更容易自燃成黑色固体(Fe3O4),请写出反应的化学方程式
(3)该方法制得的纳米级铁粉样品中常混有少量的FeCl2杂质。为除去样品中的杂质,可在无氧环境下,先加
(二)纳米铁粉的用途
纳米铁粉对处理酸性废水中的
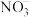 有较好的效果。
有较好的效果。
(4)废水中的
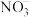 在含纳米铁粉的水处理剂表面的变化如图2,上述变化过程中,化合价降低的元素是
在含纳米铁粉的水处理剂表面的变化如图2,上述变化过程中,化合价降低的元素是(5)研究发现:
①纳米铁粉较普通铁粉去除
 的速率快得多,其原因是
的速率快得多,其原因是②已知当溶液的pH为7.6时,Fe2+开始沉淀。纳米铁粉在酸性条件下对
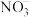 的去除效果要好于中性和碱性条件,其原因是
的去除效果要好于中性和碱性条件,其原因是③废水中溶解氧会对
 的去除产生一定影响。在其它条件相同情况下,有氧与无氧条件下
的去除产生一定影响。在其它条件相同情况下,有氧与无氧条件下 的去除率随反应时间的变化如图3所示。1~3h时,有氧条件下
的去除率随反应时间的变化如图3所示。1~3h时,有氧条件下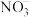 去除率低于无氧条件下,其可能原因是
去除率低于无氧条件下,其可能原因是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】某化学学习小组对泡腾片的成分和原理产生了兴趣。某品牌维生素C泡腾片部分标签如图所示,据此回答问题。
(1)碳酸氢钠(NaHCO3)属于_______ (填“酸”“碱”或“盐”)。
(2)取泡腾片溶于水,滴加紫色石蕊试剂,溶液变红﹐说明溶液pH______ 7(填“>”“<”或“=”)。
(3)泡腾片溶于水时闻到“橙味”香气,从微观角度解释其原因是______ 。
【任务二】测定柠檬酸的含量
(4)碳酸氢钠(NaHCO3)与柠檬酸(C6H8O7,相对分子质量为192)发生的反应为:3NaHCO3+ C6H8O7=Na3C6H5O7+3H2O+3CO2↑。该小组将4g泡腾片投入蒸馏水,反应过程中,相关测量数据如下表。根据化学方程式计算该品牌泡腾片中柠檬酸的质量分数。(假设泡腾片中的NaHCO3完全参与反应,其他物质均不产生气体)

(1)碳酸氢钠(NaHCO3)属于
(2)取泡腾片溶于水,滴加紫色石蕊试剂,溶液变红﹐说明溶液pH
(3)泡腾片溶于水时闻到“橙味”香气,从微观角度解释其原因是
【任务二】测定柠檬酸的含量
(4)碳酸氢钠(NaHCO3)与柠檬酸(C6H8O7,相对分子质量为192)发生的反应为:3NaHCO3+ C6H8O7=Na3C6H5O7+3H2O+3CO2↑。该小组将4g泡腾片投入蒸馏水,反应过程中,相关测量数据如下表。根据化学方程式计算该品牌泡腾片中柠檬酸的质量分数。(假设泡腾片中的NaHCO3完全参与反应,其他物质均不产生气体)
| 反应时间/min | 0 | t1 | t2 | t3 | t4 |
| 锥形瓶及瓶内物质总质量/g | 250.00 | 249.68 | 249.48 | 249.34 | 249.34 |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐1】工业上用电石(主要成分CaC2)生产乙炔(C2H2),反应的化学方程式为CaC2+2H2O=Ca(OH)2+C2H2↑。电石渣是反应后含Ca(OH)2的废渣。
(1)请计算:生产2.6t的C2H2时,生成Ca(OH)2的质量(写出计算过程及结果)。
(2)电石渣可用于制备活性纳米碳酸钙,其主要工艺流程如下图。
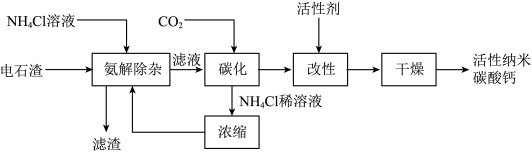
已知:Ⅰ、电石渣中含有SiO2、Al2O3、Fe2O3等杂质,不与NH4Cl反应、难溶于水。
Ⅱ、Ca(OH)2+2NH4Cl=CaCl2+2NH3∙H2O
Ⅲ、CO2+2NH3∙H2O+CaCl2=CaCO3↓+2NH4Cl+H2O
①氨解除杂中,需要进行过滤操作,目的是______ 。
②发生化学反应,生成碳酸钙的步骤是______ (填序号)。
A.氨解除杂 B.碳化 C.改性 D.干燥
③活性纳米碳酸钙中碳元素,来自的原料物质是______ 。
④该生产工艺中,可被循环使用的物质是______ 。
(1)请计算:生产2.6t的C2H2时,生成Ca(OH)2的质量(写出计算过程及结果)。
(2)电石渣可用于制备活性纳米碳酸钙,其主要工艺流程如下图。

已知:Ⅰ、电石渣中含有SiO2、Al2O3、Fe2O3等杂质,不与NH4Cl反应、难溶于水。
Ⅱ、Ca(OH)2+2NH4Cl=CaCl2+2NH3∙H2O
Ⅲ、CO2+2NH3∙H2O+CaCl2=CaCO3↓+2NH4Cl+H2O
①氨解除杂中,需要进行过滤操作,目的是
②发生化学反应,生成碳酸钙的步骤是
A.氨解除杂 B.碳化 C.改性 D.干燥
③活性纳米碳酸钙中碳元素,来自的原料物质是
④该生产工艺中,可被循环使用的物质是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是某实验室分离废弃铜片(含有铁),并用提纯的铜制取胆矾(CuSO4·5H2O)的流程(反应中部分生成物已略去)。

已知: 。
。
(1)胆矾(CuSO4·5H2O)中铜元素的化合价为_______ 。
(2)完成操作a所需要的玻璃仪器是_______ (填一种即可)。
(3)反应①的化学方程式_______ ,反应②的基本类型是_______ 。
(4)由Cu制CuSO4溶液的两种途径中,途径Ⅱ与途径Ⅰ相比较,其显著的优点是_______ 。(回答一点即可)

已知:
 。
。(1)胆矾(CuSO4·5H2O)中铜元素的化合价为
(2)完成操作a所需要的玻璃仪器是
(3)反应①的化学方程式
(4)由Cu制CuSO4溶液的两种途径中,途径Ⅱ与途径Ⅰ相比较,其显著的优点是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题。
(1)诗人陆游的笔记中记载“书灯勿用铜盏,惟瓷盏最省油,蜀中有夹瓷盏…可省油之半”“一端作小窍,注清冷水于其中,每夕一易之”,夹瓷盏被称为省油灯,用棉绳做炷(灯芯),上层盏盛油,下层盏盛水。其结构示意图如下图所示。

①图中属于可燃物的是________ 。
②省油灯的原理是:油燃烧放热,上层内盏油温________ ,下层盏内水吸热,减少油的________ ,以达到省油的目的。
③“注清冷水于其中,每夕一易之”说明下层盏中的水不断减少。对该现象的微观解释正确的是________ (多选,填字母序号)。
a.水分子受热分解b.水分子不断运动c.水分子间隔变大d.水分子数目减少
(2)蔗糖是储藏在某些植物中的糖,日常生活中食用的白糖、冰糖的主要成分就是蔗糖(C12H22O11),它是食品中常用的甜味剂。工业制备蔗糖的流程如下图所示。

①操作a的名称是________ ,在实验室进行此操作时,要用到的玻璃仪器有________ 。
②上述流程中物质M可能是________ 。
③蔗糖(C12H22O11)中碳、氧元素的质量比为________ (化为最简整数比),其中碳元素的质量分数为________ %(保留到0.1%)。
(1)诗人陆游的笔记中记载“书灯勿用铜盏,惟瓷盏最省油,蜀中有夹瓷盏…可省油之半”“一端作小窍,注清冷水于其中,每夕一易之”,夹瓷盏被称为省油灯,用棉绳做炷(灯芯),上层盏盛油,下层盏盛水。其结构示意图如下图所示。

①图中属于可燃物的是
②省油灯的原理是:油燃烧放热,上层内盏油温
③“注清冷水于其中,每夕一易之”说明下层盏中的水不断减少。对该现象的微观解释正确的是
a.水分子受热分解b.水分子不断运动c.水分子间隔变大d.水分子数目减少
(2)蔗糖是储藏在某些植物中的糖,日常生活中食用的白糖、冰糖的主要成分就是蔗糖(C12H22O11),它是食品中常用的甜味剂。工业制备蔗糖的流程如下图所示。

①操作a的名称是
②上述流程中物质M可能是
③蔗糖(C12H22O11)中碳、氧元素的质量比为
您最近一年使用:0次



