有限的元素可以组成种类繁多的物质,请根据H、C、O、Cl、Fe、Cu元素回答问题:
(1)我国著名科学家、化学家侯德榜先生发明了侯式制碱法,其中一步是向反应液体中通入大量气体(约占空气体积0.03%)而生成NaHCO。该气体的化学式为:______ 。
(2)请写出一种常用作食品干燥剂的化学式______ 。
(3)请写出一种能够鉴别出铜和黄铜(铜锌合金)两种物质的化学式______ 。
(4)《天工开物》记载:以炉甘石(ZnCO3)…掺和赤铜矿(CuO)与木炭粉,高温炼制转色为黄铜(铜、锌合金)。请用化学方程式表示该反应的原理:______ 。
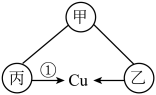
(5)甲、乙、丙是由上述部分元素组成的初中化学常见物质,它们之间有如图所示转化关系(部分反应物、生成物及反应条件已略去,“-”表示相邻一的两种物质能发生反应,“→”表示某一物质经一步反应可转化为另一种物质)。则下列判断错误的是______。(填字母序号)
(1)我国著名科学家、化学家侯德榜先生发明了侯式制碱法,其中一步是向反应液体中通入大量气体(约占空气体积0.03%)而生成NaHCO。该气体的化学式为:
(2)请写出一种常用作食品干燥剂的化学式
(3)请写出一种能够鉴别出铜和黄铜(铜锌合金)两种物质的化学式
(4)《天工开物》记载:以炉甘石(ZnCO3)…掺和赤铜矿(CuO)与木炭粉,高温炼制转色为黄铜(铜、锌合金)。请用化学方程式表示该反应的原理:
(5)甲、乙、丙是由上述部分元素组成的初中化学常见物质,它们之间有如图所示转化关系(部分反应物、生成物及反应条件已略去,“-”表示相邻一的两种物质能发生反应,“→”表示某一物质经一步反应可转化为另一种物质)。则下列判断错误的是______。(填字母序号)

| A.甲、乙、丙可能都是单质 | B.甲可能是碱 |
| C.反应① 不可能是化合反应 | D.丙不可能为氯化铜 |
更新时间:2023-06-08 21:34:54
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
【推荐1】金属及其制品是现代生活中常见的材料,请回答下列问题:
(1)铁可以做成铁锅炒菜,主要是利用了铁的_____ (填“导电”或“导热”)性。
(2)航母外壳用涂料覆盖,是为了防止钢铁材料与_____ 接触而锈蚀。
(3)铁锈的主要成分是氧化铁,用盐酸可以除去自行车钢圈上的铁锈,其反应的化学方程式是_____ 。
(4)在硝酸铜和硝酸银的混合溶液中,加入一定量铁粉,使之充分反应后,过滤,向所得滤渣中加入适量稀盐酸,没有气体产生,则滤渣中一定有_____ (填化学式),滤液中的溶质一定含有_____ (填化学式)。
(5)某同学用称量法测定铁在氧气中燃烧的产物。将 铁在一定量的氧气中燃烧得到
铁在一定量的氧气中燃烧得到 固体。则得到的固体产物可能是
固体。则得到的固体产物可能是_____ (填字母)。
A B
B  和
和 的混合物
的混合物
C 和
和 的混合物 D
的混合物 D  、
、 和
和 的混合物
的混合物
(1)铁可以做成铁锅炒菜,主要是利用了铁的
(2)航母外壳用涂料覆盖,是为了防止钢铁材料与
(3)铁锈的主要成分是氧化铁,用盐酸可以除去自行车钢圈上的铁锈,其反应的化学方程式是
(4)在硝酸铜和硝酸银的混合溶液中,加入一定量铁粉,使之充分反应后,过滤,向所得滤渣中加入适量稀盐酸,没有气体产生,则滤渣中一定有
(5)某同学用称量法测定铁在氧气中燃烧的产物。将
 铁在一定量的氧气中燃烧得到
铁在一定量的氧气中燃烧得到 固体。则得到的固体产物可能是
固体。则得到的固体产物可能是A
 B
B  和
和 的混合物
的混合物C
 和
和 的混合物 D
的混合物 D  、
、 和
和 的混合物
的混合物
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐2】已知:A、B、C、D、E、F六种物质是初中化学常见的物质。A、B是单质,C、D、E都是氧化物。A、B、C转化为F的过程较为复杂,F的成份也较复杂,其主要成分是一种红色的固体。试根据各物质间的转化关系完成下列各题。(题中除反应条件未给出外,反应物和产物均已给出。)

(1)写出F中主要成分的化学式:__________________ 。
(2)写出下列物质转化的化学方程式:
E→B+C:______________________________ ;
A+B→D:______________________________ ;

(1)写出F中主要成分的化学式:
(2)写出下列物质转化的化学方程式:
E→B+C:
A+B→D:
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
名校
解题方法
【推荐1】如图所示“雪花”各瓣代表的物质A~F,通过一步反应均可生成硫酸亚铁。A为铁,B和F属于盐,C、D、E属于其它不同类别的纯净物(或其溶液)。

(1)若E为酸
①E的化学式为_______ 。
②“D→FeSO4”发生中和反应,该反应化学方程式为___________ 。
③B、C均与E反应生成FeSO4,则C为__________ (填化学式)。
(2)若F为黄色溶液,F与铁通过化合反应生成FeSO4,该反应化学方程式__________ 。

(1)若E为酸
①E的化学式为
②“D→FeSO4”发生中和反应,该反应化学方程式为
③B、C均与E反应生成FeSO4,则C为
(2)若F为黄色溶液,F与铁通过化合反应生成FeSO4,该反应化学方程式
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐2】如图中A~F为初中常见物质,且B、C、D、E、F为不同类别的物质。已知A为世界年产量最高的金属,B物质的溶液为蓝色,D物质的俗名为烧碱。(图中“→”表示转化关系,“一”表示相互能反应,所涉及反应均为初中常见的化学反应)。回答下列问题:

(1)A物质的化学式为______ 。
(2)C物质的物质类别为______ 。
(3)B物质和D物质发生反应的化学方程式为______ 。
(4)E物质和F物质相互转化一定不涉及的基本反应类型是______ 。

(1)A物质的化学式为
(2)C物质的物质类别为
(3)B物质和D物质发生反应的化学方程式为
(4)E物质和F物质相互转化一定不涉及的基本反应类型是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】某兴趣小组利用废镍材料(含有金属Ni及少量Fe、Ag、Fe2O3)探究相关物质的性质并回收镍,设计流程如图所示。

资料:a.H2O2溶液可将Fe2+转化为Fe3+。
b.Fe2+、Fe3+、Ni2+转化为对应的氢氧化物沉淀时,溶液pH有如图关系:

(1)废镍材料“粉碎”的目的是_____ 。
(2)“酸浸”中发生的反应化学方程式除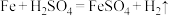 、
、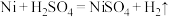 、还有
、还有_____ ;X是_____ (填名称)。
(3)在“转化1”中,加入试剂先后顺序是_____(填字母)。
(4)在“转化1”中,加NaOH溶液调节pH为_____ (填范围)。操作A是_____ ,该操作中所用到的玻璃仪器有玻璃棒、烧杯和_____ 。
(5)Ni、Fe、Ag三种金属的活动性由强到弱的顺序为_____ 。

资料:a.H2O2溶液可将Fe2+转化为Fe3+。
b.Fe2+、Fe3+、Ni2+转化为对应的氢氧化物沉淀时,溶液pH有如图关系:

(1)废镍材料“粉碎”的目的是
(2)“酸浸”中发生的反应化学方程式除
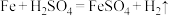 、
、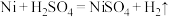 、还有
、还有(3)在“转化1”中,加入试剂先后顺序是_____(填字母)。
| A.先加H2O2溶液,再加NaOH溶液 | B.先加NaOH溶液,再加H2O2溶液 |
(5)Ni、Fe、Ag三种金属的活动性由强到弱的顺序为
您最近一年使用:0次
【推荐2】我国海岸线曲折.海洋资源十分丰富。

(1)如图1A所示,从海水中获得淡水的方法是______ ,你认为该技术的优点是__________ ;如图1B所示,是恒温下模拟海水晒盐过程的示意图,与丙烧杯烧杯溶液的溶质质量分数一定相同的是________ (填序号,下同);
(2)从海水中提取金属镁,可按图2流程进行:

①写出步骤Ⅱ发生反应的化学方程式____________________ ;
②根据图2流程图,下列说法正确的是__________________ ;
A.步骤Ⅰ通过一步反应即可实现
B.步骤Ⅱ、Ⅲ、Ⅳ的目的是从海水中提纯氧化镁
C.步骤Ⅲ发生了中和反应
D.步骤Ⅴ中化学能转化为电能
③该流程中采取的一种降低成本且减少污染的措施是________________ ;
(3)我国著名化学家侯德榜发明的“联合制碱法”主要工艺流程示意图如图3

①为了除去粗盐水中可溶性杂质,可加入下列物质,利用过滤等操作进行除杂,则加入下列三种物质的先后顺序为_____________ (填序号);用化学方程式表示加入适量盐酸后先发生反应的化学方程式___________________
a.稍过量的Na2CO3溶液 b.适量的盐酸 c.稍过量的Ba(OH)2溶液
②流程中氨化溶液的pH_____ 7(填“>”、“<”或“═”),从而有利于吸收气体A
③流程中,碳酸化时发生反应的化学方程式为____________ 。

(1)如图1A所示,从海水中获得淡水的方法是
(2)从海水中提取金属镁,可按图2流程进行:

①写出步骤Ⅱ发生反应的化学方程式
②根据图2流程图,下列说法正确的是
A.步骤Ⅰ通过一步反应即可实现
B.步骤Ⅱ、Ⅲ、Ⅳ的目的是从海水中提纯氧化镁
C.步骤Ⅲ发生了中和反应
D.步骤Ⅴ中化学能转化为电能
③该流程中采取的一种降低成本且减少污染的措施是
(3)我国著名化学家侯德榜发明的“联合制碱法”主要工艺流程示意图如图3

①为了除去粗盐水中可溶性杂质,可加入下列物质,利用过滤等操作进行除杂,则加入下列三种物质的先后顺序为
a.稍过量的Na2CO3溶液 b.适量的盐酸 c.稍过量的Ba(OH)2溶液
②流程中氨化溶液的pH
③流程中,碳酸化时发生反应的化学方程式为
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐3】游园活动中有一个“化学幸运大转盘”游戏。转盘外圈的五种物质分别是铁、盐酸、氢氧化钙、碳酸钠和硫酸铜中的一种,相邻的外圈物质能发生反应,其中C是单质,D和E可配制农药波尔多液,G的物质类别不同于外圈的五种物质,当G的指针转到的物质能与其发生反应时即中幸运大奖。

(1)E的俗称是______ 。
(2)足量C与一定量D溶液反应,足够长时间后可观察到的现象是______ 。
(3)A、E之间反应的化学方程式为______ 。
(4)某同学转动G的指针指向了B,中了幸运大奖(G和B物质发生化学反应),发生反应的化学方程式为______ (写一个)。

(1)E的俗称是
(2)足量C与一定量D溶液反应,足够长时间后可观察到的现象是
(3)A、E之间反应的化学方程式为
(4)某同学转动G的指针指向了B,中了幸运大奖(G和B物质发生化学反应),发生反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】纯碱是重要的化工原料,在玻璃、肥料、合成洗涤剂等工业中有着广泛的应用。
(1)工业上“侯氏制碱法”以NaCl、NH3、CO2及水等为原料制备纯碱,其反应原理为NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。然后再焙烧NaHCO3制得纯碱(Na2CO3)。生产纯碱的工艺流程示意图如下:

请回答下列问题:
①操作A的名称为______ 。
②可用______ 结晶的方法获得物质B固体。
③向沉淀池中先通入足量NH3,后通入CO2,析出NaHCO3晶体而不是Na2CO3晶体,其原因是______ 。
④析出NaHCO3晶体中可能含有少量氯离子杂质,实验室确定NaHCO3晶体表面杂质洗净的方法______
(2)常温下在10mL10.6g·L-1Na2CO3溶液中逐滴加入3.65g·L-1HCl溶液20mL,溶液中含碳元素的各种微粒的质量分数(纵轴)随溶液pH变化的部分情况如图所示。

根据图示回答下列问题:
①在同一溶液中, 、
、 、H2CO3
、H2CO3______ (填“能”或“不能”)大量共存。
②当pH=7时,溶液中含碳元素的主要微粒为______ 和______ (填化学式)。
(1)工业上“侯氏制碱法”以NaCl、NH3、CO2及水等为原料制备纯碱,其反应原理为NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。然后再焙烧NaHCO3制得纯碱(Na2CO3)。生产纯碱的工艺流程示意图如下:

请回答下列问题:
①操作A的名称为
②可用
③向沉淀池中先通入足量NH3,后通入CO2,析出NaHCO3晶体而不是Na2CO3晶体,其原因是
④析出NaHCO3晶体中可能含有少量氯离子杂质,实验室确定NaHCO3晶体表面杂质洗净的方法
(2)常温下在10mL10.6g·L-1Na2CO3溶液中逐滴加入3.65g·L-1HCl溶液20mL,溶液中含碳元素的各种微粒的质量分数(纵轴)随溶液pH变化的部分情况如图所示。

根据图示回答下列问题:
①在同一溶液中,
 、
、 、H2CO3
、H2CO3②当pH=7时,溶液中含碳元素的主要微粒为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
真题
解题方法
【推荐2】侯德榜是我国著名的化学家,为纯碱和氮肥工业技术的发展作出了杰出的贡献,他发明的侯氏制碱法大大提高了原料的利用率,其工业流程大致如图:
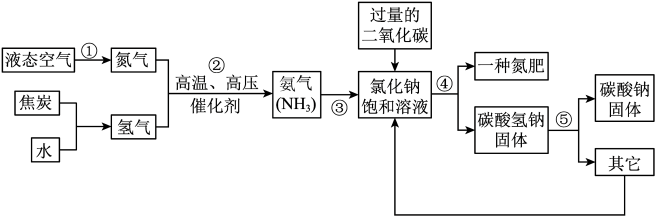
(1)上述流程中,用到的原料有空气、焦炭、水、二氧化碳、_________ 等.
(2)上述流程中,已知步骤②发生的是化合反应,步骤⑤发生的是分解反应,则步骤②、⑤发生反应的化学方程式是:②_________ ,⑤_________ .
(3)上述流程中,可循环利用的物质是_________ .
(4)上述流程中,“一种氮肥”的化学式是_________ .

(1)上述流程中,用到的原料有空气、焦炭、水、二氧化碳、
(2)上述流程中,已知步骤②发生的是化合反应,步骤⑤发生的是分解反应,则步骤②、⑤发生反应的化学方程式是:②
(3)上述流程中,可循环利用的物质是
(4)上述流程中,“一种氮肥”的化学式是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐3】1926 年,我国著名化学家侯德榜改进了国外的纯碱生产工艺,发明了“联合制碱法”,其主要流程如图所示。

已知在沉淀池中发生的反应为: 。
。
回答下列问题:
(1)操作1是_____ (填操作名称)。
(2)操作2将固体充分加热,写出反应的化学方程式_____ 。
(3)“联合制碱法 ”使原料氯化钠的利用率从70%提高到96%,主要是因为设计了循环_____ (填数字序号)。
(4)纯碱样品中可能会含有少量氯化钠杂质。为了检验纯碱样品中是否含有氯化钠应选用的试剂是_____ 。

已知在沉淀池中发生的反应为:
 。
。回答下列问题:
(1)操作1是
(2)操作2将固体充分加热,写出反应的化学方程式
(3)“联合制碱法 ”使原料氯化钠的利用率从70%提高到96%,主要是因为设计了循环
(4)纯碱样品中可能会含有少量氯化钠杂质。为了检验纯碱样品中是否含有氯化钠应选用的试剂是
您最近一年使用:0次

 溶液中,待反应完全后过滤。向滤渣中加入少量盐酸产生气泡,则滤渣中一定有
溶液中,待反应完全后过滤。向滤渣中加入少量盐酸产生气泡,则滤渣中一定有


