水和溶液在生产生活中起着重要的作用。
(1)明矾可用于净水,是因为明矾溶于水生成的胶状物可以吸附悬浮于水中的杂质,使之从水中沉淀出来;生活中常用______ 来检验某天然水是硬水还是软水,常用______ 方法降低水的硬度。
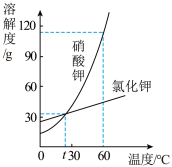
(2)硝酸钾和氯化钾两种物质的溶解度见下表,这两种物质的溶解度曲线见下图。
请回答下列问题:
①物质乙的化学式为______ 。
②60℃时,分别将等质量的KNO3饱和溶液和KCl饱和溶液温度降至t℃,所得溶液中KNO3的质量______ KCl的质量(填“大于”或“小于”或“等于”)。
③如图所示,20℃时,将一定质量的KNO3固体放入盛水的试管中,发现有少量固体未溶解,向烧杯内的水中加入生石灰后,试管内的固体会______ (填“减少”或“增多)。
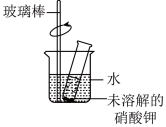
(3)请设计实验证明硝酸铵溶于水时是吸收热量的,并完成实验报告。
(1)明矾可用于净水,是因为明矾溶于水生成的胶状物可以吸附悬浮于水中的杂质,使之从水中沉淀出来;生活中常用
(2)硝酸钾和氯化钾两种物质的溶解度见下表,这两种物质的溶解度曲线见下图。

| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/ g | 甲 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
| 乙 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | |
①物质乙的化学式为
②60℃时,分别将等质量的KNO3饱和溶液和KCl饱和溶液温度降至t℃,所得溶液中KNO3的质量
③如图所示,20℃时,将一定质量的KNO3固体放入盛水的试管中,发现有少量固体未溶解,向烧杯内的水中加入生石灰后,试管内的固体会

(3)请设计实验证明硝酸铵溶于水时是吸收热量的,并完成实验报告。
| 实验步骤 | 实验现象 | 实验结论 |
| 取20mL蒸馏水于烧杯中 | 硝酸铵溶于水时是吸收热量的 |
23-24九年级下·江苏南京·开学考试 查看更多[1]
(已下线)九年级化学开学摸底考02(南京专用,人教版1-9单元)-2023-2024学年初中下学期开学摸底考试卷
更新时间:2024-02-04 15:53:33
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】人类的生活和工农业生产都离不开水。下图是自来水厂净水过程示意图。
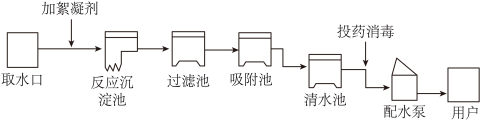
(1)在以上示意图中,上述自来水厂使用的净水方法有___________。(填标号)
(2)锅炉用水硬度高了内部容易结垢,既浪费燃料,又易使内部管道局部过热而造成危险,因此锅炉要使用软水,区分软水和硬水常用的物质是________ ;往水中加入该物质后,出现大量浮渣,几乎无泡沫,说明该水是____________ (填“硬水”或“软水”),在日常生活中,把硬水转化为软水的方法是____________ 。
(3)现要过滤一瓶浑浊的河水,除要用到铁架台(带铁圈)、玻璃棒、烧杯外,还需要的仪器是_________ ;过滤中要注意“一贴二低三靠”,“三靠”中的其中“一靠”是指玻璃棒下端要轻靠三层滤纸处,而不能靠在单层滤纸处,这样操作的原因是____________ 。
(4)如图所示是水的电解实验。与电源正极相连的试管b中的气体是_______ ;与电源负极相连的试管 a 中的气体是____________ 。

(5)下列反应中,能用来确定水是由氢、氧元素组成的是_______ 和_______ (填标号)。
A. 电解水 B. H2O 与 CO2反应 C. H2与O2反应

(1)在以上示意图中,上述自来水厂使用的净水方法有___________。(填标号)
| A.煮沸 | B.吸附 | C.蒸馏 | D.过滤 | E.沉淀 |
(3)现要过滤一瓶浑浊的河水,除要用到铁架台(带铁圈)、玻璃棒、烧杯外,还需要的仪器是
(4)如图所示是水的电解实验。与电源正极相连的试管b中的气体是

(5)下列反应中,能用来确定水是由氢、氧元素组成的是
A. 电解水 B. H2O 与 CO2反应 C. H2与O2反应
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】目前许多学校安装了直饮水机,其主要工作流程如图所示,
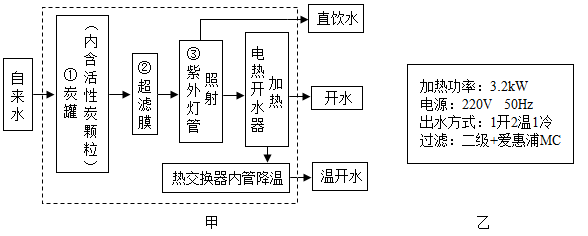
(1)图中①的作用是_______ 。
A杀毒消毒 B吸附杂质 C蒸馏 D过滤
(2)直饮水机使用方便:只有将它与自来水管网对接,截留清除水中的有害物质(如细菌等),便得到直饮水,直饮水属于________ (选填“混合物”或“纯净物”)。
(3)判断直饮水是硬水还是软水,可用的物质是_________ 。
(4)长期饮用硬水对人体健康不利,要降低水的硬度,实验室中降低水的硬度的方法是________ ,生活中通过_______ 也可以降低水的硬度。

(1)图中①的作用是
A杀毒消毒 B吸附杂质 C蒸馏 D过滤
(2)直饮水机使用方便:只有将它与自来水管网对接,截留清除水中的有害物质(如细菌等),便得到直饮水,直饮水属于
(3)判断直饮水是硬水还是软水,可用的物质是
(4)长期饮用硬水对人体健康不利,要降低水的硬度,实验室中降低水的硬度的方法是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】某县自来水的水源地是一个大型水库,某化学兴趣小组开展了一次净化水的实践活动。请回答下列问题:
(1)对所取水样进行过滤,除了滤纸和下图提供的仪器外,还需要的一种玻璃仪器是______________ 。
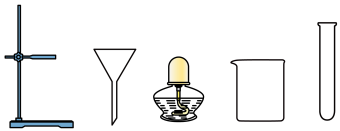
(2)向滤液中加入活性炭,利用其______________ 性除去异味,再次过滤。
(3)为了检验所得滤液是否为硬水,取样加入______________ ,根据产生白色垢状物或泡沫的多少进行判断。
(4)自来水的生产过程中常用二氧化氯(ClO2)灭菌,将Cl2通入NaClO2溶液中可制得ClO2和一种生活中常见的盐,反应的化学方程式为 ,其中X的化学式为
,其中X的化学式为______________ 。
(5)用自来水烧水的水壶底部,容易形成水垢,水垢的主要成分是碳酸钙和氢氧化镁,可以用厨房中的一种调味品来清除,这种调味品是______________ 。
(6)保护水环境,珍爱水资源,是每个公民应尽的责任和义务,下列做法有利于保护水资源的是 (填字母序号)。
(1)对所取水样进行过滤,除了滤纸和下图提供的仪器外,还需要的一种玻璃仪器是

(2)向滤液中加入活性炭,利用其
(3)为了检验所得滤液是否为硬水,取样加入
(4)自来水的生产过程中常用二氧化氯(ClO2)灭菌,将Cl2通入NaClO2溶液中可制得ClO2和一种生活中常见的盐,反应的化学方程式为
 ,其中X的化学式为
,其中X的化学式为(5)用自来水烧水的水壶底部,容易形成水垢,水垢的主要成分是碳酸钙和氢氧化镁,可以用厨房中的一种调味品来清除,这种调味品是
(6)保护水环境,珍爱水资源,是每个公民应尽的责任和义务,下列做法有利于保护水资源的是 (填字母序号)。
| A.化肥和农药的过度使用 |
| B.实验室的废液不经处理直接排放 |
| C.使用含磷的洗衣粉 |
| D.燃煤中加入石灰石作为固硫剂,减少酸雨对水源的污染 |
您最近一年使用:0次
【推荐1】如图是常见固体物质的溶解度曲线,根据图示回答:

(1)d点的意义是______ 。
(2)t2℃时A、B、C的相同质量饱和溶液中,溶剂质量由大到小顺序是__________ (用“>”“<”“=”表示)。
(3)将t1℃一定量A的饱和溶液升温至t3℃时,可用图上的点表示;若要将图中“b”点表示A的溶液情况变为“c”点,宜采取的方法______ 。
(4)若将t3℃三种物质的饱和溶液分别降温到t1℃,则对所得三种溶液说法正确是______ 。(析出晶体都不含结晶水)
I、都是饱和溶液 II、溶质的质量分数:B>C>A
III、溶剂质量都不变 IV、析出溶质的质量:A>B>C
(5)鉴别蒸馏水和稀硝酸钾溶液,完成实验报告。

(1)d点的意义是
(2)t2℃时A、B、C的相同质量饱和溶液中,溶剂质量由大到小顺序是
(3)将t1℃一定量A的饱和溶液升温至t3℃时,可用图上的点表示;若要将图中“b”点表示A的溶液情况变为“c”点,宜采取的方法
(4)若将t3℃三种物质的饱和溶液分别降温到t1℃,则对所得三种溶液说法正确是
I、都是饱和溶液 II、溶质的质量分数:B>C>A
III、溶剂质量都不变 IV、析出溶质的质量:A>B>C
(5)鉴别蒸馏水和稀硝酸钾溶液,完成实验报告。
| 实验步骤 | 实验现象 | 实验结论 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】南海是我国固有领海,汉代、南北朝时称为涨海、沸海,清代逐渐改称南海。2017年5月18日,我国南海神狐海域可燃冰试采成功,实现历史性突破。
(1)可燃冰的主要成分是甲烷,试写出甲烷在空气中燃烧的化学方程式_______ 。
(2)甲烷高温分解可得炭黑(炭黑:主要是由碳元素组成的物质),炭黑可用于制作太阳能电池。计算至少需要高温分解_______ g甲烷才能得到24g炭黑。
(3)镁元素广泛应用于火箭、导弹和飞机制造业,被称为“国防元素”,如图是以海水为原料制取单质镁的过程,试回答下列问题:

过程①中,所加石灰乳的主要成分是_______ (填写化学式);
过程②发生的化学反应类型属于_______ (填“化合反应”、“分解反应”、“置换反应”或“复分解反应”),写出该过程中的化学方程式_______ 。过程③是将_______ 转化为化学能。
(4)1926年我国著名化学家侯德榜先生创立了侯氏制碱法,促进了世界制碱技术的发展。侯氏制碱法以食盐为主要原料制取纯碱,制得的纯碱中常含有少量氯化钠。Na2CO3和NaCl的溶解度曲线如图所示,试回答下列问题:

①据图所示,t1℃时,Na2CO3的溶解度是_______ 。
②t1℃时,分别将等质量的Na2CO3和NaCl固体置于烧杯中,加水溶解,配制成该温度下的饱和溶液,所得Na2CO3饱和溶液质量_______ NaCl饱和溶液质量(填“大于”、“等于”或“小于”之一)。
③t1℃时,将不同质量的Na2CO3饱和溶液和NaCl饱和溶液均升温到t2℃,此时所得Na2CO3溶液溶质质量分数_______ NaCl溶液溶质质量分数(填“大于”、“等于”、或“小于”之一)。
④通过Na2CO3溶解度曲线图判断,可采用_______ (填“蒸发结晶”或“降温结晶”)的方法使Na2CO3从其饱和溶液中析出。
(1)可燃冰的主要成分是甲烷,试写出甲烷在空气中燃烧的化学方程式
(2)甲烷高温分解可得炭黑(炭黑:主要是由碳元素组成的物质),炭黑可用于制作太阳能电池。计算至少需要高温分解
(3)镁元素广泛应用于火箭、导弹和飞机制造业,被称为“国防元素”,如图是以海水为原料制取单质镁的过程,试回答下列问题:

过程①中,所加石灰乳的主要成分是
过程②发生的化学反应类型属于
(4)1926年我国著名化学家侯德榜先生创立了侯氏制碱法,促进了世界制碱技术的发展。侯氏制碱法以食盐为主要原料制取纯碱,制得的纯碱中常含有少量氯化钠。Na2CO3和NaCl的溶解度曲线如图所示,试回答下列问题:

①据图所示,t1℃时,Na2CO3的溶解度是
②t1℃时,分别将等质量的Na2CO3和NaCl固体置于烧杯中,加水溶解,配制成该温度下的饱和溶液,所得Na2CO3饱和溶液质量
③t1℃时,将不同质量的Na2CO3饱和溶液和NaCl饱和溶液均升温到t2℃,此时所得Na2CO3溶液溶质质量分数
④通过Na2CO3溶解度曲线图判断,可采用
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
【推荐1】如图为甲、乙两种固体物质的溶解度曲线(水的密度约为1g/cm3)
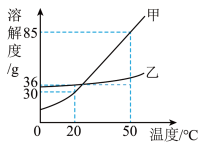
(1)两种物质中,溶解度受温度影响更大的是______ (填“甲”或“乙”);
(2)20℃时,乙的溶解度为_____ ;
(3)下列实验中:10ml水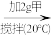 X
X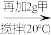 Y
Y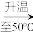 Z为饱和溶液的是
Z为饱和溶液的是______ (填“X”或“Y”或“Z”);若三种溶液中溶质的质量分数分别为a、b、c,则它们的大小关系是_______ (用“<”或“>”或“=”表示出来)。

(1)两种物质中,溶解度受温度影响更大的是
(2)20℃时,乙的溶解度为
(3)下列实验中:10ml水
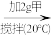 X
X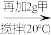 Y
Y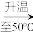 Z为饱和溶液的是
Z为饱和溶液的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】我国著名化学家侯德榜先生创立了联合制碱(Na2CO3)法,促进了世界制碱技术的发展。Na2CO3和NaCl的溶解度曲线如图1所示,试回答下列问题:
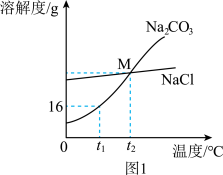
(1)t1°C时,Na2CO3的溶解度为___________ 。
(2)从氯化钠饱和溶液中得到氯化钠的方法___________ (“降温结晶”或“蒸发结晶”)。
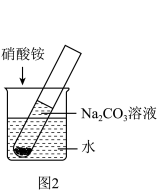
(3)t1°C时,将10gNa2CO3固体放入盛有50g水的试管中,充分溶解,所得溶液的溶质质量分数为___________ (结果保留0.1%);然后将试管放入盛有水的烧杯中(如图2所示),再取适量硝酸铵固体放入烧杯内的水中,用玻璃棒搅拌溶解,此时可观察到试管底部固体___________ (填“增加“或“减少”或“无变化”)。
(4)将t2℃时等质量的Na2CO3饱和溶液和NaCl饱和溶液均降温至t1°C,此时所得两溶液的质量相比较,Na2CO3___________ NaCl(填“>”或“<”或“=”)。


(1)t1°C时,Na2CO3的溶解度为
(2)从氯化钠饱和溶液中得到氯化钠的方法
(3)t1°C时,将10gNa2CO3固体放入盛有50g水的试管中,充分溶解,所得溶液的溶质质量分数为
(4)将t2℃时等质量的Na2CO3饱和溶液和NaCl饱和溶液均降温至t1°C,此时所得两溶液的质量相比较,Na2CO3
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】图为a、b、c三种物质的溶解度曲线,据图回答:
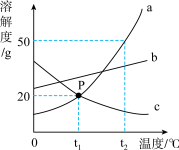
(1)t2℃时a的溶解度是_____ ,该温度下a物质的饱和溶液中溶质的质量分数是 _____ 。
(2)P点的含义是_____
(3)t2℃时将a物质40g加入到50g水中充分搅拌,形成溶液的质量是_____ g.
(4)t2℃时,a物质饱和溶液中,溶质、溶剂、溶液的质量之比为_____ (填最简比).
(5)当温度发生变化时,a、b两物质溶解度变化最明显的是_____ 物质,该物质宜采用 _____ 结晶的方法从其溶液中分离。若b中含有少量a ,要提纯b,应用 _____ 法。
(6)某温度下c物质的不饱和溶液转变为饱和溶液,可采用的方法是_____ 、 _____ 、 _____ 。
(7)t2℃时,a、b、c三种物质的饱和溶液各100g,分别降温到t1℃时,析出晶体最多的是_____ ,没有晶体析出的是 _____ 。

(1)t2℃时a的溶解度是
(2)P点的含义是
(3)t2℃时将a物质40g加入到50g水中充分搅拌,形成溶液的质量是
(4)t2℃时,a物质饱和溶液中,溶质、溶剂、溶液的质量之比为
(5)当温度发生变化时,a、b两物质溶解度变化最明显的是
(6)某温度下c物质的不饱和溶液转变为饱和溶液,可采用的方法是
(7)t2℃时,a、b、c三种物质的饱和溶液各100g,分别降温到t1℃时,析出晶体最多的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】氢氧化钙俗称熟石灰,在生产和生活中有广泛的用途。
(1)熟石灰可由生石灰溶于水制得,反应的化学方程式是________________________ 。
(2)用石灰水检验二氧化碳,反应的化学方程式是________________________ 。
(3)用熟石灰来改良酸性土壤,反应的化学方程式是_______________ (以土壤中含有硫酸为例)。
(4)用熟石灰粉与草木灰(主要成分是K2CO3)按一定比例混合可制得高效环保农药“黑白粉”。使用时,选择在有露水的早晨,把“黑白粉”撒在植物茎叶上,可消除忌碱虫体。“黑白粉”可提供植物必需的营养元素是________ (填元素符号)。
(1)熟石灰可由生石灰溶于水制得,反应的化学方程式是
(2)用石灰水检验二氧化碳,反应的化学方程式是
(3)用熟石灰来改良酸性土壤,反应的化学方程式是
(4)用熟石灰粉与草木灰(主要成分是K2CO3)按一定比例混合可制得高效环保农药“黑白粉”。使用时,选择在有露水的早晨,把“黑白粉”撒在植物茎叶上,可消除忌碱虫体。“黑白粉”可提供植物必需的营养元素是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】现有Zn、HCl、Ca(OH)2、Na2CO3、CaO五种物质.根据要求回答:
(1)可用于食品干燥剂的是_____ .
(2)从物质的组成看,有一种物质和其它四种物质不同类属.该物质是_____ .
(3)可和其它四种物质发生化学反应的物质是_____ ,写出该物质和其它四种物质中的一种反应的化学方程式_____ .
(1)可用于食品干燥剂的是
(2)从物质的组成看,有一种物质和其它四种物质不同类属.该物质是
(3)可和其它四种物质发生化学反应的物质是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】利用化学知识,完成下列填空。
(1)为了保证人身安全,进入久未开启的菜窖前,必须先做______ 实验。
(2)篝火晚会时,应将木材架空烧,原理是______ 。
(3)热水瓶胆里的水垢,可用厨房里的______ (调味品名称)除去。
(4)茶杯内的纱网可将亲叶与茶水分离,便于饮用,利用的化学原理是______ 。
(5)发令枪响时会有自烟产生,根据你所学的知识可以知道白烟的成分是______ 。
(6)“自热火锅”的原理定利用氧化钙和水反应生成氢氧化钙,此反应是______ (填“放热”“吸热”)反应的化学方程式为______ 。
(1)为了保证人身安全,进入久未开启的菜窖前,必须先做
(2)篝火晚会时,应将木材架空烧,原理是
(3)热水瓶胆里的水垢,可用厨房里的
(4)茶杯内的纱网可将亲叶与茶水分离,便于饮用,利用的化学原理是
(5)发令枪响时会有自烟产生,根据你所学的知识可以知道白烟的成分是
(6)“自热火锅”的原理定利用氧化钙和水反应生成氢氧化钙,此反应是
您最近一年使用:0次




