2023年,中国的创新动力、发展活力勃发奔涌,都高不开金属材料的应用:C919大飞机实现商飞,国产大型邮轮完成试航,神舟家族太空接力,“奋斗者”号极限深潜。
(1)C919大飞机的机身主体材料是铝合金,使用铝合金的优点主要体现在其____ 大于纯铝;铝有很好抗腐蚀性原因是_____ 。
(2)航天器的天线是由钛合金制造。工业上通常用四氯化钛(TiCl4)与金属镁在高温下发生置换反应获得金属钛,该反应的化学方程式为_____ 。
(3)金属矿物资源的储量有限,而且不能再生,我们需要保护金属资源。下列关于铁制品的防锈措施合理的是 (填字母)。
(1)C919大飞机的机身主体材料是铝合金,使用铝合金的优点主要体现在其
(2)航天器的天线是由钛合金制造。工业上通常用四氯化钛(TiCl4)与金属镁在高温下发生置换反应获得金属钛,该反应的化学方程式为
(3)金属矿物资源的储量有限,而且不能再生,我们需要保护金属资源。下列关于铁制品的防锈措施合理的是 (填字母)。
| A.经常用水冲洗自行车链条 |
| B.在铁制栏杆表面刷油漆 |
| C.用不锈钢等合金代替铁制部件 |
| D.对铁制零件进行“烤蓝”处理 |
更新时间:2024-02-26 23:04:04
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】从某废旧电子产品中可以提炼贵重金属,并得到硫酸铜溶液。其工艺流程如图所示:

(1)图中“操作”的名称是______ ,该操作用到的玻璃仪器有烧杯、玻璃棒和______ (填仪器名称)。
(2)①中发生反应的基本类型为______ 。
(3)写出所得贵重金属中任意一种成分的化学式:______ 。
(4)写出②中发生反应的化学方程式:______ 。

(1)图中“操作”的名称是
(2)①中发生反应的基本类型为
(3)写出所得贵重金属中任意一种成分的化学式:
(4)写出②中发生反应的化学方程式:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】根据所学知识回答下列问题:
(1)2021年4月1日,500米口径球面射电望远镜(简称FAST)面向全球开放。FAST是具有我国自主知识产权、世界最大单口径、最灵敏的射电望远镜,被誉为“中国天眼”。大国重器,深探苍穹,它是中国科学家二十多年的心血结晶。

①“天眼”的球面射电板是用铝合金作为材料,铝合金属于___________ (填“金属材料”“有机非金属材料”或“复合材料”)。
②铝是地壳中含量最多的金属元素,在高温条件下,铝与氧化铁反应生成单质铁和一种氧化物并放出大量的热,因此铁路工人用铝来焊接钢轨,写出该反应的化学方程式:___________ ,该反应的反应类型是___________ (填“化合”“分解”“置换”或“复分解”)反应。
③开发和利用清洁又高效的新能源,是21世纪人类面临的重要课题。氢气作为新能源,有很多优点,制取与储存氢气是氢能源利用领域的研究热点。Mg2Cu是一种潜在的贮氢材料,吸氢发生反应的化学方程式为2Mg2Cu+3H2 3MgH2+MgCu2.查阅资料可知:MgH2与水反应生成一种碱,并释放出H2.写出此反应的化学方程式
3MgH2+MgCu2.查阅资料可知:MgH2与水反应生成一种碱,并释放出H2.写出此反应的化学方程式___________ 。
(2)1926 年我国化学家侯德榜创立了“侯氏制碱法”,促进了世界制碱技术的发展,使原料NaCl的利用率由70%提高到96%,也使原来的副产物 CaCl2转化成化肥NH4Cl。“制碱” 生产过程涉及Na2CO3、NaHCO3、 NH4Cl、NaCl等物质,Na2CO3和NaCl两物质的溶解度曲线如下图所示。试回答下列问题:

①在t2 ℃时,Na2CO3的溶解度___________ NaCl的溶解度(填“大于”“小于”或“等于”)。
②在t2 ℃时,分别取质量相等的Na2CO3、NaCl溶于水制成饱和溶液,降温至t1 ℃时,Na2CO3溶液的质量___________ NaCl溶液的质量(填“大于”“小于”或“等于”)。
③生活在盐碱湖附近的人们有一句谚语“夏天晒盐,冬天捞碱”,此处的“碱”指的是纯碱,请结合溶解度曲线,说明谚语中“冬天捞碱”的原因是____________________ 。
(1)2021年4月1日,500米口径球面射电望远镜(简称FAST)面向全球开放。FAST是具有我国自主知识产权、世界最大单口径、最灵敏的射电望远镜,被誉为“中国天眼”。大国重器,深探苍穹,它是中国科学家二十多年的心血结晶。

①“天眼”的球面射电板是用铝合金作为材料,铝合金属于
②铝是地壳中含量最多的金属元素,在高温条件下,铝与氧化铁反应生成单质铁和一种氧化物并放出大量的热,因此铁路工人用铝来焊接钢轨,写出该反应的化学方程式:
③开发和利用清洁又高效的新能源,是21世纪人类面临的重要课题。氢气作为新能源,有很多优点,制取与储存氢气是氢能源利用领域的研究热点。Mg2Cu是一种潜在的贮氢材料,吸氢发生反应的化学方程式为2Mg2Cu+3H2
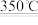 3MgH2+MgCu2.查阅资料可知:MgH2与水反应生成一种碱,并释放出H2.写出此反应的化学方程式
3MgH2+MgCu2.查阅资料可知:MgH2与水反应生成一种碱,并释放出H2.写出此反应的化学方程式(2)1926 年我国化学家侯德榜创立了“侯氏制碱法”,促进了世界制碱技术的发展,使原料NaCl的利用率由70%提高到96%,也使原来的副产物 CaCl2转化成化肥NH4Cl。“制碱” 生产过程涉及Na2CO3、NaHCO3、 NH4Cl、NaCl等物质,Na2CO3和NaCl两物质的溶解度曲线如下图所示。试回答下列问题:

①在t2 ℃时,Na2CO3的溶解度
②在t2 ℃时,分别取质量相等的Na2CO3、NaCl溶于水制成饱和溶液,降温至t1 ℃时,Na2CO3溶液的质量
③生活在盐碱湖附近的人们有一句谚语“夏天晒盐,冬天捞碱”,此处的“碱”指的是纯碱,请结合溶解度曲线,说明谚语中“冬天捞碱”的原因是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】我国是最早使用青铜器的国家之一。
I、青铜的铸造
(1)我国古代首创了“胆水炼铜”的方法,利用铁与硫酸铜溶液反应获得铜,该反应的化学方程式为______ 。
(2)商周时期,青铜文化占重要地位,青铜常被制作为武器、生产工具、生活用具等,青铜的硬度比纯铜______ (选填“大”或“小”)。
Ⅱ、青铜的锈蚀
青铜器的锈蚀产物较为复杂,一般分为有害锈和无害锈两种。无害锈可以保护青铜器,包括CuO、Cu2O、Cu2(OH)2CO3等。有害锈会加快青铜器的锈蚀速率,主要是含氯物质,如CuCl、Cu2(OH)3Cl等。
(3)Cu2(OH)2CO3的形成是青铜器与空气中的______ 共同作用的结果。
(4)将已锈蚀的青铜器浸泡在Na2CO3溶液中,可使有害锈CuCl转化为无害锈Cu2(OH)2CO3,该反应的化学方程式为: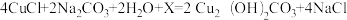 ,则气体X的化学式为
,则气体X的化学式为______ 。
现取2.22g Cu2(OH)2CO3加强热,剩余固体质量随温度变化曲线如图所示。请判断c点对应的固体物质为______ 。

I、青铜的铸造
(1)我国古代首创了“胆水炼铜”的方法,利用铁与硫酸铜溶液反应获得铜,该反应的化学方程式为
(2)商周时期,青铜文化占重要地位,青铜常被制作为武器、生产工具、生活用具等,青铜的硬度比纯铜
Ⅱ、青铜的锈蚀
青铜器的锈蚀产物较为复杂,一般分为有害锈和无害锈两种。无害锈可以保护青铜器,包括CuO、Cu2O、Cu2(OH)2CO3等。有害锈会加快青铜器的锈蚀速率,主要是含氯物质,如CuCl、Cu2(OH)3Cl等。
(3)Cu2(OH)2CO3的形成是青铜器与空气中的
(4)将已锈蚀的青铜器浸泡在Na2CO3溶液中,可使有害锈CuCl转化为无害锈Cu2(OH)2CO3,该反应的化学方程式为:
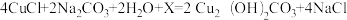 ,则气体X的化学式为
,则气体X的化学式为现取2.22g Cu2(OH)2CO3加强热,剩余固体质量随温度变化曲线如图所示。请判断c点对应的固体物质为

您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】阅读下列短文,回答问题。
三星堆遗址2021年重要考古成果:新发现6座三星堆文化“祭祀坑”,新出土重要文物1000余件,如高2.62米的青铜大立人、高3.95米的青铜神树、由金箔包裹的权杖、重约286克的金面具、玉石器、象牙、锈蚀的铁器等。

(1)青铜属于______(填字母序号)。
(2)某同学想验证铜与银的金属活动性强弱,请帮他设计一种可行的方案:______ 。
(3)“真金不怕火炼”说明______ 。
(4)铁是目前使用最广的金属,高炉炼铁主要运用了热还原法,请写出以赤铁矿为原料炼铁的化学方程式:______ 。
三星堆遗址2021年重要考古成果:新发现6座三星堆文化“祭祀坑”,新出土重要文物1000余件,如高2.62米的青铜大立人、高3.95米的青铜神树、由金箔包裹的权杖、重约286克的金面具、玉石器、象牙、锈蚀的铁器等。

(1)青铜属于______(填字母序号)。
| A.纯净物 | B.混合物 | C.化合物 |
(3)“真金不怕火炼”说明
(4)铁是目前使用最广的金属,高炉炼铁主要运用了热还原法,请写出以赤铁矿为原料炼铁的化学方程式:
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐3】对于金属材料,我们应从多角度了解。
I.金属的冶炼
(1)早在春秋战国时期,我国就开始生产和使用铁器。炼铁原理是利用一氧化碳与氧化铁在高温条件下反应,该反应的化学方程式为_______ 。现将某铁合金(只含铁和碳)8.7g放入盛有100g稀盐酸的烧杯中,恰好完全反应,得到108.1g溶液,则该样品中碳的质量分数为_______ (结果精确到0.1%)。该铁合金属于_______ (填“钢”或“生铁”)。
(2)《天工开物》中记载了炼锡的场景:“凡煎炼亦用洪炉,入砂数百斤,丛架木炭亦数百斤,鼓鞴(指鼓入空气)熔化。
①鼓入足量空气的目的是_______ ,从而提高炉温。
②“点铅勾锡”是炼锡的关键步骤,即“加铅能使锡较易熔化流出”,其原因是_______ 。
II.金属的性质
(3)铝合金与铝片相互刻画,在铝片表面会留下划痕,说明铝合金比铝硬度_______ (选填“大”或“小”)。
(4)在常温下,铝能与氧气反应,该反应的化学方程式为_______ 。
(5)汽车表面的烤漆,不仅美观还能防锈,其防锈的原理是_______ 。
(6)工人师傅切割铁板时,用硫酸铜溶液在铁板上画线,可以留下红色痕迹,产生这种现象的原因是_______ (用化学方程式表示)。
(7)为探究Fe、Zn、Cu三种金属的活动性强弱,下列选项中能达到实验目的的是_______ 。(填字母序号)
III.金属的活动性
(8)将一定量的硫酸铜溶液加入锌粉和铁粉的混合固体中,反应前后相关微粒的数量如表所示。分析可知,实验中发生反应的化学方程式是_______ 。
(9)将铜片和锡片分别伸入稀硫酸中,锡片表面有气泡生成而铜片没有,说明锡的金属活动性比铜的_______ (填“强”或“弱”)。
IV.金属资源的保护
(10)下列保护金属资源的做法正确的是_______ (填字母序号)。
I.金属的冶炼
(1)早在春秋战国时期,我国就开始生产和使用铁器。炼铁原理是利用一氧化碳与氧化铁在高温条件下反应,该反应的化学方程式为
(2)《天工开物》中记载了炼锡的场景:“凡煎炼亦用洪炉,入砂数百斤,丛架木炭亦数百斤,鼓鞴(指鼓入空气)熔化。
①鼓入足量空气的目的是
②“点铅勾锡”是炼锡的关键步骤,即“加铅能使锡较易熔化流出”,其原因是
II.金属的性质
(3)铝合金与铝片相互刻画,在铝片表面会留下划痕,说明铝合金比铝硬度
(4)在常温下,铝能与氧气反应,该反应的化学方程式为
(5)汽车表面的烤漆,不仅美观还能防锈,其防锈的原理是
(6)工人师傅切割铁板时,用硫酸铜溶液在铁板上画线,可以留下红色痕迹,产生这种现象的原因是
(7)为探究Fe、Zn、Cu三种金属的活动性强弱,下列选项中能达到实验目的的是
| A.铁、氯化锌溶液、氯化铜溶液 |
| B.铜、锌、氯化亚铁溶液 |
| C.铜、氯化锌溶液、氯化亚铁溶液 |
III.金属的活动性
(8)将一定量的硫酸铜溶液加入锌粉和铁粉的混合固体中,反应前后相关微粒的数量如表所示。分析可知,实验中发生反应的化学方程式是
| 微粒 | Zn | Fe | Cu | Cu2+ | Zn2+ |
| 反应前数量(6.02×1020个) | 100 | 100 | 0 | 100 | 0 |
| 反应后数量(6.02×1020个) | 20 | 100 | 80 | 20 | 80 |
IV.金属资源的保护
(10)下列保护金属资源的做法正确的是
| A.寻找金属代用品 | B.任意开采金属矿物 | C.回收利用废旧金属 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】现有Na、O、C、H、Fe五种元素 ,请选用其中一种或几种元素写出符合下列要求的化学式各写一个:
(1)瓦斯的主要成分_________ ;
(2)铁锈的主要成分___________ ;
(3)汽水中含有的不稳定的酸____________ ;
(4)炉具清洁剂中含有的碱是_____________ 。
(1)瓦斯的主要成分
(2)铁锈的主要成分
(3)汽水中含有的不稳定的酸
(4)炉具清洁剂中含有的碱是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】金属的研究、利用对于人类社会有着重要意义。
(l)焊锡是锡铅合金,把铅加入锡中制成合金的主要目的是________ 。
(2)铝制品表面易形成致密氧化铝薄膜,从而阻止铝进一步被空气氧化,但氧化铝能溶于酸。写出氧化铝与稀硫酸反应的化学方程式______________________________ 。
(3)在氯化铜和氯化亚铁的混合溶液中加入一定量的锌粉,充分反应后过滤,向滤出的固体中滴加稀盐酸,没有气泡产生。下列判断正确的是( )
A.滤出的固体中一定含有铜,可能含有铁和锌
B.滤出的固体一定含有铜和锌,一定不含铁
C.滤液中一定含有氯化锌和氯化亚铁,可能含有氯化铜
D.滤液中一定含有氯化锌、氯化亚铁、氯化铜
(l)焊锡是锡铅合金,把铅加入锡中制成合金的主要目的是
(2)铝制品表面易形成致密氧化铝薄膜,从而阻止铝进一步被空气氧化,但氧化铝能溶于酸。写出氧化铝与稀硫酸反应的化学方程式
(3)在氯化铜和氯化亚铁的混合溶液中加入一定量的锌粉,充分反应后过滤,向滤出的固体中滴加稀盐酸,没有气泡产生。下列判断正确的是
A.滤出的固体中一定含有铜,可能含有铁和锌
B.滤出的固体一定含有铜和锌,一定不含铁
C.滤液中一定含有氯化锌和氯化亚铁,可能含有氯化铜
D.滤液中一定含有氯化锌、氯化亚铁、氯化铜
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐3】图中A、B、C、D、E、F是八年级化学中常见的六种物质,用“—”表示两种物质间能反应,用“→”表示一种物质可以转化为另一种物质,其中A为紫红色固体(常温下),A、C、E、F均为单质,B、D都是氧化物,部分反应及转换关系已略去,请回答下列问题:_______ ;
(2)写出D转化为C的化学方程式:______________ 。
(3)写出B与E反应的实验现象:______________ 。
(4)写出F物质的一种用途:_____________ 。

(2)写出D转化为C的化学方程式:
(3)写出B与E反应的实验现象:
(4)写出F物质的一种用途:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】钢铁是使用最多的金属材料。
(1)铁制品锈蚀的过程,是铁与空气中的________________ 发生化学反应的过程。自行车的支架采取的防锈措施是__________________ ;用稀硫酸除铁锈的化学方程式为_______________________ 。
(2)用一氧化碳和赤铁矿炼铁的化学方程式为________________________________ 。回收利用废旧金属制品的目的之一是______________________________________ 。
(1)铁制品锈蚀的过程,是铁与空气中的
(2)用一氧化碳和赤铁矿炼铁的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】金属在生产和生活中具有广泛的应用。
(1)下列金属制品中,利用金属导热性的是 (填序号)。
(2)为防止铁制品锈蚀,通常在铁制品表面喷漆,其防锈原理是使铁制品与_______ 隔绝。
(3)铝的化学性质比铁活泼,但通常铝制品比铁制品更耐腐蚀的原因是______ (请用化学方程式说明)。
(1)下列金属制品中,利用金属导热性的是 (填序号)。
A. 黄金饰品 黄金饰品 | B. 铜导线 铜导线 | C. 铁炒锅 铁炒锅 |
(2)为防止铁制品锈蚀,通常在铁制品表面喷漆,其防锈原理是使铁制品与
(3)铝的化学性质比铁活泼,但通常铝制品比铁制品更耐腐蚀的原因是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】金属及金属材料广泛用于生产、生活及科学实验,其应用推动了社会的发展。
(1)铁锅用来炒菜,主要是利用铁的______ (选填“导热”或“导电”)性。
(2)生活中我们发现铁制品易生锈,防止自行车车架生锈厂家采用喷漆的方法,其防锈原理是________ 。
(3)铝合金常用作垃圾桶的内筒,其优点是________ 。
(4)同学们在实验室进行“探究金属的性质”实验。将锌粉和铁粉的混合物加入盛有一定量硝酸银溶液的烧杯中,充分反应后过滤,得到滤渣和滤液。请回答下列问题,若将所得滤渣加入稀盐酸中,有气泡产生,则:
①滤液里一定含有的溶质_______ (填化学式,下同)。
②滤渣中一定含有的成分是________ 。
(5)在质量为w克的AgNO3和Cu(NO3)2混合溶液中加入铁粉,充分反应后,溶液质量与加入铁粉的质量关系如图所示,b点的滤液中一定含有的溶质是_______ (填化学式)。

(1)铁锅用来炒菜,主要是利用铁的
(2)生活中我们发现铁制品易生锈,防止自行车车架生锈厂家采用喷漆的方法,其防锈原理是
(3)铝合金常用作垃圾桶的内筒,其优点是
(4)同学们在实验室进行“探究金属的性质”实验。将锌粉和铁粉的混合物加入盛有一定量硝酸银溶液的烧杯中,充分反应后过滤,得到滤渣和滤液。请回答下列问题,若将所得滤渣加入稀盐酸中,有气泡产生,则:
①滤液里一定含有的溶质
②滤渣中一定含有的成分是
(5)在质量为w克的AgNO3和Cu(NO3)2混合溶液中加入铁粉,充分反应后,溶液质量与加入铁粉的质量关系如图所示,b点的滤液中一定含有的溶质是

您最近一年使用:0次




