氯化钠( )和硝酸钾(
)和硝酸钾( )在不同温度时的溶解度如下表。20℃时甲乙两个烧杯中各有
)在不同温度时的溶解度如下表。20℃时甲乙两个烧杯中各有 水,分别都加入质量为m的氯化钠和硝酸钾固体,充分溶解后如图所示:
水,分别都加入质量为m的氯化钠和硝酸钾固体,充分溶解后如图所示:
_______ 。
(2)20℃时等质量的氯化钠和硝酸钾的饱和溶液中,溶剂质量较大的是_______ 溶液。
(3)20℃时将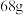 氯化钠的饱和溶液稀释成10%的溶液需加水
氯化钠的饱和溶液稀释成10%的溶液需加水_______ g。
(4)下列说法正确的是________。
 )和硝酸钾(
)和硝酸钾( )在不同温度时的溶解度如下表。20℃时甲乙两个烧杯中各有
)在不同温度时的溶解度如下表。20℃时甲乙两个烧杯中各有 水,分别都加入质量为m的氯化钠和硝酸钾固体,充分溶解后如图所示:
水,分别都加入质量为m的氯化钠和硝酸钾固体,充分溶解后如图所示:| 温度(℃) | 10 | 20 | 40 | 60 | 80 | |
| 溶解度/g |  | 20.9 | 31.6 | 63.9 | 110 | 169 |
 | 35.8 | 36 | 36.6 | 37.3 | 38.4 | |
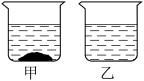
(2)20℃时等质量的氯化钠和硝酸钾的饱和溶液中,溶剂质量较大的是
(3)20℃时将
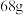 氯化钠的饱和溶液稀释成10%的溶液需加水
氯化钠的饱和溶液稀释成10%的溶液需加水(4)下列说法正确的是________。
| A.若将甲、乙烧杯中的溶液都升温到40℃,所得溶液溶质质量分数相等 |
| B.上图中烧杯乙内溶液中溶质的质量分数>烧杯甲内上层清液中溶质的质量分数 |
C.上图中若向甲烧杯中加入 水,则甲中溶质质量分数一定减小 水,则甲中溶质质量分数一定减小 |
D.60℃时,取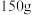 硝酸钾的不饱和溶液分别倒入两个烧杯中,第一份 硝酸钾的不饱和溶液分别倒入两个烧杯中,第一份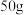 ,第二份 ,第二份 ,都恒温蒸发 ,都恒温蒸发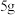 水。若第一份析出晶体 水。若第一份析出晶体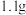 ,则第二份一定没有晶体析出 ,则第二份一定没有晶体析出 |
更新时间:2024-05-26 22:26:33
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】请根据图1甲、乙、丙三中物质的溶解度曲线,回答下列问题:
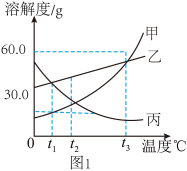
(1)在_____ ℃时,甲、丙两种物质的溶解度相等。
(2)在t3℃时,向盛有50.0g甲物质的烧杯中加入50.0g水,充分溶解后,所得溶液的质量为_____ g
(3)t1℃时,甲、乙、丙三种物质的饱和溶液各100.0g,所含溶剂的质量由大到小的顺序是_____ 。
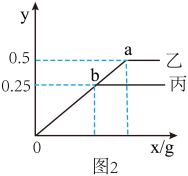
(4)在某温度下,分别向盛有等质量蒸馏水的两烧杯中逐渐加入固体溶质乙或丙,图2中x表示所加固体的质量,y表示溶液中溶质与水的质量比。下列有关说法正确的是_____。


(1)在
(2)在t3℃时,向盛有50.0g甲物质的烧杯中加入50.0g水,充分溶解后,所得溶液的质量为
(3)t1℃时,甲、乙、丙三种物质的饱和溶液各100.0g,所含溶剂的质量由大到小的顺序是
(4)在某温度下,分别向盛有等质量蒸馏水的两烧杯中逐渐加入固体溶质乙或丙,图2中x表示所加固体的质量,y表示溶液中溶质与水的质量比。下列有关说法正确的是_____。
| A.a点之前,该温度下两溶液均为不饱和溶液 |
| B.该温度时乙物质的溶解度比丙物质的溶解度大 |
| C.该温度时,乙物质的溶解度为50g |
| D.该温度时,丙饱和溶液的溶质质量分数为25% |
| E.配制一定溶质质量分数的乙物质的溶液,若量取水时俯视读数,其他操作均正确,则配制的乙溶液中溶质质量分数将偏高 |
您最近一年使用:0次
【推荐2】溶液与人们的生产生活密切相关。
(1)下列常见物质不属于溶液的是_____ (填序号)。
A 生理盐水B 糖水C 酒精D 雪碧
(2)下图是A物质的溶解度曲线,下表是B物质在不同温度时的溶解度。
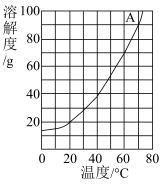
Ⅰ、60℃时,A物质的溶解度是_____ g/100g水。
Ⅱ、50℃时,向100g水中加入40gB物质,充分溶解后得到的是_____ (填“饱和”或“不饱和”)溶液,此时溶液的溶质质量分数是_____ 。
Ⅲ、请根据表格数据,在A物质溶解度曲线图中绘出B物质的溶解度曲线_____ 。
Ⅳ、A、B两种物质溶解度相同时的温度是_____ ℃。
(3)生活中常用酒精消毒液对手和皮肤进行消毒。请根据下表分析酒精浓度与杀死细菌的时间数据,下表中不同浓度的酒精溶液中最合适用于消毒的浓度应为_____ 。
(1)下列常见物质不属于溶液的是
A 生理盐水B 糖水C 酒精D 雪碧
(2)下图是A物质的溶解度曲线,下表是B物质在不同温度时的溶解度。

| 温度/℃ | B物质溶解度/g |
| 0 | 32 |
| 20 | 35 |
| 40 | 40 |
| 60 | 45 |
| 80 | 55 |
Ⅱ、50℃时,向100g水中加入40gB物质,充分溶解后得到的是
Ⅲ、请根据表格数据,在A物质溶解度曲线图中绘出B物质的溶解度曲线
Ⅳ、A、B两种物质溶解度相同时的温度是
(3)生活中常用酒精消毒液对手和皮肤进行消毒。请根据下表分析酒精浓度与杀死细菌的时间数据,下表中不同浓度的酒精溶液中最合适用于消毒的浓度应为
| 酒精浓度(%) | 大肠杆菌 | 金黄色葡萄球菌 | 溶血性链球菌 |
| 90 | 15小时 | 30分钟 | 5分钟 |
| 80 | 1小时 | 30分钟 | 5分钟 |
| 70 | 30秒 | 5分钟 | 10秒 |
| 60 | 20秒 | 30分钟 | 10秒 |
| 50 | 20秒 | 2小时 | 20秒 |
| 40 | 22分钟 | 4小时 | 2分钟 |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐3】NaCl、KNO3的部分溶解度数据见下表。
(1)60℃时,105g饱和硝酸钾溶液中的溶质质量为_______ g。
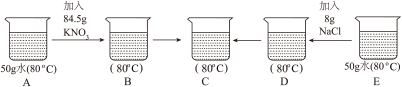
(2)按照下图步骤进行实验,充分溶解后,烧杯B和D中属于饱和溶液的是_______ 。
(3)将B、D烧杯中溶液倒入烧杯C中,从混合溶液C中提纯硝酸钾,步骤如下图:
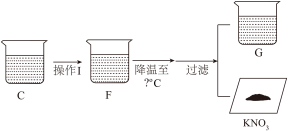
①操作I不改变溶质质量,恒温蒸发掉_______ g水,得到了硝酸钾的饱和溶液。
②过滤后,得到溶液G和68.7g硝酸钾固体,则需降温至_______ ℃。
③对整个实验过程分析正确的是_______ (填字母序号)。
A.氯化钠溶液在整个过程中溶质质量不变
B.上述方法得到的G溶液是纯净物
C.若溶液C直接降温至20℃,析出硝酸钾的质量仍为68.7g
| 温度/℃ | 10 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | KNO3 | 20.9 | 31.6 | 63.9 | 110 | 169.0 | 246 |
| NaCl | 35.8 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
(1)60℃时,105g饱和硝酸钾溶液中的溶质质量为
(2)按照下图步骤进行实验,充分溶解后,烧杯B和D中属于饱和溶液的是

(3)将B、D烧杯中溶液倒入烧杯C中,从混合溶液C中提纯硝酸钾,步骤如下图:

①操作I不改变溶质质量,恒温蒸发掉
②过滤后,得到溶液G和68.7g硝酸钾固体,则需降温至
③对整个实验过程分析正确的是
A.氯化钠溶液在整个过程中溶质质量不变
B.上述方法得到的G溶液是纯净物
C.若溶液C直接降温至20℃,析出硝酸钾的质量仍为68.7g
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】下图是硝酸钾和氯化钠的溶解度曲线。

(1)两种物质中,_______ 的溶解度受温度影响较小。
(2)t1℃时,使接近饱和的氯化钠溶液变为饱和溶液的一种方法是_______ 。
(3)t2℃时,硝酸钾饱和溶液中溶质、溶剂的质量比(最简整数比)是_______ 。
(4)硝酸钾中混有少量的氯化钠,提纯硝酸钾可采用的方法是_______ 。

(1)两种物质中,
(2)t1℃时,使接近饱和的氯化钠溶液变为饱和溶液的一种方法是
(3)t2℃时,硝酸钾饱和溶液中溶质、溶剂的质量比(最简整数比)是
(4)硝酸钾中混有少量的氯化钠,提纯硝酸钾可采用的方法是
您最近一年使用:0次
【推荐2】水与溶液在生产生活中有广泛的用途。请结合所学知识回答下列问题。
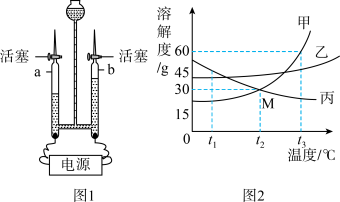
(1)如图1为实验室电解水的装置,通电一段时间后,b端玻璃管中产生的气体是_______ ,该反应的反应物与生成物间的微观粒子个数比(H2O:H2:O2)为_______ 。
(2)如图2是不含结晶水的甲、乙、丙三种固体物质的溶解度曲线。
①M点表示的含义是_______ (答一条即可)。
②t3℃时,将40g甲物质加入到50g水中,充分溶解后所得溶液的质量是______ g。
③t3℃时,将等质量的甲、乙、丙三种物质的饱和溶液分别降温至t2℃,所得溶液中溶剂最多的是____________ 。

(1)如图1为实验室电解水的装置,通电一段时间后,b端玻璃管中产生的气体是
(2)如图2是不含结晶水的甲、乙、丙三种固体物质的溶解度曲线。
①M点表示的含义是
②t3℃时,将40g甲物质加入到50g水中,充分溶解后所得溶液的质量是
③t3℃时,将等质量的甲、乙、丙三种物质的饱和溶液分别降温至t2℃,所得溶液中溶剂最多的是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐3】甲、乙两种固体物质的溶解度曲线如图1所示,请结合溶解度曲线回答下列问题。
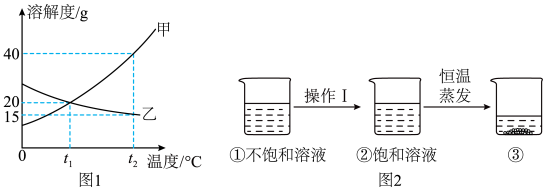
(1)降低温度可将饱和溶液变为不饱和溶液的是____ (填“甲”或“乙”)。
(2)t2℃时,将两种物质各ag分别加入到50g水中,充分溶解后,若只有一种物质能形成饱和溶液,则a的取值范围是_______ 。
(3)将t1℃时的甲、乙两种物质的饱和溶液升温至t2℃,所得溶液中溶质的质量分数甲_____ 乙(填“<”、“=”或“>”)。
(4)图2是有关甲溶液的实验操作及变化情况,下列有关说法不正确 的是 (填字母)。

(1)降低温度可将饱和溶液变为不饱和溶液的是
(2)t2℃时,将两种物质各ag分别加入到50g水中,充分溶解后,若只有一种物质能形成饱和溶液,则a的取值范围是
(3)将t1℃时的甲、乙两种物质的饱和溶液升温至t2℃,所得溶液中溶质的质量分数甲
(4)图2是有关甲溶液的实验操作及变化情况,下列有关说法
| A.①与②的溶质质量可能相等 |
| B.溶质质量分数:②>③ |
| C.若将等温度等质量的甲和乙的饱和溶液恒温蒸发等质量的水,析出的晶体质量一定是:甲>乙 |
| D.若将等温度等质量的甲和乙的饱和溶液,降低相同的温度所得溶液质量一定是:甲>乙 |
您最近一年使用:0次
【推荐1】水和溶液在生产生活中起着重要的作用。
(1)电解水实验可以得出水是由______ 组成的。
(2)天然水中含有许多杂质,现向水样中加入明矾搅拌溶解,静置一段时间后,进行过滤,过滤时需要用到的玻璃仪器有______ (填序号)。
①带铁圈的铁架台 ②酒精灯 ③漏斗 ④玻璃棒 ⑤量筒 ⑥烧杯 ⑦滤纸
(3)少量下列物质加入到水中,充分搅拌后,可以得到无色溶液的是______。
(4)Ⅰ、甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图。下列说法正确的是______。
(5)Ⅱ、硝酸钾在不同温度时的溶解度见下表:
下图A、B、C、D四个烧杯中分别盛有100g水,分别向其中加入110g、86g、64g、32g硝酸钾,充分溶解后得到40℃时的溶液。______ 中的液体是饱和溶液(选填字母)。
②表中的一组数据“20、32”的含义是______ 。
③将一瓶接近饱和的硝酸钾溶液变成饱和溶液的方法是______ (任写一种)。
④向B烧杯中加适量的水得到饱和溶液(保持40℃)的最大质量为______ g。
⑤A烧杯中溶液的溶质质量分数为______ 。
(1)电解水实验可以得出水是由
(2)天然水中含有许多杂质,现向水样中加入明矾搅拌溶解,静置一段时间后,进行过滤,过滤时需要用到的玻璃仪器有
①带铁圈的铁架台 ②酒精灯 ③漏斗 ④玻璃棒 ⑤量筒 ⑥烧杯 ⑦滤纸
(3)少量下列物质加入到水中,充分搅拌后,可以得到无色溶液的是______。
| A.植物油 | B.蔗糖 | C.乙醇 | D.高锰酸钾 |
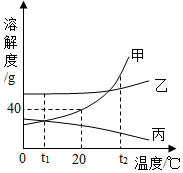
| A.t1℃时,三种物质的溶解度:乙>甲=丙 |
| B.20℃时,将30g甲放入50g水中,充分搅拌,所得溶液的质量是80g |
| C.分别将t2℃时三种物质的饱和溶液降温到t1℃,甲溶液中析出的晶体质量最大 |
| D.分别将t1℃时三种物质的饱和溶液升温到t2℃,溶液中溶质的质量分数:乙>甲>丙 |
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| 溶解度/g | 21 | 32 | 46 | 64 | 86 | 110 | 138 |
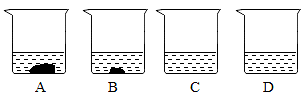
②表中的一组数据“20、32”的含义是
③将一瓶接近饱和的硝酸钾溶液变成饱和溶液的方法是
④向B烧杯中加适量的水得到饱和溶液(保持40℃)的最大质量为
⑤A烧杯中溶液的溶质质量分数为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】如图所示,是A、B、C三种固体物质的溶解度曲线,请据图回答下列问题:
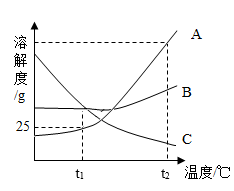
(1)t1℃时,A物质饱和溶液的溶质质量分数为___________ 。
(2)t2℃时,A 、B、C三种物质的溶解度最大的是___________ 。
(3)要从B物质的饱和溶液中得到B物质的晶体,一般采用___________ 的方法,这是因为___________ 。
(4)将t1℃时C物质的不饱和溶液,可以通过减少溶剂、增加溶质或___________ ,可使其变为饱和溶液。
(5)从t2℃降低到t1℃时,等质量的A 、B、C三种物质的饱和溶液,析出晶体最多的是___________ 物质。

(1)t1℃时,A物质饱和溶液的溶质质量分数为
(2)t2℃时,A 、B、C三种物质的溶解度最大的是
(3)要从B物质的饱和溶液中得到B物质的晶体,一般采用
(4)将t1℃时C物质的不饱和溶液,可以通过减少溶剂、增加溶质或
(5)从t2℃降低到t1℃时,等质量的A 、B、C三种物质的饱和溶液,析出晶体最多的是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐3】甲、乙两种固体物质的溶解度曲线如图1所示,请结合溶解度曲线回答下列问题。

(1)降低温度可将饱和溶液变为不饱和溶液的是____ (填“甲”或“乙”)。
(2)t2℃时,将两种物质各ag分别加入到50g水中,充分溶解后,若只有一种物质能形成饱和溶液,则a的取值范围是_______ 。
(3)将t1℃时的甲、乙两种物质的饱和溶液升温至t2℃,所得溶液中溶质的质量分数甲_____ 乙(填“<”、“=”或“>”)。
(4)图2是有关甲溶液的实验操作及变化情况,下列有关说法不正确 的是 (填字母)。

(1)降低温度可将饱和溶液变为不饱和溶液的是
(2)t2℃时,将两种物质各ag分别加入到50g水中,充分溶解后,若只有一种物质能形成饱和溶液,则a的取值范围是
(3)将t1℃时的甲、乙两种物质的饱和溶液升温至t2℃,所得溶液中溶质的质量分数甲
(4)图2是有关甲溶液的实验操作及变化情况,下列有关说法
| A.①与②的溶质质量可能相等 |
| B.溶质质量分数:②>③ |
| C.若将等温度等质量的甲和乙的饱和溶液恒温蒸发等质量的水,析出的晶体质量一定是:甲>乙 |
| D.若将等温度等质量的甲和乙的饱和溶液,降低相同的温度所得溶液质量一定是:甲>乙 |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
【推荐1】如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,回答下列问题。
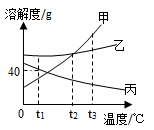
①t3℃ 时,物质甲、乙、丙的溶解度由小到大的是____ 。
②t1℃时,将25g丙加入到50g水中充分溶解后所得溶液的质量为____ 。
③甲中含有少量的乙,欲提纯甲应采用的方法是____ 。
④将100g10%的甲溶液稀释到4%需加入____ 水。
⑤t3℃时,将甲、乙、丙三种物质的饱和溶液降温至t1℃时,这时三种溶液的溶质质量分数由大到小是___________ 。

①t3℃ 时,物质甲、乙、丙的溶解度由小到大的是
②t1℃时,将25g丙加入到50g水中充分溶解后所得溶液的质量为
③甲中含有少量的乙,欲提纯甲应采用的方法是
④将100g10%的甲溶液稀释到4%需加入
⑤t3℃时,将甲、乙、丙三种物质的饱和溶液降温至t1℃时,这时三种溶液的溶质质量分数由大到小是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐2】将一瓶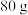 10%的氯化钠溶液分为两等份。
10%的氯化钠溶液分为两等份。
(1)每份溶液中溶质的质量分数是______ 。
(2)若将其中的一份溶质质量分数减少一半,应加水的质量是______ 。
(3)若将另一份溶液中的溶质质量分数增大一倍,应加入氯化钠的质量是______  ,或蒸发掉水的质量是
,或蒸发掉水的质量是______  。
。
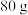 10%的氯化钠溶液分为两等份。
10%的氯化钠溶液分为两等份。(1)每份溶液中溶质的质量分数是
(2)若将其中的一份溶质质量分数减少一半,应加水的质量是
(3)若将另一份溶液中的溶质质量分数增大一倍,应加入氯化钠的质量是
 ,或蒸发掉水的质量是
,或蒸发掉水的质量是 。
。
您最近一年使用:0次
【推荐3】研究“水”可从多角度展开。
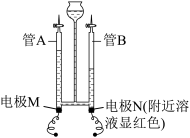
(1)认识水:某同学在水电解器中加入含酚酞的稀Na2SO4溶液(Na2SO4溶液呈中性且不参与反应),至充满管A和管B.通直流电一段时间后现象如下图所示。电解结束后将容器内所有液体倒入烧杯中,溶液呈无色。___________ (填字母)。
A.硫酸钠在水中解离出Na+和 ,可增强导电性
,可增强导电性
B.电极M与电源负极相连
C.电解过程中化学能转化为电能
D.该实验说明水是由氢、氧元素组成的
②电解过程中,电极N附近产生的微粒有___________ (填微粒符号)。理论上电解水得到氧气和氢气的体积比为1:2,某同学用碳棒作电极进行电解水实验,得到氧气和氢气的体积比小于1::2,对产生此现象原因的猜想不合理的是___________ 。
A.部分氧气溶于水
B.部分氧气与碳棒反应
C.部分氧气被碳棒吸附
D.部分氧气与氢气反应重新生成了水
(2)处理水:大多数天然淡水需要经过处理方可直接饮用。
①“生命吸管”将大运河水转变为饮用水的过程示意图如下:___________ 性。“离子交换树脂”将硬水软化的反应之一是: ,由此可知一个Ca2+可交换出
,由此可知一个Ca2+可交换出___________ (填数字)个Na+。
②废水中氨氮(以NH3形式存在)含量过高,直接排放会导致水体富营养化。次氯酸(HClO)可除去废水中的NH3发生的反应为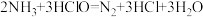 。若废水碱性过强(pH>10)。NH3的去除率会显著降低。原因是
。若废水碱性过强(pH>10)。NH3的去除率会显著降低。原因是___________ 。
(4)学校用50g20%的过氧乙酸溶液配制成0.5%的过氢乙酸溶液,需要加水___________ mL(密度为1g/cm3)。配制过氧乙酸溶液的主要步骤有:计算、___________ 、稀释、装瓶并贴标签。
(1)认识水:某同学在水电解器中加入含酚酞的稀Na2SO4溶液(Na2SO4溶液呈中性且不参与反应),至充满管A和管B.通直流电一段时间后现象如下图所示。电解结束后将容器内所有液体倒入烧杯中,溶液呈无色。
A.硫酸钠在水中解离出Na+和
 ,可增强导电性
,可增强导电性B.电极M与电源负极相连
C.电解过程中化学能转化为电能
D.该实验说明水是由氢、氧元素组成的
②电解过程中,电极N附近产生的微粒有
A.部分氧气溶于水
B.部分氧气与碳棒反应
C.部分氧气被碳棒吸附
D.部分氧气与氢气反应重新生成了水
(2)处理水:大多数天然淡水需要经过处理方可直接饮用。
①“生命吸管”将大运河水转变为饮用水的过程示意图如下:

 ,由此可知一个Ca2+可交换出
,由此可知一个Ca2+可交换出②废水中氨氮(以NH3形式存在)含量过高,直接排放会导致水体富营养化。次氯酸(HClO)可除去废水中的NH3发生的反应为
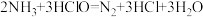 。若废水碱性过强(pH>10)。NH3的去除率会显著降低。原因是
。若废水碱性过强(pH>10)。NH3的去除率会显著降低。原因是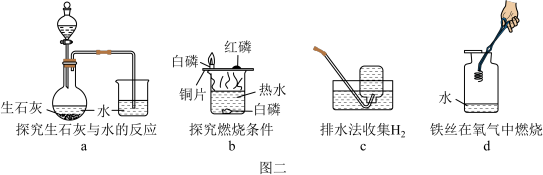
| A.a图中的水便于观察烧瓶内气压变化 |
| B.d图中的水防止熔融物炸裂集气瓶 |
| C.c图集气瓶中的水排尽空气且便于观察H2何时集满 |
| D.b图中的水提供热量 |
您最近一年使用:0次



