铝、铜、铁是生活中常见的金属
(1)用金属铜制电线主要是利用铜具有良好的_______ 。
(2)铝、铜、铁三种金属活动性由强到弱的顺序是_______ ,为了验证铝、铁、铜的金属活动性顺序,除了选择用砂纸打磨干净的铁钉外,还需要选择的药品是_______ 和_______
(3)铁在空气中容易生锈,这是因为铁和空气中的_______ 和_______ 共同作用的结果,防止铁制品锈蚀的方法有_______ (写一种即可)目前世界上已有50%以上的废钢铁得到回收利用,其目的是 _______ 。
A.节约金属资源 B.合理开采矿物 C.防止钢铁生锈
(1)用金属铜制电线主要是利用铜具有良好的
(2)铝、铜、铁三种金属活动性由强到弱的顺序是
(3)铁在空气中容易生锈,这是因为铁和空气中的
A.节约金属资源 B.合理开采矿物 C.防止钢铁生锈
更新时间:2016-11-28 12:34:07
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】人类的生活和生产都离不开金属材料。
(1)在汽车电路中,经常用铜作导线,这是利用了铜的_________ 性。
(2)铁生锈的条件是:铁与空气和__________ 直接接触,根据铁生锈的条件,自行车支架大梁采取的防锈措施是 _____________________ 。
(3)某同学为了验证镁、铁、铜的活动性顺序,他选择了打磨过的铁丝,你认为他还需要的另外两种溶液是____________ 溶液和 ______________ 溶液。请根据选定的试剂写出上述实验中发生反应的一个化学方程式 _______________________________________ 。
(4)某化学小组用一定量AgNO3和Al(NO3)3的混合溶液进行了下图实验,已知溶液甲呈蓝色。
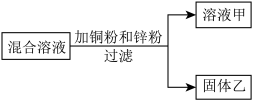
向固体乙上滴加盐酸时___________ (填“有”或“没有”)气泡产生,溶液甲中一定含有的溶质
是______________________________ (写化学式),写出一个该实验过程中所发生反应的化学方程式 _____________________________________________ 。
(1)在汽车电路中,经常用铜作导线,这是利用了铜的
(2)铁生锈的条件是:铁与空气和
(3)某同学为了验证镁、铁、铜的活动性顺序,他选择了打磨过的铁丝,你认为他还需要的另外两种溶液是
(4)某化学小组用一定量AgNO3和Al(NO3)3的混合溶液进行了下图实验,已知溶液甲呈蓝色。

向固体乙上滴加盐酸时
是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氢氧燃料电池汽车是一种真正意义上的“零排放,无污染”载运工具,是利用原电池原理,将氢气与氧气通过反应形成电流,并为电动机供电驱动车辆行驶。请回答问题:

(1)一些汽车车体采用铝合金制成,是因为铝合金与铁合金相比,其在物理性质上具有的优点是______ (填字母)。
A 抗腐蚀性好
B 密度小
C 硬度大
(2)氢氧燃料电池汽车在行驶过程中的能量转化过程是________ (用“→”表示)。
(3)工业上制取铝通常采用电解法,氧化铝在通电和催化剂条件下分解生成两种单质,请写出电解氧化铝的化学方程式________ 。
(4)氢氧燃料电池汽车相对于燃油汽车,不仅节约了________ 还减少了汽车尾气的排放。
(5)电动汽车中的导线材质都是铜。某兴趣小组同学想从铁和硫酸铜反应后的废液中回收金属铜,设计了如下方案,
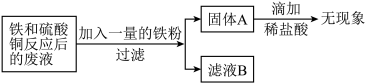
试回答:
①固体A中一定不含________ (填化学式)
②滤液B中一定含有的溶质________ (填化学式)

(1)一些汽车车体采用铝合金制成,是因为铝合金与铁合金相比,其在物理性质上具有的优点是
A 抗腐蚀性好
B 密度小
C 硬度大
(2)氢氧燃料电池汽车在行驶过程中的能量转化过程是
(3)工业上制取铝通常采用电解法,氧化铝在通电和催化剂条件下分解生成两种单质,请写出电解氧化铝的化学方程式
(4)氢氧燃料电池汽车相对于燃油汽车,不仅节约了
(5)电动汽车中的导线材质都是铜。某兴趣小组同学想从铁和硫酸铜反应后的废液中回收金属铜,设计了如下方案,

试回答:
①固体A中一定不含
②滤液B中一定含有的溶质
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】“飞翔的速度,白色的闪电,青春的光影,这就是中国速度”高铁好,高铁妙,高铁高铁呱呱叫。

(1)高铁动车车身应采用的材料可以是________ (填字母)。
A 硬度和强度好的硬铝合金
B 抗老化、弹性好的合成橡胶
C 密度小、熔点高的钛合金
(2)高铁动车属电动车组,动车行驶过程中也同时为车体内的蓄电池充电,是车厢内的用电器储备应急电能,车体内蓄电池工作时的初始能量是_________ ;工业上以纯净的氧化铝为原料在通电且熔融的冰晶石作催化剂条件下制取铝,同时生成一种气体单质,写出此过程发生的化学方程式_________ ;此变化前后化合价发生变化的元素是________ (写元素符号)。乘坐轨道交通出行既节能又环保,符合低碳生活的理念,与传统汽车相比能够减少_________ (填一种化学式)空气污染物的排放。

(1)高铁动车车身应采用的材料可以是
A 硬度和强度好的硬铝合金
B 抗老化、弹性好的合成橡胶
C 密度小、熔点高的钛合金
(2)高铁动车属电动车组,动车行驶过程中也同时为车体内的蓄电池充电,是车厢内的用电器储备应急电能,车体内蓄电池工作时的初始能量是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】一个国家的强大,不仅仅是经济实力上的强大,而拥有先进的武器,是保卫领土完整的重要保障.歼20战斗机,空军代号为“威龙”,该机担负我军未来对空、对海的主权维护.该机是由中国成都飞机工业公司制造的多用途歼击机,是我国第四代战机的主力机型.请回答下列有关问题.

(1)为了增强歼20的空中灵活性,其机体材料可以最好选用__________ ;(在A、B、C中选填)
A韧性好、硬度大的锰钢
B熔点高、密度小的钛合金
C抗腐蚀性好的不锈钢
(2)歼20火炮炮弹射出炮膛时的能量转化为__________ ;
(3)歼20工作时产生的尾气中含有一氧化氮和一氧化碳,对空气会造成污染,可在催化剂和加热的条件下转化为空气中的两种无害气体,则发生反应的化学方程式是__________ ,该反应前后氮元素的化合价变化为__________ .

(1)为了增强歼20的空中灵活性,其机体材料可以最好选用
A韧性好、硬度大的锰钢
B熔点高、密度小的钛合金
C抗腐蚀性好的不锈钢
(2)歼20火炮炮弹射出炮膛时的能量转化为
(3)歼20工作时产生的尾气中含有一氧化氮和一氧化碳,对空气会造成污染,可在催化剂和加热的条件下转化为空气中的两种无害气体,则发生反应的化学方程式是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】我国古代科技璀璨夺目,金属的冶炼与使用在当时已处于世界先进水平。
(1)日常生活中,适合制作电缆的金属是______(填标号)。
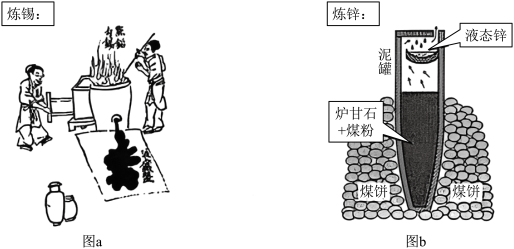
(2)明代《天工开物》描述了锡的冶炼方法,如图a。
①原料锡砂中的SnO2和木炭反应得到锡和二氧化碳,化学方程式为______ 。
②炼锡时混入少许铅形成合金,产物更易熔化流出,原因是______ 。
①泥罐外煤饼的主要作用是燃烧提供热量,泥罐内煤粉的主要作用是______ 。
②已知锌的沸点为907℃。泥罐下部温度可达1200℃,上部约为600℃,该工艺从反应混合物中收集液态锌的方法属于______ (填标号)。
A.结晶 B.蒸发 C.蒸馏 D.升华
③必须冷却后才能取锌,是为了防止发生反应:______ (写化学方程式)。
(4)湿法冶金利用置换反应。向Cu(NO3)2、AgNO3混合液中加入Fe粉,充分反应后过滤。若滤渣中有两种金属,则滤液中一定不含的金属阳离子是______ 。
(1)日常生活中,适合制作电缆的金属是______(填标号)。
| A.金 | B.铜 | C.汞 | D.钨 |
①原料锡砂中的SnO2和木炭反应得到锡和二氧化碳,化学方程式为
②炼锡时混入少许铅形成合金,产物更易熔化流出,原因是
①泥罐外煤饼的主要作用是燃烧提供热量,泥罐内煤粉的主要作用是
②已知锌的沸点为907℃。泥罐下部温度可达1200℃,上部约为600℃,该工艺从反应混合物中收集液态锌的方法属于
A.结晶 B.蒸发 C.蒸馏 D.升华
③必须冷却后才能取锌,是为了防止发生反应:
(4)湿法冶金利用置换反应。向Cu(NO3)2、AgNO3混合液中加入Fe粉,充分反应后过滤。若滤渣中有两种金属,则滤液中一定不含的金属阳离子是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】高层建筑的楼顶常装有用钢铁做的避雷针,其作用是将雷电引导到地下,这说明钢铁具有良好的__________ 性(填一物理性质)。处于楼顶的避雷针生锈了,铁生锈需要的条件是要有__________ (填名称)的参与。用盐酸除去铁锈的化学方程式为____________________ 。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】实验创新可以使现象更明显,操作更简便。Y形管的使用能增强实验的对比性,增添实验的趣味性。某化学兴趣小组同学利用Y形管设计了如图三个实验进行探究活动,请回答下列问题:
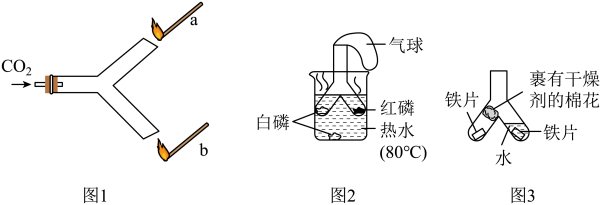
(1)如图1,向Y形管中缓慢通入二氧化碳,并在两端分别放一根燃着的木条a、b,观察到燃着的木条_______ (填“a”或“b”)先熄灭,由此得出二氧化碳的物理性质为:____________ 。
(2)如图2所示实验中(已知白磷的着火点是40℃,红磷的着火点是240℃),根据Y形管左右两侧现象对比,可得到可燃物燃烧的条件是___________ ,Y型管顶端气球的主要作用是_________ 。
(3)如图3所示实验中,一段时间后,Y形管右侧铁片生锈,由此可得出结论、__________ 是铁生锈的必要条件。下列对钢铁制品的防锈措施不合理的是_________ (填序号)。
A.在车船的表面喷涂油漆 B.将使用后的菜刀用布擦干
C.在铁制品表面镀上一层铬 D.用洗涤剂把铁制品表面的油膜洗净

(1)如图1,向Y形管中缓慢通入二氧化碳,并在两端分别放一根燃着的木条a、b,观察到燃着的木条
(2)如图2所示实验中(已知白磷的着火点是40℃,红磷的着火点是240℃),根据Y形管左右两侧现象对比,可得到可燃物燃烧的条件是
(3)如图3所示实验中,一段时间后,Y形管右侧铁片生锈,由此可得出结论、
A.在车船的表面喷涂油漆 B.将使用后的菜刀用布擦干
C.在铁制品表面镀上一层铬 D.用洗涤剂把铁制品表面的油膜洗净
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】钢铁是应用广泛的金属材料。
(1)英国学者R·坦普尔论证了我国古代冶铁技术世界第一。早在公元前4世纪,中国已广泛利用磁铁矿与木炭生产生铁,并加入“黑土”以降低生铁的熔化温度;公元前2世纪,中国人发明了“充氧”等炼钢法。
①“黑土”含有磷酸铁(FePO4),其中磷元素的化合价为_____________ 。
②生铁生产过程中,一氧化碳与氧化铁在高温下反应的化学方程式为_____________ 。
③炼钢中“充氧”的目的是降低生铁中的_____________ ,获得性能更好的钢;
(2)对钢铁制品进行“发蓝”处理,使表面生成氧化膜,能有效防止钢铁锈蚀。
①“发蓝”过程生成的氧化膜是_____________ 的(填“致密”或“疏松”)。
②铁生锈的原因是铁与空气中_____________ 接触。
(1)英国学者R·坦普尔论证了我国古代冶铁技术世界第一。早在公元前4世纪,中国已广泛利用磁铁矿与木炭生产生铁,并加入“黑土”以降低生铁的熔化温度;公元前2世纪,中国人发明了“充氧”等炼钢法。
①“黑土”含有磷酸铁(FePO4),其中磷元素的化合价为
②生铁生产过程中,一氧化碳与氧化铁在高温下反应的化学方程式为
③炼钢中“充氧”的目的是降低生铁中的
(2)对钢铁制品进行“发蓝”处理,使表面生成氧化膜,能有效防止钢铁锈蚀。
①“发蓝”过程生成的氧化膜是
②铁生锈的原因是铁与空气中
您最近一年使用:0次



