为了达到收旧利废节能减排的目的,从含有金属镁、铁、铜的粉末中,分离和提取出重要化工原料MgSO4和有关金属,实验过程如下:
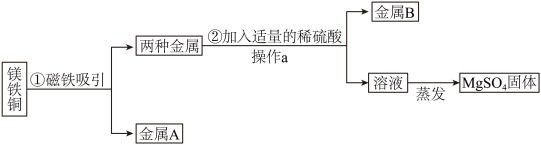
请回答:
(1)操作①中被磁铁吸引的金属A是__________ ;
(2)在蒸发过程中需要使用玻璃棒,其作用是______________________________ ;
(3)写出步骤②所涉及的化学反应方程式:___________________________________ ;
(4)实验步骤②中除了加入稀硫酸外,还可选用下列试剂__________ (填标号)。
a.硫酸铜溶液 b.氯化钠溶液 c.硝酸银溶液

请回答:
(1)操作①中被磁铁吸引的金属A是
(2)在蒸发过程中需要使用玻璃棒,其作用是
(3)写出步骤②所涉及的化学反应方程式:
(4)实验步骤②中除了加入稀硫酸外,还可选用下列试剂
a.硫酸铜溶液 b.氯化钠溶液 c.硝酸银溶液
更新时间:2016-11-28 12:59:02
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】金属是一种重要的资源,在日常生活中已得到广泛的应用。
(1)铁常制作成铁皮和铁线,因为其具有良好的________ 。
(2)将纯铝和铝合金相互刻画,纯铝上留下明显划痕,说明_______ 。
(3)据图答题:
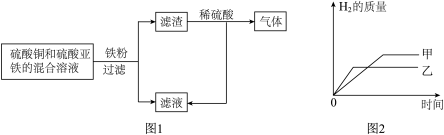
①根据如图甲所示回答:滤渣中一定有的金属是______ ,滤渣能与稀硫酸反应的化学方程式为 ______ 。
②把某稀硫酸分为等体积的两份,放入两个烧杯中,分别加入等质量的锌、铁两种金属,反应后金属都没有剩余,产生氢气的质量随反应时间变化曲线如图乙。 下列说法错误的是______ (填字母序号)
A.甲是铁,乙是锌
B.铁消耗硫酸的质量比锌大
C.如果甲中稀硫酸反应完,乙中的稀硫酸一定有剩余
D.充分反应后,稀硫酸一定都有剩余。
(4)将一定质量的 Fe 和 Zn 的混合粉末加入 AgNO3 溶液中,充分反应后过滤,得到滤渣和滤液。 若滤液呈无色,则滤渣中一定含有的金属单质是_______ 。
(1)铁常制作成铁皮和铁线,因为其具有良好的
(2)将纯铝和铝合金相互刻画,纯铝上留下明显划痕,说明
(3)据图答题:

①根据如图甲所示回答:滤渣中一定有的金属是
②把某稀硫酸分为等体积的两份,放入两个烧杯中,分别加入等质量的锌、铁两种金属,反应后金属都没有剩余,产生氢气的质量随反应时间变化曲线如图乙。 下列说法错误的是
A.甲是铁,乙是锌
B.铁消耗硫酸的质量比锌大
C.如果甲中稀硫酸反应完,乙中的稀硫酸一定有剩余
D.充分反应后,稀硫酸一定都有剩余。
(4)将一定质量的 Fe 和 Zn 的混合粉末加入 AgNO3 溶液中,充分反应后过滤,得到滤渣和滤液。 若滤液呈无色,则滤渣中一定含有的金属单质是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】金属在生活生产中有着非常广泛的应用。请回答下列问题:
(1)根据下图金属应用实例推断,金属具有的物理性质有__________ (至少答两点)。

(2)铝制品表面会形成一层致密的氧化膜,该氧化膜的成分是_____ (用化学式表示)。
(3)工业常用赤铁矿和一氧化碳在高温条件下炼铁,该反应的化学方程式为_______ 。
(4)在古代人们把烧红的生铁放在铁砧上反复捶打最终使生铁转化为钢,这就是“百炼成钢”的来历,这样做的目的是降低生铁中__________ 元素的含量。
(1)根据下图金属应用实例推断,金属具有的物理性质有

(2)铝制品表面会形成一层致密的氧化膜,该氧化膜的成分是
(3)工业常用赤铁矿和一氧化碳在高温条件下炼铁,该反应的化学方程式为
(4)在古代人们把烧红的生铁放在铁砧上反复捶打最终使生铁转化为钢,这就是“百炼成钢”的来历,这样做的目的是降低生铁中
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】日常生活中的不少用品与水银有关,体温计就是其中之一。小明偶患感冒,量体温时不小心将体温计滑落摔碎,地面上散落许多水银珠。小明想:水银有毒吗?怎样清理?经网络搜寻,小明获取以下有关水银的资料:水银学名为汞(Hg),常温下是银白色液体,密度大,受热易蒸发且吸附性特别好,不溶于水,及汞的大多数化合物有毒。在化合物中常表现为+2价,能与硫反应生成不易溶于水的无毒物质——硫化汞(HgS)。

依据以上信息,完成下面问题:
(1)小明关掉室内所有热源,这样做的目的是________________________ ;
(2)小明戴上手套以避免________________ ,用小勺把水银收集到盛有水的玻璃瓶中,送交实验室。
(3)小明从实验室带回了硫磺粉,他向不易收集的细小水银珠布上撒硫磺粉降低危害,他的依据是_________________________________ (用化学方程式表示).

依据以上信息,完成下面问题:
(1)小明关掉室内所有热源,这样做的目的是
(2)小明戴上手套以避免
(3)小明从实验室带回了硫磺粉,他向不易收集的细小水银珠布上撒硫磺粉降低危害,他的依据是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】如图甲是A、B、C三种固体物质的溶解度曲线图。

(1)甲图中,P点所表示的含义为______ 。
(2)t2℃时,当A中混有少量的B时,可用______ 方法提纯A。
(3)如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5L稀盐酸,立即产生大量的气泡,同时烧杯中出现浑浊,则X可能为A、B、C三种固体物质中的哪一种?______ ;原因是______ 。

(1)甲图中,P点所表示的含义为
(2)t2℃时,当A中混有少量的B时,可用
(3)如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5L稀盐酸,立即产生大量的气泡,同时烧杯中出现浑浊,则X可能为A、B、C三种固体物质中的哪一种?
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】化学是一门研究物质、创造物质的学科。
(1)“沉睡三千年,一醒惊天下”。2021年3月20日,三星堆考古发掘出大量黄金制品和青铜器。判断该黄金制品是真金的方法是______ 。三星堆青铜器是古代青铜器的代表。青铜,是铜、锡、铅按一定比例熔炼出的合金。青铜的强度和硬度比纯铜的______ (填“高”或“低”)。
(2)同学们在探究金属性质实验后,得到含ZnCl2、HCl和CuCl2的废液,为回收金属铜,对废液的处理设计了如图所示方案,请回答下列问题。
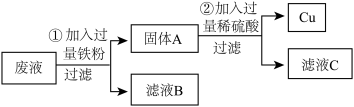
I、写出步骤①中发生反应的一个化学方程式______ 。溶液中的现象是______ 。
II、步骤②中能说明Fe的金属活动性比Cu强的现象是______ ,滤液B中溶质有______ 。
III、为了避免废液对环境的污染,并要使滤液B、C中溶质为同一物质,则对原实验方案应进行的调整是______ 。
(1)“沉睡三千年,一醒惊天下”。2021年3月20日,三星堆考古发掘出大量黄金制品和青铜器。判断该黄金制品是真金的方法是
(2)同学们在探究金属性质实验后,得到含ZnCl2、HCl和CuCl2的废液,为回收金属铜,对废液的处理设计了如图所示方案,请回答下列问题。

I、写出步骤①中发生反应的一个化学方程式
II、步骤②中能说明Fe的金属活动性比Cu强的现象是
III、为了避免废液对环境的污染,并要使滤液B、C中溶质为同一物质,则对原实验方案应进行的调整是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】黄铜是Zn以主要添加元素的铜合金。黄铜渣中约含Zn 7%、ZnO 31%、Cu50% CuO5%,其余为杂质。处理黄铜渣可得到硫酸锌,其主要流程如下(杂质不溶于水、不参与反应) :
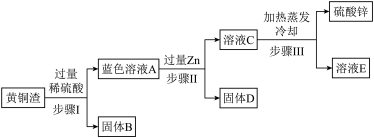
(1)步骤I中产生气体的化学反应属于____________ 反应(填基本类型)。
(2)溶液A中的金属阳离子有____________ (填离子符号)。
(3)步骤I、II中均包含的操作名称为____________ ,此操作和步骤III中的蒸发操作都要用到的玻璃仪器是______________ 。
(4)溶液A__________ (填“大于”、“小于”或“等于”)溶液C的质量。原因____________ 。

(1)步骤I中产生气体的化学反应属于
(2)溶液A中的金属阳离子有
(3)步骤I、II中均包含的操作名称为
(4)溶液A
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
【推荐1】今年5月5日,我国国产大型客机C919在上海浦东国际机场首飞成功,C919大型客机的研制,实现了以第三代铝锂合金、复合材料为代表的先进材料首次在国产民机上大规模应用.请回答:
(1)铝可制成蒸锅,这是利用铝的______ 性和延展性,这属于铝的______ (填“物理”或“化学”)性质
(2)铝具有很好的抗腐蚀性,是因为铝在空气中与_____ (填物质名称)反应,在其表面生成一层致密的氧化膜,从而阻止铝进一步氧化
(3)纯金属铝太软,当在铝中加入少量的锂(Li)等金属熔成合金,这样既轻便,又能增强它的__________ 和抗腐蚀性.
(4)锂-氯化银电池的电池反应为:Li+AgCl=LiCl+Ag,可知Li的金属活动性比Ag的_____ (填“强”或“弱”)
(1)铝可制成蒸锅,这是利用铝的
(2)铝具有很好的抗腐蚀性,是因为铝在空气中与
(3)纯金属铝太软,当在铝中加入少量的锂(Li)等金属熔成合金,这样既轻便,又能增强它的
(4)锂-氯化银电池的电池反应为:Li+AgCl=LiCl+Ag,可知Li的金属活动性比Ag的
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】将适量的铜粉和镁粉的混合物放入一定量的硝酸银溶液中,充分反应后过滤,得到固体物质和无色滤液,则滤出的固体中一定含有___________ 。古籍记载:“曾青得铁则化为铜”(曾青指硫酸铜溶液),该反应的化学方程式为___________ 。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】金属材料在生活、生产和科学研究中有着广泛的应用。
(1)用铜作导线是利用其有良好的______ 性。用青铜(铜锡合金)制机器零件不易变形,是因为青铜的硬度比纯铜的______ (填“大”或“小”)。
(2)氢化镁(MgH2)是一种贮氢合金,当它与水混合时释放出最轻的气体,同时生成一种碱,该反应的化学方程式是______ 。
(3)某化学兴趣小组将一定质量的锌粉加入硝酸银和硝酸铜的混合溶液中,充分反应后过滤,向滤渣中加入盐酸无气泡产生。
①一定发生反应的化学方程式为______ 。
②关于滤渣和滤液成分的判断,下列叙述中正确的是______ 。(填序号)
A.滤渣中一定含有银,一定不含铜
B.滤液中一定含有硝酸锌,一定不含有硝酸银
C.若滤液呈蓝色,则滤液中的溶质一定含有硝酸铜和硝酸锌
D.若滤液呈无色,则滤渣中一定含有银和铜,滤液中的溶质一定只含硝酸锌
(1)用铜作导线是利用其有良好的
(2)氢化镁(MgH2)是一种贮氢合金,当它与水混合时释放出最轻的气体,同时生成一种碱,该反应的化学方程式是
(3)某化学兴趣小组将一定质量的锌粉加入硝酸银和硝酸铜的混合溶液中,充分反应后过滤,向滤渣中加入盐酸无气泡产生。
①一定发生反应的化学方程式为
②关于滤渣和滤液成分的判断,下列叙述中正确的是
A.滤渣中一定含有银,一定不含铜
B.滤液中一定含有硝酸锌,一定不含有硝酸银
C.若滤液呈蓝色,则滤液中的溶质一定含有硝酸铜和硝酸锌
D.若滤液呈无色,则滤渣中一定含有银和铜,滤液中的溶质一定只含硝酸锌
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐1】医用氯化钙常用于合成药物。以工业碳酸钙(含少量Fe3+等杂质)为原料生产二水合氯化钙(CaCl2·2H2O)的流程图如下所示。
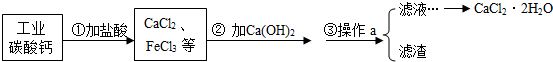
(1)写出第①步中碳酸钙与盐酸反应的化学方程式:_____ 。
(2)第②步中是否发生化学变化?_____ (填“是”或“否”)。
(3)操作a的名称是_____ ,实验室进行该操作时玻璃棒的作用是_____ 。
(4)青少年正处于生长发育阶段,需要摄入足够的钙,写出一种合理的补钙方法:_____ 。
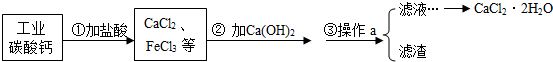
(1)写出第①步中碳酸钙与盐酸反应的化学方程式:
(2)第②步中是否发生化学变化?
(3)操作a的名称是
(4)青少年正处于生长发育阶段,需要摄入足够的钙,写出一种合理的补钙方法:
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】以镁矿石(主要成分 MgCO3、SiO2)为原料生产 MgO 的工艺流程如下:
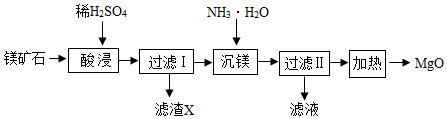
注SiO2难溶于水和常见的酸;“沉镁”过程中有 Mg(OH)2生成。
(1)滤渣 X 的主要成分为_____ (填化学式)。
(2)实验室中用图 1 所示装置进行过滤。
①该装置中玻璃棒的作用是_____ 。
②若过滤时滤液出现浑浊,可能的原因是_____ 。
(3)沉镁时 MgSO4与 NH3·H2O 发生反应,写出该反应的化学方程式_____ 。
(4)已知在不同温度下,充分加热等质量的 Mg(OH)2,加热温度与固体残留率的关系如图2。加热时温度至少要达到 350℃,原因是_____ 。


注SiO2难溶于水和常见的酸;“沉镁”过程中有 Mg(OH)2生成。
(1)滤渣 X 的主要成分为
(2)实验室中用图 1 所示装置进行过滤。
①该装置中玻璃棒的作用是
②若过滤时滤液出现浑浊,可能的原因是
(3)沉镁时 MgSO4与 NH3·H2O 发生反应,写出该反应的化学方程式
(4)已知在不同温度下,充分加热等质量的 Mg(OH)2,加热温度与固体残留率的关系如图2。加热时温度至少要达到 350℃,原因是

您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐3】能源、环境与人类的生活和社会发展密切相关,煤是社会生产、生活中最重要的能源,其主要成分是碳,还含有疏,直接燃烧煤容易导致酸雨等环境问题,工业上常把煤进行气化和液化处理,使煤变成清洁能源,减少对空气的污染.煤气化和液化流程示意图如下

(1)煤属于_________ (填“可再生”或“不可再生”)能源,它燃烧提供热量的主要反应方程式是_____________ ;
(2)第①步操作原理与化学实验操作_________ (填写实验操作名称)原理一样,实验室进行此操作时玻璃棒的作用是_____________ ;
(3)第②步是精炼煤与水蒸气在高温条件下制得水煤气,其反应的化学方程式为_______________ ,此反应属___________ 反应(填基本反应类型);
(4)硫酸中所含的原子团的符号为___________ ;己知X是氧化物,其中硫元素的化合价与硫酸中硫元素化合价相同,则X的名称为___________ 。

(1)煤属于
(2)第①步操作原理与化学实验操作
(3)第②步是精炼煤与水蒸气在高温条件下制得水煤气,其反应的化学方程式为
(4)硫酸中所含的原子团的符号为
您最近一年使用:0次



