Ⅰ.质量守恒定律的发现对化学的发展做出了重要贡献。
(1)通过称量下列各组试剂在密闭容器内混合前后的总质量,能验证质量守恒定律的是____________ (填数字序号)。
① 食盐和水 ② 氯化钠溶液和硝酸钾溶液 ③ 铁和氯化铜溶液
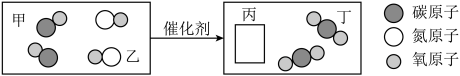
(2)某反应的微观示意图如下图所示:

① A的化学式为_________ 。
② 该反应所属的基本反应类型为_________ 反应。
③ 参加反应的A物质和生成的C物质分子数目比为________ 。
Ⅱ.甲和乙两种固态物质的饱和溶液中溶质质量分数与温度的关系如右图所示:
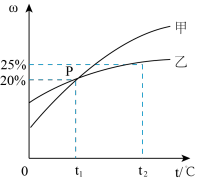
(1)甲和乙两种物质的溶解度随温度的升高而___________ (填“增大”或“减小”)。
(2)下列对P点的含义叙述正确的是________ (填字母序号)。
A.t1℃时,甲和乙两种物质的溶解度相等
B.t1℃时,甲和乙两种物质溶液的溶质质量分数相等
C.t1℃时,甲和乙两种物质的饱和溶液中溶质的质量相等
(3)25 g乙物质完全溶于100g水中所需的最低温度是________ ℃。
(4)t2℃时,若甲和乙两种物质的饱和溶液中析出等量的固体须蒸发掉较多水的是_________ (填“甲”或“乙”)物质饱和溶液。
(1)通过称量下列各组试剂在密闭容器内混合前后的总质量,能验证质量守恒定律的是
① 食盐和水 ② 氯化钠溶液和硝酸钾溶液 ③ 铁和氯化铜溶液
(2)某反应的微观示意图如下图所示:

① A的化学式为
② 该反应所属的基本反应类型为
③ 参加反应的A物质和生成的C物质分子数目比为
Ⅱ.甲和乙两种固态物质的饱和溶液中溶质质量分数与温度的关系如右图所示:

(1)甲和乙两种物质的溶解度随温度的升高而
(2)下列对P点的含义叙述正确的是
A.t1℃时,甲和乙两种物质的溶解度相等
B.t1℃时,甲和乙两种物质溶液的溶质质量分数相等
C.t1℃时,甲和乙两种物质的饱和溶液中溶质的质量相等
(3)25 g乙物质完全溶于100g水中所需的最低温度是
(4)t2℃时,若甲和乙两种物质的饱和溶液中析出等量的固体须蒸发掉较多水的是
更新时间:2017/03/25 21:29:44
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】建立正确微粒观可以更好的理解化学问题,下图是某化学变化的微粒图,请认真观察、理解并回答问题:
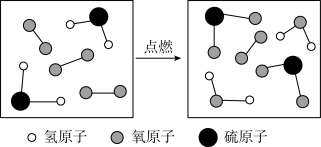
(1)化学反应后有剩余的微粒的是______ (填化学式)。
(2)是否有单质生成______ (填“有”或“没有”)。
(3)由以上变化过程从微观角度总结一个结论:______ 。
(4)写出该变化过程化学方程式______ 。

(1)化学反应后有剩余的微粒的是
(2)是否有单质生成
(3)由以上变化过程从微观角度总结一个结论:
(4)写出该变化过程化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】下图是氯气和水反应的微观示意图。
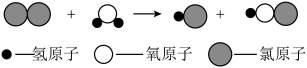
(1)图中共有______ 种化合物;共涉及到_______ 种元素;
(2)保持水的化学性质的最小粒子是_________ (填名称);
(3)参加反应的氯气和水的粒子个数比是_________ ;
(4)该反应的化学方程式为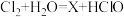 ,则X的化学式为
,则X的化学式为________ 。

(1)图中共有
(2)保持水的化学性质的最小粒子是
(3)参加反应的氯气和水的粒子个数比是
(4)该反应的化学方程式为
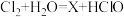 ,则X的化学式为
,则X的化学式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】微观—宏观—符号”三重表征是化学独特的表示方法,如图是某密闭容器中物质变化过程的微观示意图。请回答:
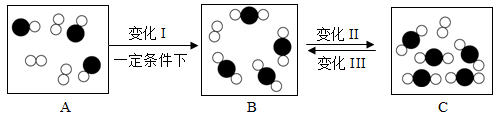
(1)A、B、C中属于混合物的是___________ (填序号)。
(2)关于上述变化Ⅰ、Ⅱ和Ⅲ的说法中,正确的是___________ (填序号)。
A 变化Ⅰ发生的是置换反应,变化Ⅱ和Ⅲ发生的是物理变化
B 变化Ⅲ发生的条件可能是升高温度
C 变化Ⅰ可能表示的是一氧化碳燃烧
D 变化Ⅰ中参加反应的 和
和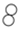 两种分子个数比为3:2
两种分子个数比为3:2
(3)若“●”代表碳原子,请画出碳原子的结构示意图___________ 。

(1)A、B、C中属于混合物的是
(2)关于上述变化Ⅰ、Ⅱ和Ⅲ的说法中,正确的是
A 变化Ⅰ发生的是置换反应,变化Ⅱ和Ⅲ发生的是物理变化
B 变化Ⅲ发生的条件可能是升高温度
C 变化Ⅰ可能表示的是一氧化碳燃烧
D 变化Ⅰ中参加反应的
 和
和 两种分子个数比为3:2
两种分子个数比为3:2(3)若“●”代表碳原子,请画出碳原子的结构示意图
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】我国研究人员研制出一种新型复合光催化剂,利用太阳光实现高效分解水,其主要过程如图所示。______ 。
(2)整个过程中数目保持不变的微粒是______ (填微粒符号)。
(3)写出整个过程的总反应化学方程式______ 。
(4)与电解水法相比,该方法最显著的优点是______ 。
(5)反应中的新型复合光催化剂经烘干后可以直接反复使用,其原因是______ 。

(2)整个过程中数目保持不变的微粒是
(3)写出整个过程的总反应化学方程式
(4)与电解水法相比,该方法最显著的优点是
(5)反应中的新型复合光催化剂经烘干后可以直接反复使用,其原因是
您最近一年使用:0次
【推荐2】图1是碘元素在元素周期表中的信息及其原子结构示意图;图2是某化学反应的微观示意图。请回答下列问题。
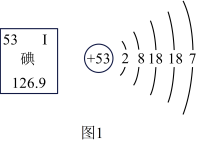

(1)碘有“智力元素”之称,处于元素周期表的第___________ 周期,碘原子核内质子数为________ 。
(2)图2中反应前后化合价发生改变的元素是___________ 。该反应中属于化合物的有___________ 种。两种反应物的分子个数比为___________ 。


(1)碘有“智力元素”之称,处于元素周期表的第
(2)图2中反应前后化合价发生改变的元素是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】根据图中A、B、C三种固体的溶解度曲线回答:
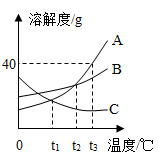
(1)在某一温度时,A、B两饱和溶液的溶质质量分数相等,此温度为_________ ℃;
(2)在t3℃时,将30gA物质充分溶解在50g水中,所得溶液的质量为__________ g;
(3)要使C的饱和溶液变为不饱和溶液,可采用的一种方法是__________ ;
(4)将t3℃的A、B、C三种物质的饱和溶液分别降温到t1℃时,所得溶液的溶质质量分数由大到小的顺序是__________ 。

(1)在某一温度时,A、B两饱和溶液的溶质质量分数相等,此温度为
(2)在t3℃时,将30gA物质充分溶解在50g水中,所得溶液的质量为
(3)要使C的饱和溶液变为不饱和溶液,可采用的一种方法是
(4)将t3℃的A、B、C三种物质的饱和溶液分别降温到t1℃时,所得溶液的溶质质量分数由大到小的顺序是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】KNO3是一种重要的化工原料。
(1)《天工开物》记载“凡研硝(KNO3)不以铁碾入石臼,相激火生,祸不可测”。是指硝酸钾性质不稳定,受到撞击会分解生成一种可助燃的气体_______ 。(填化学式)
(2)查得资料:古代曾用硝土(含有Ca(NO3)2、少量NaCl等)和草木灰(含有K2CO3)作原料制取KNO3。某化学兴趣小组据此设计了如图1实验流程:_______ 。
②若在实验室开展过滤操作,下列玻璃仪器无需用到的是_______ (选填字母)。_______ 。
④若要用制得的硝酸钾晶体配制40℃的硝酸钾饱和溶液330g,则至少需要硝酸钾固体_______ g。
(1)《天工开物》记载“凡研硝(KNO3)不以铁碾入石臼,相激火生,祸不可测”。是指硝酸钾性质不稳定,受到撞击会分解生成一种可助燃的气体
(2)查得资料:古代曾用硝土(含有Ca(NO3)2、少量NaCl等)和草木灰(含有K2CO3)作原料制取KNO3。某化学兴趣小组据此设计了如图1实验流程:
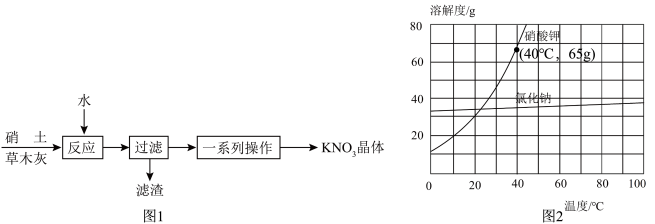
②若在实验室开展过滤操作,下列玻璃仪器无需用到的是
A.  B.
B. 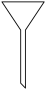 C.
C. 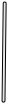 D.
D. 
④若要用制得的硝酸钾晶体配制40℃的硝酸钾饱和溶液330g,则至少需要硝酸钾固体
您最近一年使用:0次
【推荐3】下图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题:

(1)P点表示的意义是______ 。
(2)t3℃时,甲、乙、丙三种物质的溶解度由小到大的顺序为______ 。
(3)三种物质中,______ 的溶解度受温度的影响最小,______ 的溶解度随温度的升高而减小。
(4)t2℃时,将15 g甲物质溶解于50 g水中,所得到的溶液质量为______ g。
(5)t3℃时,等质量的三种饱和溶液中溶剂质量最少的是______ 。
(6)要使接近饱和的甲溶液变成饱和溶液,可采用的方法有______ (写一种)。

(1)P点表示的意义是
(2)t3℃时,甲、乙、丙三种物质的溶解度由小到大的顺序为
(3)三种物质中,
(4)t2℃时,将15 g甲物质溶解于50 g水中,所得到的溶液质量为
(5)t3℃时,等质量的三种饱和溶液中溶剂质量最少的是
(6)要使接近饱和的甲溶液变成饱和溶液,可采用的方法有
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐1】以石灰浆为原料制备KClO3的流程如图:
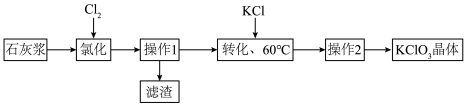
(1)过程中用石灰浆而不用石灰水的原因是______ 。
(2)“氯化”反应为6Ca(OH)2+6Cl2=Ca(ClO3)2+5X+6H2O.则X的化学式为______ 。为提高Cl2转化率,可行措施有 ______ (填序号)。
A适当减缓通入Cl2速率 B充分搅拌浆料 C加水使Ca(OH)2完全溶解
(3)如表是60℃时相关物质的溶解度。
转化时加入稍过量KCl固体可将Ca(ClO3)2转化为KClO3,原因是______ 。

(1)过程中用石灰浆而不用石灰水的原因是
(2)“氯化”反应为6Ca(OH)2+6Cl2=Ca(ClO3)2+5X+6H2O.则X的化学式为
A适当减缓通入Cl2速率 B充分搅拌浆料 C加水使Ca(OH)2完全溶解
(3)如表是60℃时相关物质的溶解度。
| 物质 | KCl | KClO3 | Ca(ClO3)2 | CaCl2 |
| 溶解度 | 43 | 24 | 62 | 70 |
转化时加入稍过量KCl固体可将Ca(ClO3)2转化为KClO3,原因是
您最近一年使用:0次
【推荐2】福建海盐的开采历史悠久;
(1)《天工开物·作咸》记载了“煎盐”技术:“凡煎盐锅古谓之‘牢盆’……南海有编竹为者,将竹编成阔丈深尺,糊以‘蜃灰’,附于釜背,火燃釜底,滚沸延及成盐……”,“牢盆”、蒸发结晶装置和氯化钠的溶解度曲线如下图所示,请和小组同学一起研究。________ (填仪器名称);
②“蜃灰”指的是蛤蜊壳(主要成分是 )烧成的“灰”,“蜃灰”的主要成分是
)烧成的“灰”,“蜃灰”的主要成分是________ (填化学式);
③结合图3分析,该“煎盐”技术不采用降温结晶的原因是________ ;析出晶体后,“牢盆”中剩余液体是 的
的________ (填“饱和”或“不饱和”)溶液;
(2)明代《兴化府志·货殖志》记载:“天下盐皆烹煎,独莆盐用晒法”,即“晒盐”法是莆田独创;
①相比“煎盐”,从能源利用角度分析“晒盐”的优点是________ ;
②海水中 含量为
含量为 ,则
,则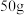 海水最多能晒出
海水最多能晒出________ g的 。
。
(1)《天工开物·作咸》记载了“煎盐”技术:“凡煎盐锅古谓之‘牢盆’……南海有编竹为者,将竹编成阔丈深尺,糊以‘蜃灰’,附于釜背,火燃釜底,滚沸延及成盐……”,“牢盆”、蒸发结晶装置和氯化钠的溶解度曲线如下图所示,请和小组同学一起研究。
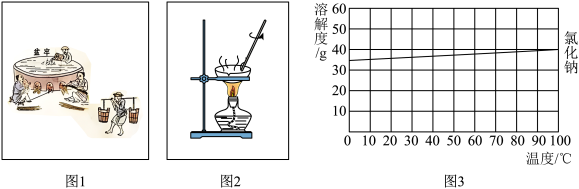
②“蜃灰”指的是蛤蜊壳(主要成分是
 )烧成的“灰”,“蜃灰”的主要成分是
)烧成的“灰”,“蜃灰”的主要成分是③结合图3分析,该“煎盐”技术不采用降温结晶的原因是
 的
的(2)明代《兴化府志·货殖志》记载:“天下盐皆烹煎,独莆盐用晒法”,即“晒盐”法是莆田独创;
①相比“煎盐”,从能源利用角度分析“晒盐”的优点是
②海水中
 含量为
含量为 ,则
,则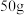 海水最多能晒出
海水最多能晒出 。
。
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】许多工厂未做处理直接将含铜废液、废渣等排放,既污染环境又浪费资源。一种从含铜废液[主要成分为CuCl2、FeCl2、CuSO4、Al2(SO4)3]中提取硫酸铜的工艺流程如图所示:

(1)反应器中充分反应后,排出的尾液的主要成分是_____ (写化学式)。
(2)净化器的主要目的是除去其中的杂质金属,加入的除杂试剂可能是_____ 。
(3)酸浸槽中发生反应的化学方程式为______ 。
(4)在结晶槽中冷却结晶得到硫酸铜,可知硫酸铜的溶解度随温度升高而_____ (填“增大”或“减小”)。
(5)酸浸槽中,不同浸出温度下铜的转化率变化如图所示,结合曲线分析在实际生产中如何设置反应条件,能使铜的转化率更高_____ 。


(1)反应器中充分反应后,排出的尾液的主要成分是
(2)净化器的主要目的是除去其中的杂质金属,加入的除杂试剂可能是
(3)酸浸槽中发生反应的化学方程式为
(4)在结晶槽中冷却结晶得到硫酸铜,可知硫酸铜的溶解度随温度升高而
(5)酸浸槽中,不同浸出温度下铜的转化率变化如图所示,结合曲线分析在实际生产中如何设置反应条件,能使铜的转化率更高

您最近一年使用:0次