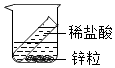
某同学用如图装置验证质量守恒定律.试管中盛有10g的稀盐酸,烧杯中加入一定量锌粒.使用电子天平称量反应前装置总质量为252.50g,将试管中的盐酸全部倒入烧杯中,充分反应后,烧杯底部仍有剩余固体,称量装置总质量为252.48g,发现质量减轻了.
(1)反思实验结论,由此可知,有气体参加或生成的化学反应,在验证质量守恒定律时,实验必须在__________的条件下进行.
(2)请根据题中信息计算稀盐酸的溶质质量分数_______.

(1)反思实验结论,由此可知,有气体参加或生成的化学反应,在验证质量守恒定律时,实验必须在__________的条件下进行.
(2)请根据题中信息计算稀盐酸的溶质质量分数_______.
2017·陕西·模拟预测 查看更多[3]
(已下线)【万唯原创】2018年陕西省中考化学试题研究卷九年级讲解册题型研究题型七(已下线)【万唯原创】2018年陕西省中考化学面对面卷九年级讲解册重点题型攻略题型五陕西省陕西师范大学附属中学2017届九年级中考五模化学试题
更新时间:2018-11-15 15:38:04
|
相似题推荐
【推荐1】用“化学的视角”认识身边的物质。
(1)水和溶液在生活、生产及航天事业中具有广泛的用途。如图1为核心舱环控生保半封闭系统工作原理示意图。请分析过程,回答下列问题。

①从微观角度分析液态水与气态水的区别是_________ 。
②通过环控生保系统得到的饮用水为软水。生活中常用__________ 区分硬水和软水。
③早期空间站内二氧化碳可用超氧化钾(KO2)吸收,生成碳酸钾和氧气,该反应的化学方程式是__________ 。
(2)图2甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:
①若甲物质中混有少量乙物质,最好采用___________ (选填“降温结晶”或“蒸发结晶”)的方法提纯甲。
②t1℃时,甲、乙、丙三种物质的饱和溶液同时升温至t2℃,所得溶液中溶质质量分数由大到小的顺序为_________ 。
(3)下列是初中化学常见的实验,请回答下列问题。

①图一中在集气瓶底部加入少量水的作用是__________ 。
②图二中可观察到干燥的紫色石蕊试纸不变色,湿润的紫色石蕊试纸变红,说明CO2具有的性质是__________ 。
③某同学用图三实验装置直接来验证质量守恒定律不成功,原因是__________ 。
(1)水和溶液在生活、生产及航天事业中具有广泛的用途。如图1为核心舱环控生保半封闭系统工作原理示意图。请分析过程,回答下列问题。

①从微观角度分析液态水与气态水的区别是
②通过环控生保系统得到的饮用水为软水。生活中常用
③早期空间站内二氧化碳可用超氧化钾(KO2)吸收,生成碳酸钾和氧气,该反应的化学方程式是
(2)图2甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:
①若甲物质中混有少量乙物质,最好采用
②t1℃时,甲、乙、丙三种物质的饱和溶液同时升温至t2℃,所得溶液中溶质质量分数由大到小的顺序为
(3)下列是初中化学常见的实验,请回答下列问题。

①图一中在集气瓶底部加入少量水的作用是
②图二中可观察到干燥的紫色石蕊试纸不变色,湿润的紫色石蕊试纸变红,说明CO2具有的性质是
③某同学用图三实验装置直接来验证质量守恒定律不成功,原因是
您最近一年使用:0次
综合应用题
|
较易
(0.85)
解题方法
【推荐1】回答问题:
(1)国人在庆生、婚嫁、老人祝寿等一些喜庆的场合,喜欢买金银饰品相赠,除了考虑价格和美观的因素外,从金属的化学性质角度考虑,主要是因为金银的化学性质比较______ (选填“稳定”或“活泼”)。
(2)在实验室做完铁、银金属活泼性探究的实验后,溶液中含有较多的Fe(NO3)2、AgNO3,小陶同学想从废液中回收金属银,向1000g的废液中加入过量的铁粉并充分反应后,再过滤、洗涤、烘干,得到的滤渣中一定含有______ (填化学式)。
(3)为了得到纯净的金属银,分离杂质可用一个简单的物理方法,用______ 即可。
(4)小陶同学最终一共回收了21.6g的金属银,请问原1000g废液中硝酸银的溶质质量分数是多少?相对原子质量:N-14,O-16,Ag-108(写出计算过程)
(1)国人在庆生、婚嫁、老人祝寿等一些喜庆的场合,喜欢买金银饰品相赠,除了考虑价格和美观的因素外,从金属的化学性质角度考虑,主要是因为金银的化学性质比较
(2)在实验室做完铁、银金属活泼性探究的实验后,溶液中含有较多的Fe(NO3)2、AgNO3,小陶同学想从废液中回收金属银,向1000g的废液中加入过量的铁粉并充分反应后,再过滤、洗涤、烘干,得到的滤渣中一定含有
(3)为了得到纯净的金属银,分离杂质可用一个简单的物理方法,用
(4)小陶同学最终一共回收了21.6g的金属银,请问原1000g废液中硝酸银的溶质质量分数是多少?相对原子质量:N-14,O-16,Ag-108(写出计算过程)
您最近一年使用:0次
综合应用题
|
较易
(0.85)
解题方法
【推荐2】每当夏季来临,泳池就成为了炙手可热的休闲和避暑的场所。化学兴趣小组对游泳池内水质净化杀菌产生好奇。
(1)游泳馆要求我们在一个浅水池内对拖鞋和脚进行消毒,浅水池中的水呈紫红色,该池中起消毒作用的物质可能是_______ 。
活动一:偏爱游泳馆的人都知道,游泳池的水经常呈现淡淡的蓝色。他们对池水呈现蓝色的原因、溶质成分、池水处理方法和对环境的影响,展开了实验探究。
实验探究1:寻找池水呈现蓝色的原因。
【查阅资料】水吸收红色波段光反射蓝色波段光引起池水呈现蓝色,当水深到1-2米深度后才呈现出蓝色,且水越深蓝色越深。
【交流讨论】分别取一杯海水和泳池水观察:海水是无色,而泳池水依然显蓝色。有同学质疑:池水呈现蓝色可能加入了铜离子。
实验探究2:检验泳池水中是否含有铜离子。
(2)取少量池水于试管中,滴加几滴氢氧化钠溶液,有______ 证明池水中含有Cu2+。
【实验调查】同学们咨询了泳馆的管理人员得知,池水中加入硫酸铜起到抑制藻类繁殖等作用。
(3)请你再设计一种方法证明铜离子的存在_______ (写出操作、现象和结论)。
活动二:设计泳池水净化模拟实验装置。
(4)为确保游泳池的水质达到国际泳联最新卫生标准,将采用“砂滤—臭氧—活性炭”净水工艺净化游泳池里的水,下列有关说法错误的是______。
活动三:解谜里约夏季奥运会“碧池”(清澈湛蓝的游泳池水,一夜之间变成浑浊的碧绿色),场馆人员的解释是:工作人员误将80L过氧化氢溶液倾倒入池中消毒,氯气和过氧化氢产生氧气和另一化合物,导致水体中藻类疯长。
(5)处理方式:常用的灭藻剂以硫酸铜为主,它能扰乱藻类的光合反应,导致光合作用无法正常运行。通常泳池中含铜为0.4%时,灭藻效果最好,则为达到最佳灭藻效果,泳池中硫酸铜溶液的浓度为_______ 。
(1)游泳馆要求我们在一个浅水池内对拖鞋和脚进行消毒,浅水池中的水呈紫红色,该池中起消毒作用的物质可能是
活动一:偏爱游泳馆的人都知道,游泳池的水经常呈现淡淡的蓝色。他们对池水呈现蓝色的原因、溶质成分、池水处理方法和对环境的影响,展开了实验探究。
实验探究1:寻找池水呈现蓝色的原因。
【查阅资料】水吸收红色波段光反射蓝色波段光引起池水呈现蓝色,当水深到1-2米深度后才呈现出蓝色,且水越深蓝色越深。
【交流讨论】分别取一杯海水和泳池水观察:海水是无色,而泳池水依然显蓝色。有同学质疑:池水呈现蓝色可能加入了铜离子。
实验探究2:检验泳池水中是否含有铜离子。
(2)取少量池水于试管中,滴加几滴氢氧化钠溶液,有
【实验调查】同学们咨询了泳馆的管理人员得知,池水中加入硫酸铜起到抑制藻类繁殖等作用。
(3)请你再设计一种方法证明铜离子的存在
活动二:设计泳池水净化模拟实验装置。
(4)为确保游泳池的水质达到国际泳联最新卫生标准,将采用“砂滤—臭氧—活性炭”净水工艺净化游泳池里的水,下列有关说法错误的是______。
| A.砂滤是利用过滤原理,除去水中较大的固体颗粒 |
| B.臭氧的作用是消毒杀菌 |
| C.游泳池水中的臭氧浓度越大越好 |
| D.活性炭可以吸附水中悬浮的杂质 |
活动三:解谜里约夏季奥运会“碧池”(清澈湛蓝的游泳池水,一夜之间变成浑浊的碧绿色),场馆人员的解释是:工作人员误将80L过氧化氢溶液倾倒入池中消毒,氯气和过氧化氢产生氧气和另一化合物,导致水体中藻类疯长。
(5)处理方式:常用的灭藻剂以硫酸铜为主,它能扰乱藻类的光合反应,导致光合作用无法正常运行。通常泳池中含铜为0.4%时,灭藻效果最好,则为达到最佳灭藻效果,泳池中硫酸铜溶液的浓度为
您最近一年使用:0次
综合应用题
|
较易
(0.85)
解题方法
【推荐3】酸、碱、盐在工农业生产和生活中应用广泛,是初中化学重要的化合物。
(1)将①浓盐酸,②NaOH溶液,③Ca(OH)2溶液分别敞口放置于空气中,一段时间后,溶液质量增加的是___________ (填序号)。
(2)在烧杯内放入少量小苏打,向其中滴加稀盐酸,观察到___________ ,说明小苏打能与酸反应。
(3)某校化学小组在利用稀硫酸和氢氧化钾溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图像如图所示。

该实验是将___________ (选填“稀硫酸”或“氢氧化钾溶液”)滴加到另一种液中,c点所示溶液中溶质的化学式为___________ 。
(4)某氯化钠样品中,可能含有下列杂质BaCl2、MgCl2、Na2SO4中的一种或几种,某化学兴趣小组的同学欲探究其杂质成分,进行了如下图所示实验。

①步骤Ⅰ中玻璃棒的作用是___________ 。
②步骤Ⅱ中,加入NaOH溶液的目的是什么___________ ?
③步骤Ⅲ中发生反应的化学方程式为___________ 。
(5)某炼铁厂有一批赤铁矿,为测定该赤铁矿中氧化铁的含量,小组同学取10g该赤铁矿样品于烧杯中,向其中加入100g稀硫酸,恰好完全反应(杂质不溶于水也不与酸反应),过滤,得到2g滤渣,计算稀硫酸的溶质质量分数。
(1)将①浓盐酸,②NaOH溶液,③Ca(OH)2溶液分别敞口放置于空气中,一段时间后,溶液质量增加的是
(2)在烧杯内放入少量小苏打,向其中滴加稀盐酸,观察到
(3)某校化学小组在利用稀硫酸和氢氧化钾溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图像如图所示。

该实验是将
(4)某氯化钠样品中,可能含有下列杂质BaCl2、MgCl2、Na2SO4中的一种或几种,某化学兴趣小组的同学欲探究其杂质成分,进行了如下图所示实验。

①步骤Ⅰ中玻璃棒的作用是
②步骤Ⅱ中,加入NaOH溶液的目的是什么
③步骤Ⅲ中发生反应的化学方程式为
(5)某炼铁厂有一批赤铁矿,为测定该赤铁矿中氧化铁的含量,小组同学取10g该赤铁矿样品于烧杯中,向其中加入100g稀硫酸,恰好完全反应(杂质不溶于水也不与酸反应),过滤,得到2g滤渣,计算稀硫酸的溶质质量分数。
您最近一年使用:0次



