目前世界上60%的镁是从海水中提取的。其主要步骤如下:
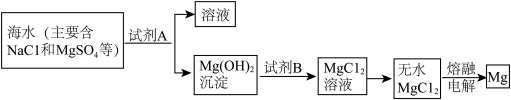
(1)提取镁的过程中,试剂A选用__________ ,试剂B选用________ ,由MgCl2制取镁的化学方程式为_____________ 。
(2)分离出Mg(OH)2后的NaCl溶液中还含有CaCl2、Na2SO4等杂质,为了获得纯净的NaCl溶液,在分离后的溶液中依次加入过量的BaCl2溶液、Na2CO3溶液,过滤,再向溶液中加入适量盐酸。实验中加入过量BaCl2溶液是为了除去__________ ,加入过量Na2CO3溶液的目的是________

(1)提取镁的过程中,试剂A选用
(2)分离出Mg(OH)2后的NaCl溶液中还含有CaCl2、Na2SO4等杂质,为了获得纯净的NaCl溶液,在分离后的溶液中依次加入过量的BaCl2溶液、Na2CO3溶液,过滤,再向溶液中加入适量盐酸。实验中加入过量BaCl2溶液是为了除去
更新时间:2019-05-22 15:43:39
|
相似题推荐
填空与简答-推断题
|
适中
(0.65)
【推荐1】如图是命题老师智能手机的屏幕解锁图形,好像有点简单哦。若A、B、C、D、E、F、G分别是炭粉、水、二氧化碳、氧化铁、盐酸、氢氧化钙溶液、氯化铁溶液中的一种,其中B常用来改良酸性土壤,C是人体胃液中的主要成分。
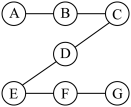
图中“一”表示两物质能发生反应。请完成下列各题:
(1)C、D的化学式分别为______ 、______ 。两种物质发生反应的实验现象是______ 。
(2)A与B反应的化学方程式为______ ; E与F反应的化学方程式为______ 。
(3)若要用实验的方法证明F和G两种物质能发生化学反应,可选用的试剂为______ 。

图中“一”表示两物质能发生反应。请完成下列各题:
(1)C、D的化学式分别为
(2)A与B反应的化学方程式为
(3)若要用实验的方法证明F和G两种物质能发生化学反应,可选用的试剂为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
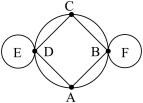
【推荐2】化学小组的同学们在假期参观了博物馆后,结合碱的化学性质设计了下图所示的古钱币形状的趣味模型。图中A、B、C、D、E、F分别代表酸碱指示剂、二氧化碳、稀硫酸、硫酸铜溶液、氢氧化钠溶液、氢氧化钙溶液。旋转古钱币形状的圆时,与E、F接触的物质均能与之发生反应。_____ (填字母)。
a.B与E b.D与F c.D与E
(2)若将D换成纯碱溶液,则它与F的反应_____ (选填“能”或“不能”)体现碱的通性。
(3)若A为紫色石蕊溶液,A与E接触时,能观察到的现象是_____ 。
(4)写出该模型涉及的反应中能表示氢氧化钠敞口放置会变质的原因的反应的化学方程式:_____ 。
a.B与E b.D与F c.D与E
(2)若将D换成纯碱溶液,则它与F的反应
(3)若A为紫色石蕊溶液,A与E接触时,能观察到的现象是
(4)写出该模型涉及的反应中能表示氢氧化钠敞口放置会变质的原因的反应的化学方程式:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
名校
【推荐3】分析下列反应,回答有关问题:
①2KOH+CO2═K2CO3+H2O;
②2NaOH+CO2═Na2CO3+H2O;
③Ca(OH)2+CO2═CaCO3↓+H2O.
(1)由上述反应可知,碱与二氧化碳反应的规律是都生成___________ 和水;
(2)根据上述规律,写出Ba(OH)2与CO2反应的化学方程式____________________________ ;
(3)用CO2鉴别NaOH和Ca(OH)2两种溶液时,能观察到明显现象的是________________ 溶液。
①2KOH+CO2═K2CO3+H2O;
②2NaOH+CO2═Na2CO3+H2O;
③Ca(OH)2+CO2═CaCO3↓+H2O.
(1)由上述反应可知,碱与二氧化碳反应的规律是都生成
(2)根据上述规律,写出Ba(OH)2与CO2反应的化学方程式
(3)用CO2鉴别NaOH和Ca(OH)2两种溶液时,能观察到明显现象的是
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐1】根据下图推断,假设都恰好完全反应:
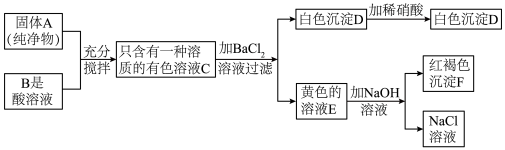
(1)固体物A是___________ (填化学式,下同);红褐色沉淀是:_____________ ;
(2)写出溶液C与BaCl2 反应的化学方程式________________________________ 。

(1)固体物A是
(2)写出溶液C与BaCl2 反应的化学方程式
您最近一年使用:0次
【推荐2】蛋白质是组成细胞的基础物质,没有蛋白质就没有生命。人体内的血红蛋白,各种酶都是蛋白质、蛋清、鲜乳汁中也有蛋白质。一些可溶性的重金属盐(如含Cu2+、Ba2+、Ag+等可溶性盐)与蛋白质作用会使蛋白质发生凝固而变性,从而丧失其生理功能,危及生命。因此,可溶性重金属盐为有毒物质。根据上述所给知识回答下列问题。
(1)在CuSO4、AgNO3、Ba(NO3)2、AgCl四种物质中无毒的是________ 。
(2)在医疗上用x射线检查肠胃病时,让病人服用_____ (填物质的化学式)的悬浊液(俗称钡餐),而不能服用碳酸钡,其原因是人体胃液中含有一定量的(填物质的化学式)______ ,与碳酸钡反应后,产生了一定量的使人中毒的________ (填离子符号)。
(3)若服用BaCO3中毒,下列方案中可作为最佳解毒措施的是______ 。(填序号)
A 多饮糖水 B 饮用Na2SO4溶液 C 饮用食盐水 D 多饮鲜牛乳
(1)在CuSO4、AgNO3、Ba(NO3)2、AgCl四种物质中无毒的是
(2)在医疗上用x射线检查肠胃病时,让病人服用
(3)若服用BaCO3中毒,下列方案中可作为最佳解毒措施的是
A 多饮糖水 B 饮用Na2SO4溶液 C 饮用食盐水 D 多饮鲜牛乳
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐1】现有实验室常见的A、B、C、D、E五种溶液,它们分别是澄清石灰水、硫酸铁溶液、碳酸钠溶液、氯化钠溶液和稀硫酸中的一种。鉴别它们可按如图所示的步骤进行。回答下列问题:
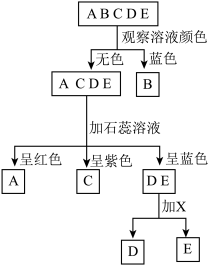
(1)B是_____ 溶液。
(2)用X鉴别D、E时,X可以选用不同类别的物质。
①若X为稀盐酸,写出有气体生成的反应的化学方程式_____ 。
②若X为碱,写出一个符合要求的物质的化学式_____ 。
(3)鉴别这五种溶液时,能否不用其他试剂,仅利用组内物质互相反应?_____ (选填“能”或“不能”)。

(1)B是
(2)用X鉴别D、E时,X可以选用不同类别的物质。
①若X为稀盐酸,写出有气体生成的反应的化学方程式
②若X为碱,写出一个符合要求的物质的化学式
(3)鉴别这五种溶液时,能否不用其他试剂,仅利用组内物质互相反应?
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
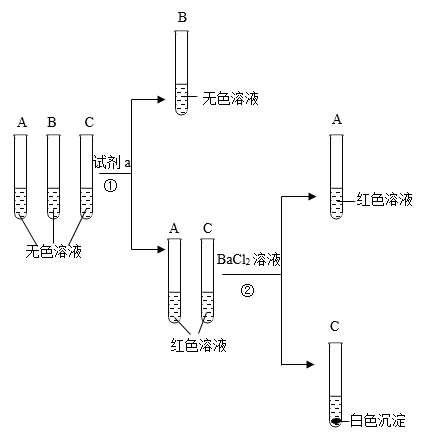
【推荐2】有A、B、C三瓶失去标签的无色溶液,它们分别是盐酸、澄清石灰水和碳酸钠溶液中的一种.为了鉴别它们,各取少量溶液两两混合,实验结果如下表所示.表中“↓”表示有沉淀产生;“↑”表示有气体产生;“﹣”表示观察不到明显的现象变化.
回答下列问题:
(1)A中溶质的化学式是_____________ ,A与C反应的基本类型是_____________ ;
(2)A与B、B与C反应的化学方程式分别是____________ 、_______________ .
| A | B | C | |
| A | ↑ | ﹣ | |
| B | ↑ | ↓ | |
| C | ﹣ | ↓ |
(1)A中溶质的化学式是
(2)A与B、B与C反应的化学方程式分别是
您最近一年使用:0次
【推荐1】利用海洋资源是我们国家建设海洋强国的必然需要。
(1)①海水晒盐的基本原理为______ (填"蒸发"或"降温")结晶。
②粗盐水中主要含有CaCl2、MgSO4等可溶性杂质可加下了物质,利用过建等操作进行除杂,则加入下列三种物质的先后顺序为______ (填字母序号)。
A.适量的盐酸
B.稍过量的Na2CO3溶液
C.稍过量的Ba(OH)2溶液
③加入过量的Na2CO3溶液的目的是______ 。
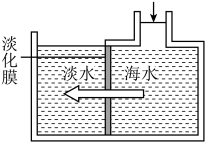
(2)海水淡化可采用膜分离技术,如图所示,对淡化膜右侧的海水加压,水分子可以透过谈化膜进入左侧淡水池,而海水中的各种离子不能透过淡化膜,从而得到淡水。对加压后右侧海水成分变化进行分析,正确的是______(填选项序号)。
(3)海水制镁的工艺流程如图。

其中发生的中和反应的化学方程式为______ 。
(4)海水制碱:我国著名制碱专家侯德榜创立“侯氏制碱法”,促进了世界制碱技术的发展。其生产原理示意图如下:
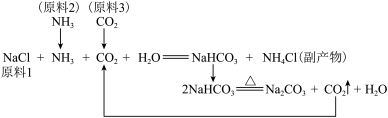
①由上图可知制碱过程中可以循环利用的物质是______ ,产物中可作氮肥的是______ 。
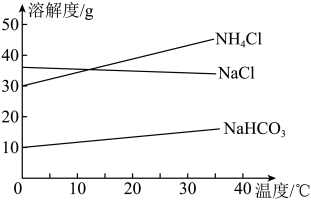
②产物中NaHCO3比NH4Cl先结晶析出。请结合生产原理及如图解释其原因:______ (共答两条)。
(1)①海水晒盐的基本原理为
②粗盐水中主要含有CaCl2、MgSO4等可溶性杂质可加下了物质,利用过建等操作进行除杂,则加入下列三种物质的先后顺序为
A.适量的盐酸
B.稍过量的Na2CO3溶液
C.稍过量的Ba(OH)2溶液
③加入过量的Na2CO3溶液的目的是
(2)海水淡化可采用膜分离技术,如图所示,对淡化膜右侧的海水加压,水分子可以透过谈化膜进入左侧淡水池,而海水中的各种离子不能透过淡化膜,从而得到淡水。对加压后右侧海水成分变化进行分析,正确的是______(填选项序号)。

| A.溶质质量减少 | B.溶剂质量减少 | C.溶液质量减少 | D.溶质质量分数减小 |
(3)海水制镁的工艺流程如图。

其中发生的中和反应的化学方程式为
(4)海水制碱:我国著名制碱专家侯德榜创立“侯氏制碱法”,促进了世界制碱技术的发展。其生产原理示意图如下:

①由上图可知制碱过程中可以循环利用的物质是
②产物中NaHCO3比NH4Cl先结晶析出。请结合生产原理及如图解释其原因:

您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】海洋中蕴含丰富的资源。
(1)海水淡化
①海水淡化是解决淡水资源不足的重要方法,下列方法中,可以使海水淡化的是_____ (填字母序号);
A.过滤 B.吸附 C.沉降 D.蒸馏
②用化学方法区分蒸馏水和海水可采用的试剂是______ 。
(2)利用海水制取纯碱和金属镁的流程如图所示,试回答问题:
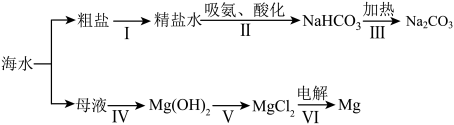
①1925 年我国化学家_____ 创立了联合制碱法,促进了世界制碱技术的发展。
②步骤Ⅰ粗盐形成精盐水的过程中需去除泥沙。除去泥沙需经过溶解、过滤、蒸发三个步骤,均要用到玻璃棒,其中玻璃棒在蒸发中的作用是_____ 。
③步骤Ⅰ粗盐形成精盐水的过程中还要除去 MgCl2、CaCl2、Na2SO4杂质。可依次加入过量的 BaCl2、NaOH、Na2CO3溶液,充分反应后过滤,并在滤液中加入适量稀盐酸形成精盐水。加入稀盐酸的目的______ 。
④步骤Ⅱ中吸氨的目的是______ ,第Ⅱ步反应的化学方程式为______ 。
⑤其第Ⅲ步反应的化学方程式为_______ 。
⑥在工业生产中为了减低成本,步骤Ⅳ中所加试剂最好选择的是______ 。
⑦步骤Ⅵ中需电解______ 状态的氯化镁获得金属镁。
(1)海水淡化
①海水淡化是解决淡水资源不足的重要方法,下列方法中,可以使海水淡化的是
A.过滤 B.吸附 C.沉降 D.蒸馏
②用化学方法区分蒸馏水和海水可采用的试剂是
(2)利用海水制取纯碱和金属镁的流程如图所示,试回答问题:

①1925 年我国化学家
②步骤Ⅰ粗盐形成精盐水的过程中需去除泥沙。除去泥沙需经过溶解、过滤、蒸发三个步骤,均要用到玻璃棒,其中玻璃棒在蒸发中的作用是
③步骤Ⅰ粗盐形成精盐水的过程中还要除去 MgCl2、CaCl2、Na2SO4杂质。可依次加入过量的 BaCl2、NaOH、Na2CO3溶液,充分反应后过滤,并在滤液中加入适量稀盐酸形成精盐水。加入稀盐酸的目的
④步骤Ⅱ中吸氨的目的是
⑤其第Ⅲ步反应的化学方程式为
⑥在工业生产中为了减低成本,步骤Ⅳ中所加试剂最好选择的是
⑦步骤Ⅵ中需电解
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
真题
解题方法
【推荐3】二十一世纪是海洋开发与利用的世纪,我市实施黄蓝两大国家战略形成新的发展格局,海洋化学资源的综合利用将是重点发展领域之一。
(1)海水晒盐:将海水引入蒸发池,经日晒蒸发到一定程度时,导入结晶池,继续日晒,海水就会成为食盐的饱和溶液,再晒就会逐渐析出粗盐,剩余的液体称为母液(也称卤水)。
1L海水在逐渐浓缩过程中不断析出的盐的种类和质量(单位:g)关系如下表所示:
I、海水晒盐是 1 (选填“物理”或“化学”)变化,包含蒸发、 2 等过程。
II、若得到纯度较高的粗盐和含浓度较高的卤水,卤水的密度应控制在什么范围 3 ,原因是 4 。
(2)海水制镁:海水晒盐后,以其母液(卤水)和贝壳(主要成分是CaCO3)为原料制镁,其工艺流程如下图所示:
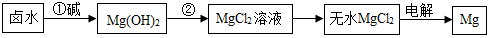
I、步骤①所加的碱应该是 5 (选填“氢氧化钠”或“石灰乳”),步骤②反应的化学方程式是 6 ;若要验证镁、铁、铜的活动性顺序,选择铁丝后,还要选择 7 、 8 两种溶液。
II、Mg(OH)2加热分解生成MgO和H2O,MgO是高熔点的化合物,某些阻燃剂(阻碍燃烧的物质)的有效成分是Mg(OH)2。你认为Mg(OH)2能够阻燃的原因可能是 9 (选填序号)
A.Mg(OH)2分解需要吸收大量的热,降低了可燃物的着火点
B.生成的氧化镁覆盖在可燃物表面,隔绝了空气
C.生成的水蒸气降低了可燃物周围氧气浓度
D.反应因吸热降低了环境温度,使可燃物不易达到着火点
(1)海水晒盐:将海水引入蒸发池,经日晒蒸发到一定程度时,导入结晶池,继续日晒,海水就会成为食盐的饱和溶液,再晒就会逐渐析出粗盐,剩余的液体称为母液(也称卤水)。
1L海水在逐渐浓缩过程中不断析出的盐的种类和质量(单位:g)关系如下表所示:
| 海水密度(g/mL) | CaSO4 | NaCl | MgCl2 | MgSO4 |
| 1.20 | 0.91 | |||
| 1.21 | 0.05 | 3.26 | 0.004 | 0.008 |
| 1.22 | 0.015 | 9.65 | 0.01 | 0.04 |
| 1.26 | 0.01 | 2.64 | 0.02 | 0.02 |
| 1.31 | 1.40 | 0.54 | 0.03 |
II、若得到纯度较高的粗盐和含浓度较高的卤水,卤水的密度应控制在什么范围
(2)海水制镁:海水晒盐后,以其母液(卤水)和贝壳(主要成分是CaCO3)为原料制镁,其工艺流程如下图所示:
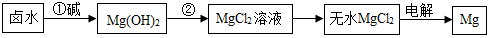
I、步骤①所加的碱应该是
II、Mg(OH)2加热分解生成MgO和H2O,MgO是高熔点的化合物,某些阻燃剂(阻碍燃烧的物质)的有效成分是Mg(OH)2。你认为Mg(OH)2能够阻燃的原因可能是
A.Mg(OH)2分解需要吸收大量的热,降低了可燃物的着火点
B.生成的氧化镁覆盖在可燃物表面,隔绝了空气
C.生成的水蒸气降低了可燃物周围氧气浓度
D.反应因吸热降低了环境温度,使可燃物不易达到着火点
您最近一年使用:0次