用图1所示的装置制取二氧化碳并测定石灰石中碳酸钙的质量,化学反应方程式是 ,将稀盐酸全部加入锥形瓶中,天平示数的变化如图2所示,请计算:
,将稀盐酸全部加入锥形瓶中,天平示数的变化如图2所示,请计算:
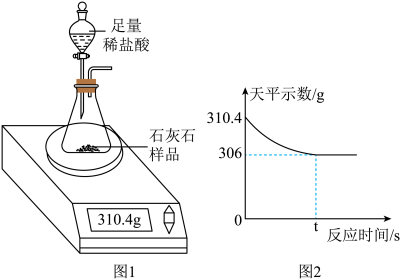
(1)生产二氧化碳气体的质量为_____________?
(2)计算石灰石样品中碳酸钙的质量_____________?
 ,将稀盐酸全部加入锥形瓶中,天平示数的变化如图2所示,请计算:
,将稀盐酸全部加入锥形瓶中,天平示数的变化如图2所示,请计算:
(1)生产二氧化碳气体的质量为_____________?
(2)计算石灰石样品中碳酸钙的质量_____________?
19-20九年级上·河北保定·期中 查看更多[7]
(已下线)2023年人教版同步单元精练第五单元化学方程式03巩固练山东省临沂市平邑县塞博中学2022-2023学年九年级上学期期中化学试题四川省眉山市仁寿县龙正中学2022-2023学年九年级上学期期中化学试题四川省眉山市仁寿县龙正镇初级中学校2022-2023学年九年级上学期期中化学试题(已下线)第7单元 燃料及其利用(检测卷)-2020-2021学年九年级化学上册同步课堂课件精讲及好题精练(人教版)(已下线)《课时同步练》5.3 利用化学方程式进行简单的计算-2020-2021学年九年级化学上册课时同步练(人教版)河北省保定市定州市2019-2020学年九年级上学期期中化学试题
更新时间:2019-11-20 20:30:39
|
相似题推荐
计算题
|
适中
(0.65)
真题
解题方法
【推荐1】“7150灭火剂”(C3H9B3O6,相对分子质量为174)以雾状形式喷射到燃着的金属时,立即发生燃烧反应: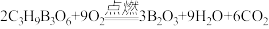 。反应能很快耗尽金属物品附近的氧气,生成的玻璃状B2O3覆盖在金属物品表面而隔绝空气,从而有效灭火。若充分燃烧348g“7150灭火剂”,会消耗常温下的氧气多少升?(常温下氧气密度约为1.4g·L-1,结果保留一位小数)。
。反应能很快耗尽金属物品附近的氧气,生成的玻璃状B2O3覆盖在金属物品表面而隔绝空气,从而有效灭火。若充分燃烧348g“7150灭火剂”,会消耗常温下的氧气多少升?(常温下氧气密度约为1.4g·L-1,结果保留一位小数)。
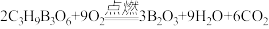 。反应能很快耗尽金属物品附近的氧气,生成的玻璃状B2O3覆盖在金属物品表面而隔绝空气,从而有效灭火。若充分燃烧348g“7150灭火剂”,会消耗常温下的氧气多少升?(常温下氧气密度约为1.4g·L-1,结果保留一位小数)。
。反应能很快耗尽金属物品附近的氧气,生成的玻璃状B2O3覆盖在金属物品表面而隔绝空气,从而有效灭火。若充分燃烧348g“7150灭火剂”,会消耗常温下的氧气多少升?(常温下氧气密度约为1.4g·L-1,结果保留一位小数)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】将6g碳和18g氧气在密闭容器中燃烧,充分反应后得到的二氧化碳为多少g?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】甲、乙、丙三位同学用下列试剂分别进行实验,均恰好完全反应。所用试剂及质量见下表:
已知a1+a2+a3=23.04g,b1+b2+b3=189.8g,现将甲、乙、丙三同学所得溶液全部倒入一个容器内,称得溶液为206.16g,试求此混合溶液的溶质质量分数(精确到0.1%,写出计算过程)
| 试剂及质量 | 反应后所得溶液质量 | ||
| 甲 | CaO(固)a1g | 10%盐酸b1g | C1 |
| 乙 | Ca(OH)2(固)a2g | 10%盐酸b2g | C2 |
| 丙 | CaCO3(固)a3g | 10%盐酸b3g | C3 |
已知a1+a2+a3=23.04g,b1+b2+b3=189.8g,现将甲、乙、丙三同学所得溶液全部倒入一个容器内,称得溶液为206.16g,试求此混合溶液的溶质质量分数(精确到0.1%,写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】向某锌粉样品(所含杂质既不溶于水也不溶于酸)中加入足量的稀盐酸123.4g。使其充分反应,所加锌粉的质量与产生气体的质量的关系如图所示:
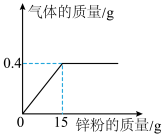
试计算:反应后所得溶液中溶质的质量分数____ 。

试计算:反应后所得溶液中溶质的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】请根据如图所示的实验过程和提供的数据计算(铜与硫酸不发生反应)
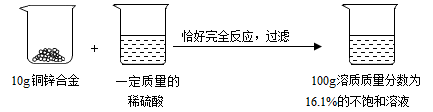
(1)生成氢气___________g;
(2)该铜锌合金中锌元素的质量分数是多少?

(1)生成氢气___________g;
(2)该铜锌合金中锌元素的质量分数是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】实验室有一瓶标签残损的白色固体粉末,已知其可能是 NaCl、Na2CO3、NaHCO3 三种物质中的一种,小路同学想通过实验的方法来确定其成分组成。其实步骤及现象如图1、2、3所示:(已知:20℃时,碳酸钠的溶解度为 21.8g,碳酸氢钠的溶解度为 9.6g。)
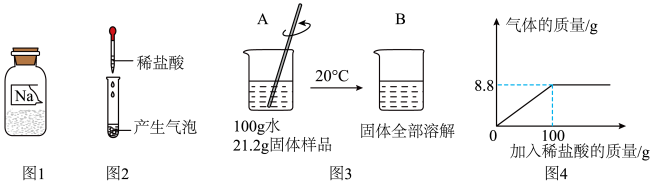
根据上述信息,是回答下列问题
(1)由图2可推知,该白色固体不是 。
(2)由图3可推知,该白色固体是 ,理由为 。
(3)利用烧杯B中的溶液可测定某稀盐酸的溶质质量分数,测得反应过程中某些量的数据关系,如图4所示:请你根据化学方程式,写出具体计算过程(计算结果精确到 0.1%)。

根据上述信息,是回答下列问题
(1)由图2可推知,该白色固体不是 。
(2)由图3可推知,该白色固体是 ,理由为 。
(3)利用烧杯B中的溶液可测定某稀盐酸的溶质质量分数,测得反应过程中某些量的数据关系,如图4所示:请你根据化学方程式,写出具体计算过程(计算结果精确到 0.1%)。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】鸡蛋壳的主要成分是碳酸钙,某兴趣小组为了测定鸡蛋壳中CaCO3的含量。现取清洗、晾干、捣碎的鸡蛋壳碎片15g,放在烧杯中,然后向其中加入80g的稀盐酸,使之充分反应(鸡蛋壳中除CaCO3外的其他成分不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示。
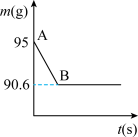
(1)实验前将鸡蛋壳捣碎,其目的是___________ ;
(2)依据图中数据分析,生成CO2的质量为___________ ;
(3)计算该鸡蛋壳中CaCO3的质量分数(结果精确到0.1%);
(4)下列情况会导致鸡蛋壳中碳酸钙质量分数测量值偏小的是___________(双选)。

(1)实验前将鸡蛋壳捣碎,其目的是
(2)依据图中数据分析,生成CO2的质量为
(3)计算该鸡蛋壳中CaCO3的质量分数(结果精确到0.1%);
(4)下列情况会导致鸡蛋壳中碳酸钙质量分数测量值偏小的是___________(双选)。
| A.向鸡蛋壳中滴加过量稀盐酸 | B.鸡蛋壳碎片未完全反应 |
| C.烧杯中部分氯化氢和水蒸气随二氧化碳逸出 | D.鸡蛋壳未晾干,有残留的水 |
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】实验室常用石灰石与稀盐酸反应制取二氧化碳。为了测定石灰石中碳酸钙的含量,小乐进行了如下实验:取12.0g石灰石放于烧杯中,向烧杯中滴加稀盐酸,实验测得烧杯中剩余物质的质量与加入稀盐酸的质量之间的关系如图所示。整个过程不考虑稀盐酸的挥发和气体的溶解,石灰石中的杂质也不与稀盐酸反应。求:

(1)产生CO2的总质量为______ g
(2)石灰石中碳酸钙的质量分数(写出计算过程)

(1)产生CO2的总质量为
(2)石灰石中碳酸钙的质量分数(写出计算过程)
您最近一年使用:0次

 等质量分数的稀盐酸,充分反应后测得的实验数据如下:
等质量分数的稀盐酸,充分反应后测得的实验数据如下:

