解题方法
1 . 早在战国时期,《周礼·考工记》就记载了我国劳动人民制取氢氧化钾以漂洗丝帛的工艺;大意是:先将干燥的木头烧成草木灰(主要成分为 );加水后形成灰汁(主要为
);加水后形成灰汁(主要为 溶液),用其灰汁浸泡丝帛,再加入石灰(主要成分为
溶液),用其灰汁浸泡丝帛,再加入石灰(主要成分为 )即可;化学实践小组的同学以此为依据,进行了相应的科学实践活动;
)即可;化学实践小组的同学以此为依据,进行了相应的科学实践活动;
已知: 与
与 化学性质相似
化学性质相似
【实践内容】探究灰汁的性质
【实验一】灰汁酸碱度测定
(1)在玻璃片上放一小片 试纸,用玻璃棒蘸取灰汁,滴在
试纸,用玻璃棒蘸取灰汁,滴在 试纸上,把试纸显示的颜色与标准比色卡比较,酸碱度为
试纸上,把试纸显示的颜色与标准比色卡比较,酸碱度为
_______ 7(填“>”、“<”或“=”);
【实验二】灰汁反应后成分分析
将上述灰汁与石灰进行混合,观察到有白色沉淀产生.对沉淀进行过滤后,得到无色滤液
小组成员随即对滤液成分进行了分析
[提出猜想]滤液中溶质成分有:
(2)猜想1、 ; 猜想2、
; 猜想2、
猜想3、_______ ; 猜想4、
(3)同学们一致认为猜4不合理,理由是_______ ;
[实验验证]
(4)
(5)写出实验二涉及到的方程式_______ ;
[实验拓展]实验结束后,小明进行了补充实验三
(6)小明的实验结论与小组同学得出的实验结论结果不一致,指导教师指出小明的实验设计存在问题,才导致其结论错误,小明实验设计出现的问题是_______ 。
 );加水后形成灰汁(主要为
);加水后形成灰汁(主要为 溶液),用其灰汁浸泡丝帛,再加入石灰(主要成分为
溶液),用其灰汁浸泡丝帛,再加入石灰(主要成分为 )即可;化学实践小组的同学以此为依据,进行了相应的科学实践活动;
)即可;化学实践小组的同学以此为依据,进行了相应的科学实践活动;已知:
 与
与 化学性质相似
化学性质相似【实践内容】探究灰汁的性质
【实验一】灰汁酸碱度测定
(1)在玻璃片上放一小片
 试纸,用玻璃棒蘸取灰汁,滴在
试纸,用玻璃棒蘸取灰汁,滴在 试纸上,把试纸显示的颜色与标准比色卡比较,酸碱度为
试纸上,把试纸显示的颜色与标准比色卡比较,酸碱度为
【实验二】灰汁反应后成分分析
将上述灰汁与石灰进行混合,观察到有白色沉淀产生.对沉淀进行过滤后,得到无色滤液
小组成员随即对滤液成分进行了分析
[提出猜想]滤液中溶质成分有:
(2)猜想1、
 ; 猜想2、
; 猜想2、
猜想3、

(3)同学们一致认为猜4不合理,理由是
[实验验证]
(4)
| 实验步骤 | 实验现象 | 结论 | |
| 实验一 | 取少许该滤液,加入 ,溶液 ,溶液 | 观察到 | 猜想2不正确 |
| 实验二 | 另取少许该滤液,加入 | 观察到有沉淀生成 | 猜想3正确 |
(5)写出实验二涉及到的方程式
[实验拓展]实验结束后,小明进行了补充实验三
| 实验步骤 | 实验现象 | 结论 | |
| 实验三 | 另取少许该滤液,加入少量的稀盐酸溶液 | 观察到无气泡产生 | 猜想3不正确 |
(6)小明的实验结论与小组同学得出的实验结论结果不一致,指导教师指出小明的实验设计存在问题,才导致其结论错误,小明实验设计出现的问题是
您最近一年使用:0次
2 . 某化学兴趣小组同学用足量稀盐酸除去铁钉表面的铁锈(主要成分是Fe2O3)时,发现反应开始时铁锈消失,有气泡产生,溶液颜色为黄色,放置一天后黄色溶液变为浅绿色。同学们对此异常现象展开探究。
【查阅资料】①FeCl3溶液呈黄色;②Fe2+在空气中易氧化成Fe3+。
【做出猜想】
(1)猜想1:溶液变浅绿色与_______ 有关;
猜想2:溶液变浅绿色与铁有关;
猜想3:溶液变浅绿色与铁和稀盐酸都有关。
【实验1】同学们设计如下实验,对上述猜想进行验证(已知氢气对该反应无影响.实验时间为1天)。
【实验现象及结论】
(2)实验结束后,观察到甲组溶液颜色仍为黄色,乙组产生红竭色沉淀,丙组溶液逐渐从黄色变浅绿色。由此得知猜想_______ 成立。
【反思交流】
(3)铁生锈是铁与空气中的_______ 发生反应的结果。
(4)查阅资料得知,溶液变为浅绿色的过程中是Fe与FeCl3反应生成FeCl2,该反应的化学方程式为_______ 。
(5)有同学提出疑问,乙组中的Fe也能与FeCl3发生反应,为何最终得到红褐色沉淀?
老师告诉同学们,乙组生成的FeCl2与空气中的物质经过一系列复杂反应后产生红褐色的Fe(OH)3,而丙组实验的溶液显酸性,则不会出现此种情况。由此可知,保存FeCl2溶液时应注意______ 。
探究二:探究溶液颜色变化速率的影响因素
【实验2】同学们用生锈程度相同的铁钉和5mL稀盐酸进行下列三组实验,实验现象记录在表中:
【分析讨论】
(6)生锈铁钉与盐酸反应时,溶液的颜色变化速率与______ 有关。
(7)基于上述实验推测,下列关于工业上用盐酸除铁锈的说法合理的是_______(填字母序号)。
【查阅资料】①FeCl3溶液呈黄色;②Fe2+在空气中易氧化成Fe3+。

【做出猜想】
(1)猜想1:溶液变浅绿色与
猜想2:溶液变浅绿色与铁有关;
猜想3:溶液变浅绿色与铁和稀盐酸都有关。
【实验1】同学们设计如下实验,对上述猜想进行验证(已知氢气对该反应无影响.实验时间为1天)。
【实验现象及结论】
(2)实验结束后,观察到甲组溶液颜色仍为黄色,乙组产生红竭色沉淀,丙组溶液逐渐从黄色变浅绿色。由此得知猜想
【反思交流】
(3)铁生锈是铁与空气中的
(4)查阅资料得知,溶液变为浅绿色的过程中是Fe与FeCl3反应生成FeCl2,该反应的化学方程式为
(5)有同学提出疑问,乙组中的Fe也能与FeCl3发生反应,为何最终得到红褐色沉淀?
老师告诉同学们,乙组生成的FeCl2与空气中的物质经过一系列复杂反应后产生红褐色的Fe(OH)3,而丙组实验的溶液显酸性,则不会出现此种情况。由此可知,保存FeCl2溶液时应注意
探究二:探究溶液颜色变化速率的影响因素
【实验2】同学们用生锈程度相同的铁钉和5mL稀盐酸进行下列三组实验,实验现象记录在表中:
| 实验编号 | 所用试剂 | 实验现象 | |
| 反应开始时 | 24h后 | ||
| ① | 生锈铁钉和2%的盐酸 | 生锈铁钉、溶液均无明显变化 | 铁锈消失,溶液变为浅绿色 |
| ② | 生锈铁钉和5%的盐酸 | 铁钉表面有少量气泡,铁钉逐渐消失,溶液逐渐由无色变浅黄色 | 溶液变为浅绿色 |
| ③ | 生锈铁钉和10%的盐酸 | 铁钉表面产生大量气泡,铁钉逐渐消失,溶液很快由无色变为黄色 | 溶液变为浅绿色 |
(6)生锈铁钉与盐酸反应时,溶液的颜色变化速率与
(7)基于上述实验推测,下列关于工业上用盐酸除铁锈的说法合理的是_______(填字母序号)。
| A.除铁锈时,加入的盐酸越多越好 |
| B.在除锈过程中,生成的FeCl3对铁也有腐蚀作用 |
| C.用盐酸除锈时,应注意控制反应的时间 |
您最近一年使用:0次
3 . 央视报道了保温杯重金属超标案例。某校化学兴趣小组进行了调查,发现不锈钢含金属锰。因常见金属活动性顺序未包含锰,他们为确定锰、铁、铜的金属活动性顺序,进行了探究活动。
【查阅资料】硫酸锰中锰元素显+2价,其溶液颜色呈浅粉红色。
【猜想与假设】
(1)猜想一:Fe>Cu>Mn 猜想二:Mn>Fe>Cu 猜想三:________
【设计实验】
同学们经过讨论一致认为,可以先探究Mn与酸是否反应,确定锰在金属活动顺序中是否位于氢前;若在氢前,只需比较锰、铁与酸反应的剧烈程度。
【药品选用】纯铁片、纯铜片、纯锰片、硫酸亚铁溶液、硫酸铜溶液、硫酸锰溶液、稀硫酸
(2)【进行实验】
(3)实验过程中,甲同学发现还可以利用金属与盐溶液的反应得出锰与铁、铜的金属活动性顺序。
【反思与交流】
(4)通过以上实验得出金属的化学性质有____________ 。
【查阅资料】硫酸锰中锰元素显+2价,其溶液颜色呈浅粉红色。
【猜想与假设】
(1)猜想一:Fe>Cu>Mn 猜想二:Mn>Fe>Cu 猜想三:
【设计实验】
同学们经过讨论一致认为,可以先探究Mn与酸是否反应,确定锰在金属活动顺序中是否位于氢前;若在氢前,只需比较锰、铁与酸反应的剧烈程度。
【药品选用】纯铁片、纯铜片、纯锰片、硫酸亚铁溶液、硫酸铜溶液、硫酸锰溶液、稀硫酸
(2)【进行实验】
实验操作 | 实验现象 | 实验结论 | 化学方程式 |
| 铁片与锰片表面产生气泡,铜片表面无明显现象,铁片表面产生气泡的速率比锰片慢 | 猜想二正确 |
实验操作 | 实验现象 | 实验结论 | 化学方程式 |
猜想二正确 |
【反思与交流】
(4)通过以上实验得出金属的化学性质有
您最近一年使用:0次
解题方法
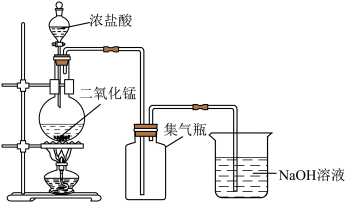
4 . 实验小组用MnO2与浓盐酸反应制取氯气(Cl2),如下图所示。
已知:氯气是黄绿色具有刺激性气味的有毒气体。____ MnO2+_____ HCl
_____ MnCl2+_____ Cl2↑+_____ ______ 。
(2)用向上排空气法收集Cl2,依据Cl2的物理性质是________ 。
(3)NaOH溶液的作用是__________ 。
小组同学发现,反应停止时反应物均有剩余。
【提出问题】反应停止与什么有关呢?
【查阅资料】
Ⅰ.初中常见的酸(如H2SO4、HCl)、碱(如NaOH)及可溶性盐(如NaCl)在水溶液中能完全解离出阳离子和阴离子。例如,HCl在水中能解离出H+和Cl-。
Ⅱ.Cl2能与KI反应置换出I2;淀粉遇I2变蓝,在本实验中作为指示剂,指示I2是否存在。
【提出猜想】
①反应停止与溶液中的Cl-浓度降低到一定程度有关;
②_________。
【进行实验】
为验证猜想,取适量反应后的固液混合物于试管中,分别进行以下实验:
【解释与结论】
(4)猜想②是___________ 。
(5)A中加入的固体是________ 。
(6)B中试纸变蓝的原因是________ 。
【反思与评价】
(7)小组同学认为实验B还不够严谨,原因是________ 。
已知:氯气是黄绿色具有刺激性气味的有毒气体。

(2)用向上排空气法收集Cl2,依据Cl2的物理性质是
(3)NaOH溶液的作用是
小组同学发现,反应停止时反应物均有剩余。
【提出问题】反应停止与什么有关呢?
【查阅资料】
Ⅰ.初中常见的酸(如H2SO4、HCl)、碱(如NaOH)及可溶性盐(如NaCl)在水溶液中能完全解离出阳离子和阴离子。例如,HCl在水中能解离出H+和Cl-。
Ⅱ.Cl2能与KI反应置换出I2;淀粉遇I2变蓝,在本实验中作为指示剂,指示I2是否存在。
【提出猜想】
①反应停止与溶液中的Cl-浓度降低到一定程度有关;
②_________。
【进行实验】
为验证猜想,取适量反应后的固液混合物于试管中,分别进行以下实验:
| 序号 | 实验操作 | 实验现象 | 实验结论 |
| A | 向试管中加入_____固体,充分振荡后加热,将湿润的淀粉KI试纸置于管口 | 试纸未变蓝 | 猜想①不成立 |
| B | 向试管中滴入2滴浓硫酸,充分振荡后加热,将湿润的淀粉KI试纸置于管口 | 试纸变蓝 | 猜想②成立 |
(4)猜想②是
(5)A中加入的固体是
(6)B中试纸变蓝的原因是
【反思与评价】
(7)小组同学认为实验B还不够严谨,原因是
您最近一年使用:0次
解题方法
5 . 食用碱(Na2CO3)是厨房中常见的一种物质,可用作食品膨松剂,发酵面粉。在生活中,食用碱还有哪些妙用呢?为此同学们展开了下列探究。
探究一:自制炉具清洁剂
【提供物品】食品包装袋中的食品干燥剂(CaO)、食用碱(Na2CO3)、水。
【交流讨论】
(1)Na2CO3溶液呈碱性,测溶液酸碱度最简单的方法可选用_______ 。
【实验1】
(2)如图实验,同学们自制炉具清洁剂,写出生成沉淀的化学方程式_______ 。
【提出问题】炉具清洁剂中的溶质成分是什么?
【作出猜想】
(3)猜想1:NaOH、Na2CO3
猜想2:NaOH
猜想3:______ 。
(4)【进行实验2】
探究三:熟悉炉具清洁剂的使用方法
【查阅资料】
(5)炉具清洁剂说明书上介绍:将护具清洁剂喷洒到待清洗油污的表面、停留3~6分钟(在50-60℃时使用效果更好)然后用湿抹布即可抹去油污、再用清水冲洗。相较于冷水,护具清洁剂在50~60℃时比在常温下使用效果更好。从微观角度分析其原因是_______ 。
探究一:自制炉具清洁剂
【提供物品】食品包装袋中的食品干燥剂(CaO)、食用碱(Na2CO3)、水。
【交流讨论】
(1)Na2CO3溶液呈碱性,测溶液酸碱度最简单的方法可选用
【实验1】
(2)如图实验,同学们自制炉具清洁剂,写出生成沉淀的化学方程式

【提出问题】炉具清洁剂中的溶质成分是什么?
【作出猜想】
(3)猜想1:NaOH、Na2CO3
猜想2:NaOH
猜想3:
(4)【进行实验2】
| 实验方案 | 实验现象 | 实验结论 |
| ①取少量炉具清洁剂于试管中,向其中滴加足量稀盐酸 | 猜想1错误 | |
| ②取少量炉具清洁剂于试管中,向其中滴加 | 产生白色沉淀 | 猜想3正确 |
探究三:熟悉炉具清洁剂的使用方法
【查阅资料】
(5)炉具清洁剂说明书上介绍:将护具清洁剂喷洒到待清洗油污的表面、停留3~6分钟(在50-60℃时使用效果更好)然后用湿抹布即可抹去油污、再用清水冲洗。相较于冷水,护具清洁剂在50~60℃时比在常温下使用效果更好。从微观角度分析其原因是
您最近一年使用:0次
6 . 某化学兴趣小组同学取一定量的碳酸钙固体高温煅烧一段时间,冷却后,对剩余固体成分进行如下探究。
【查阅资料】
(1)①氢氧化钙微溶于水,其水溶液的pH_______ (选填“>”、“<"或“=”)7。
②高温煅烧碳酸钙发生的反应的化学方程式为_______ 。
【作出猜想】
(2)猜想一:全部是氧化钙;
猜想二:_______ 。
猜想三:全部是碳酸钙。
【交流讨论】
(3)甲同学取一定量的剩余固体于试管中,加入一定量的水,振荡,有白色不溶物。甲同学据此认为试管中的固体有碳酸钙。乙同学认为上述实验不足以证明剩余固体中有碳酸钙,其理由是_______ 。
(4)乙同学取一定量的剩余固体于试管中,加入一定量的水,触摸试管外壁感觉发热,据此得出剩余固体中一定含有______ 。
[进行实验]
(5)最后在老师的指导下,全组同学共同制定了如下实验方案,并得出了正确的实验结论。
【查阅资料】
(1)①氢氧化钙微溶于水,其水溶液的pH
②高温煅烧碳酸钙发生的反应的化学方程式为
【作出猜想】
(2)猜想一:全部是氧化钙;
猜想二:
猜想三:全部是碳酸钙。
【交流讨论】
(3)甲同学取一定量的剩余固体于试管中,加入一定量的水,振荡,有白色不溶物。甲同学据此认为试管中的固体有碳酸钙。乙同学认为上述实验不足以证明剩余固体中有碳酸钙,其理由是
(4)乙同学取一定量的剩余固体于试管中,加入一定量的水,触摸试管外壁感觉发热,据此得出剩余固体中一定含有
[进行实验]
(5)最后在老师的指导下,全组同学共同制定了如下实验方案,并得出了正确的实验结论。
| 实验操作 | 实验现象 | 实验结论 | |
| 取一定量剩余固体于试管中,加水溶解并过滤 | 向滤液中滴加少量 | 溶液变红 | 猜想二成立 |
| 向滤渣中加入足量的稀盐酸 | |||
您最近一年使用:0次
2024-05-30更新
|
94次组卷
|
2卷引用:2024年江西省吉安市吉安县城北中学中考三模化学试题
解题方法
7 . CaCl2可用于冷冻剂、干燥剂、融雪剂、医药及冶金工业等。化学兴趣小组在完成实验室制取二氧化碳的实验后,欲对剩余废液的组成进行探究,并制定回收CaCl2的方案。
【猜想与假设】猜想一:CaCl2猜想二:CaCl2和HCl
【查阅资料】CaCl2溶液呈中性
【探究活动一】取少量废液等分成2份,甲、乙两组同学分别利用其中一份进行如下探究:
(1)甲组同学向废液中滴加紫色石蕊溶液,溶液变成________ 色,证明猜想二成立。
乙组同学用图1装置进行实验,将80mL一定质量分数的碳酸钠溶液逐滴加入废液,测得数据如图2。
【数据分析】乙组同学对图2数据进行讨论分析,证明猜想二成立。
(2)I.a点的实验现象为________ 。
Ⅱ.b点发生反应的化学方程式为________ 。
Ⅲ.c点对应溶液中全部溶质的化学式为________ 。
【探究活动二】
(3)丙组同学提出直接蒸发溶剂可从剩余废液中回收纯净CaCl2,理由是________ 。
【交流与反思】
(4)甲组同学认为丙组同学提出的方法会对空气造成污染。在不借助其它试剂和仪器的情况下,除去废液中对空气造成污染的物质,建议最好先在废液中加入过量的下面 (填选项序号)试剂。

【猜想与假设】猜想一:CaCl2猜想二:CaCl2和HCl
【查阅资料】CaCl2溶液呈中性
【探究活动一】取少量废液等分成2份,甲、乙两组同学分别利用其中一份进行如下探究:
(1)甲组同学向废液中滴加紫色石蕊溶液,溶液变成
乙组同学用图1装置进行实验,将80mL一定质量分数的碳酸钠溶液逐滴加入废液,测得数据如图2。
【数据分析】乙组同学对图2数据进行讨论分析,证明猜想二成立。
(2)I.a点的实验现象为
Ⅱ.b点发生反应的化学方程式为
Ⅲ.c点对应溶液中全部溶质的化学式为
【探究活动二】
(3)丙组同学提出直接蒸发溶剂可从剩余废液中回收纯净CaCl2,理由是
【交流与反思】
(4)甲组同学认为丙组同学提出的方法会对空气造成污染。在不借助其它试剂和仪器的情况下,除去废液中对空气造成污染的物质,建议最好先在废液中加入过量的下面 (填选项序号)试剂。
| A.CaO | B.Ca(OH)2 | C.CaCO3 |
您最近一年使用:0次
8 . 实验小组同学对密闭体系中影响蜡烛燃烧时间的因素进行探究。
(1)猜想与假设:蜡烛高度,蜡烛______ ,烛芯长度,等均会影响蜡烛燃烧时间。
【探究活动一】探究蜡烛高度,烛芯长度对燃烧时间的影响。
实验操作:小组同学分别将下列点燃的蜡烛放置于玻璃片上,将集气瓶倒扣在玻璃片上,记录从倒扣集气瓶至蜡烛熄灭的时间。
解释与结论:
(2)为了得到正确结论,该小组同学在设计实验方案、进行实验操作时还注意了___ 的问题。
(3)表中x的取值范围是______ 。
(4)实验①②③的目的是______ 。
(5)该小组同学认为比较实验①④没有价值,他们的理由是______ 。
【探究活动二】探究氧气的浓度对燃烧时间的影响。
实验操作:用高度均为3cm、烛芯长度均为0.5cm的蜡烛进行实验,集气瓶中的气体用不同体积比的氧气和氮气填充,操作时同样注意(1)的问题,实验结果如图2所示。
解释与结论:
(6)图中a点对应实验与探究活动一中实验②中蜡烛燃烧时间接近,原因是________ 。
反思与评价:
(7)同学们发现氧气体积分数提升至50%以上时,发现蜡烛燃烧更剧烈,烛芯长度变大和蜡烛高度变小越显著,蜡烛燃烧时间却变短。结合活动一分析蜡烛燃烧时间变短原因是________ 。
(8)除了探究密闭体系中影响蜡烛燃烧时间的因素外,你对蜡烛还想研究的问题是_____ (写出1条即可)。
(1)猜想与假设:蜡烛高度,蜡烛
【探究活动一】探究蜡烛高度,烛芯长度对燃烧时间的影响。
实验操作:小组同学分别将下列点燃的蜡烛放置于玻璃片上,将集气瓶倒扣在玻璃片上,记录从倒扣集气瓶至蜡烛熄灭的时间。

| 实验序号 | 蜡烛高度/cm | 烛芯长度/cm | 燃烧时间/s |
| ① | 1 | 0.5 | 17.58 |
| ② | 3 | 0.5 | 11.40 |
| ③ | 5 | 0.5 | 8.99 |
| ④ | 2 | 0.2 | 16.01 |
| ⑤ | 2 | 0.5 | x |
| ⑥ | 2 | 0.7 | 11.06 |
(2)为了得到正确结论,该小组同学在设计实验方案、进行实验操作时还注意了
(3)表中x的取值范围是
(4)实验①②③的目的是
(5)该小组同学认为比较实验①④没有价值,他们的理由是
【探究活动二】探究氧气的浓度对燃烧时间的影响。
实验操作:用高度均为3cm、烛芯长度均为0.5cm的蜡烛进行实验,集气瓶中的气体用不同体积比的氧气和氮气填充,操作时同样注意(1)的问题,实验结果如图2所示。
解释与结论:
(6)图中a点对应实验与探究活动一中实验②中蜡烛燃烧时间接近,原因是
反思与评价:
(7)同学们发现氧气体积分数提升至50%以上时,发现蜡烛燃烧更剧烈,烛芯长度变大和蜡烛高度变小越显著,蜡烛燃烧时间却变短。结合活动一分析蜡烛燃烧时间变短原因是
(8)除了探究密闭体系中影响蜡烛燃烧时间的因素外,你对蜡烛还想研究的问题是
您最近一年使用:0次
解题方法
9 . 某课外化学兴趣小组发现木炭与浓硫酸加热后产生了气体,该气体有刺激性气味,能使澄清的石灰水变浑浊。同学们在老师的指导下对该气体成分进行了探究。
【提出问题】该气体的成分是什么?
【猜想】
(1)猜想一:该气体是CO2;猜想二:该气体是_______ ;猜想三:该气体是SO2和CO2。
【查阅资料】
①SO2能与酸性高锰酸钾溶液反应,使其褪色。
②SO2+Ca(OH)2=CaSO3↓+H2O
【实验设计】
(2)装置B中出现_______ 现象,说明气体中含有SO2。装置B中高锰酸钾必须足量的原因是_______ 。
(3)装置C中澄清石灰水变浑浊,说明气体中含有CO2,请写出反应的化学方程式_______ 。
【实验结论】猜想三成立。
【反思交流】
(4)有同学认为,木炭与浓硫酸加热后生成的产物中,除上述已验证的物质外,至少还有一种产物,理由是_______ 。
【提出问题】该气体的成分是什么?
【猜想】
(1)猜想一:该气体是CO2;猜想二:该气体是
【查阅资料】
①SO2能与酸性高锰酸钾溶液反应,使其褪色。
②SO2+Ca(OH)2=CaSO3↓+H2O
【实验设计】

(2)装置B中出现
(3)装置C中澄清石灰水变浑浊,说明气体中含有CO2,请写出反应的化学方程式
【实验结论】猜想三成立。
【反思交流】
(4)有同学认为,木炭与浓硫酸加热后生成的产物中,除上述已验证的物质外,至少还有一种产物,理由是
您最近一年使用:0次
10 . 2021年12月9日“天宫课堂”开讲,航天员王亚平带来了有趣的“太空泡腾片实验”,同学们做了对照实验并进行了如下拓展探究。
【查阅资料】
(1)某品牌维生素 泡腾片的主要成分:维生素
泡腾片的主要成分:维生素 。
。
辅料:碳酸钠 、碳酸钙
、碳酸钙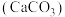 、碳酸氢钠、蔗糖、柠檬酸、橙味香料等。分析:从成分可得知,碳酸钠的俗名
、碳酸氢钠、蔗糖、柠檬酸、橙味香料等。分析:从成分可得知,碳酸钠的俗名______ 。
【对照实验】
(2)同学们将该泡腾片放入盛有水的烧杯中,观察到与太空中相似的实验现象:有大量气泡产生,同时闻到橙汁香味,从分子的角度解释能闻到香味的原因:______ 。
【提出猜想】
(3)小刚同学猜想该气泡中可能含有 ;小超同学猜想该气泡可能含有
;小超同学猜想该气泡可能含有______ 。
【设计实验】
(4)探究气体成分。
【反思评价】
(5)请写出日常生活中保存维生素 泡腾片的方法
泡腾片的方法______ 。
【拓展延伸】检验气体时,要注意气体的纯度,以防止杂质的干扰。
【查阅资料】
(1)某品牌维生素
 泡腾片的主要成分:维生素
泡腾片的主要成分:维生素 。
。辅料:碳酸钠
 、碳酸钙
、碳酸钙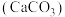 、碳酸氢钠、蔗糖、柠檬酸、橙味香料等。分析:从成分可得知,碳酸钠的俗名
、碳酸氢钠、蔗糖、柠檬酸、橙味香料等。分析:从成分可得知,碳酸钠的俗名【对照实验】
(2)同学们将该泡腾片放入盛有水的烧杯中,观察到与太空中相似的实验现象:有大量气泡产生,同时闻到橙汁香味,从分子的角度解释能闻到香味的原因:
【提出猜想】
(3)小刚同学猜想该气泡中可能含有
 ;小超同学猜想该气泡可能含有
;小超同学猜想该气泡可能含有【设计实验】
(4)探究气体成分。
| 实验步骤 | 实验现象 | 实验结论 |
| 气泡中含有 。试管中发生反应的化学方程式为 。试管中发生反应的化学方程式为 |
【反思评价】
(5)请写出日常生活中保存维生素
 泡腾片的方法
泡腾片的方法【拓展延伸】检验气体时,要注意气体的纯度,以防止杂质的干扰。
您最近一年使用:0次




