名校
解题方法
1 . 土壤是地球的“皮肤”,不同“肤色”的背后蕴藏着生命密码。允公允能化学实践小组的同学们对校园内的紫色土产生了极大的兴趣,开启了项目学习之旅。
【信息检索】
①目前重庆的土壤类型有红壤、黄壤、紫色土、山地草甸土等12种。其中最典型的是紫色土,因其含有较多的Fe2O3,所以呈紫色。紫色土中还可能含有极少量的Fe2(SO4)3、FeCl3等物质。
②无色的硫氰化钾(KSCN)溶液遇含Fe3+的溶液,溶液会呈血红色。
③溶液中Fe3+浓度太低,溶液可能呈无色。
【实验准备】同学们在校园花坛里取少量紫色土带回实验室,在土壤样品中加入足量的蒸馏水浸泡一段时间,搅拌、静置、过滤、洗涤得到滤渣和无色滤液,并将滤渣烘干。
任务一:验证紫色土中含有较多的Fe2O3
【进行实验1】
(1)
任务二:验证紫色土中含有极少量的Fe2(SO4)3、FeCl3
【进行实验2】
(2)
【反思评价】
(3)步骤②中发生反应的化学方程式为____________________ 。
(4)有同学认为步骤③不能证明紫色土中含有Cl﹣,理由是____________________ 。
【成果分享】在项目化学习的成果报告中,同学们认为我们周围的物质都是由许许多多的化学元素组成的,学好化学可以帮助我们更好的认识世界。
【信息检索】
①目前重庆的土壤类型有红壤、黄壤、紫色土、山地草甸土等12种。其中最典型的是紫色土,因其含有较多的Fe2O3,所以呈紫色。紫色土中还可能含有极少量的Fe2(SO4)3、FeCl3等物质。
②无色的硫氰化钾(KSCN)溶液遇含Fe3+的溶液,溶液会呈血红色。
③溶液中Fe3+浓度太低,溶液可能呈无色。
【实验准备】同学们在校园花坛里取少量紫色土带回实验室,在土壤样品中加入足量的蒸馏水浸泡一段时间,搅拌、静置、过滤、洗涤得到滤渣和无色滤液,并将滤渣烘干。
任务一:验证紫色土中含有较多的Fe2O3
【进行实验1】
(1)
| 实验操作 | 实验现象 | 实验结论 |
| 取少量烘干的滤渣于试管中,加入 | 滤渣固体逐渐减少, | 紫色土中含有Fe2O3 |
任务二:验证紫色土中含有极少量的Fe2(SO4)3、FeCl3
【进行实验2】
(2)
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量无色滤液于试管中,滴加几滴硫氰化钾溶液 | 紫色土中含有Fe3+ | |
| ②另取少量无色滤液于试管中,滴加几滴氯化钡溶液和足量的稀盐酸。 | 产生白色沉淀 | 紫色土中含有 |
| ③取步骤②中的上层清液于试管中,向其中滴加几滴硝酸银溶液和过量的稀硝酸。 | 紫色土中含有Cl﹣ |
【反思评价】
(3)步骤②中发生反应的化学方程式为
(4)有同学认为步骤③不能证明紫色土中含有Cl﹣,理由是
【成果分享】在项目化学习的成果报告中,同学们认为我们周围的物质都是由许许多多的化学元素组成的,学好化学可以帮助我们更好的认识世界。
您最近一年使用:0次
名校
解题方法
2 . 化学反应在防治环境污染中扮演了重要角色。某工厂废气中的SO2,处理方式之一为:2SO2+O2+4NaOH=2Na2SO4+2H2O。若处理25.6tSO2,加入一定质量的20%的NaOH溶液,恰好完全反应,试计算:
[已知:相对分子质量为SO264;O232;NaOH40;Na2SO4142]
(1)Na2SO4中S和O的质量之比为________ 。
(2)处理过程中需加入20%的NaOH溶液的质量是多少?
(3)最后所得溶液中Na2SO4的质量分数为多少?(结果保留到0.1%)
[已知:相对分子质量为SO264;O232;NaOH40;Na2SO4142]
(1)Na2SO4中S和O的质量之比为
(2)处理过程中需加入20%的NaOH溶液的质量是多少?
(3)最后所得溶液中Na2SO4的质量分数为多少?(结果保留到0.1%)
您最近一年使用:0次
名校
解题方法
3 . 锡在材料、医药、化工等方面有广泛的应用,锡精矿(主要成分为SnO2)中主要有Fe、S、Pb等杂质元素。如图为锡的冶炼工艺流程。
回答下列问题:
(1)烟尘和烟气中的主要杂质元素是_____ (填元素符号)。
(2)酸浸滤液中的Pb2+可用Na2S与其反应生成PbS沉淀,并通过与熔融的NaOH反应获得Pb,化学反应方程式为2PbS+4NaOH═2Pb+2X+O2↑+2H2O,其中X的化学式为_________ 。为了提高酸浸时的浸出速率,可采用的方法有 ________________ (填一种即可)。
(3)还原时需加入焦炭,写出在高温条件下该反应的化学方程式____________________ 。
(4)现有含SnO2质量分数为75.5%的锡精矿200t(其它成分不含锡元素),假设以上过程中锡元素不损失,经上述反应后可制得精锡(Sn)________ t。

回答下列问题:
(1)烟尘和烟气中的主要杂质元素是
(2)酸浸滤液中的Pb2+可用Na2S与其反应生成PbS沉淀,并通过与熔融的NaOH反应获得Pb,化学反应方程式为2PbS+4NaOH═2Pb+2X+O2↑+2H2O,其中X的化学式为
(3)还原时需加入焦炭,写出在高温条件下该反应的化学方程式
(4)现有含SnO2质量分数为75.5%的锡精矿200t(其它成分不含锡元素),假设以上过程中锡元素不损失,经上述反应后可制得精锡(Sn)
您最近一年使用:0次
名校
解题方法
4 . 2024重庆“两江四岸”夜景灯饰联动展演多媒体灯光秀震撼上演,3000余架无人机上演“赛博烟花”,擦亮了重庆夜景名片。
(1)制造无人机螺旋桨的材料应具有的优良性能是 (填序号)。
(2)制造无人机主要用铝合金,是因为铝合金密度小且抗腐蚀性能强。铝具有很好的抗腐蚀性的原因是_______ (用化学方程式表示)。
(3)为了探究无人机材料中铝、铁、铜三种金属活动性强弱,某同学设计了下列实验(每步均充分反应),其中能达到目的的是_______ (填序号)。
①稀盐酸中加入足量铁后,再加铜粉,最后加入铝粉
②AlCl3溶液中加入足量铁粉后,再加入CuCl2溶液
③AlCl3溶液中加入足量铜粉后,再加入铁粉
(4)无人机上使用了锂电池。金属锂比铁活泼,请写出金属锂(Li)与稀盐酸反应的方程式_______ 。
(1)制造无人机螺旋桨的材料应具有的优良性能是 (填序号)。
| A.熔点低 | B.密度大 | C.强度高 |
(3)为了探究无人机材料中铝、铁、铜三种金属活动性强弱,某同学设计了下列实验(每步均充分反应),其中能达到目的的是
①稀盐酸中加入足量铁后,再加铜粉,最后加入铝粉
②AlCl3溶液中加入足量铁粉后,再加入CuCl2溶液
③AlCl3溶液中加入足量铜粉后,再加入铁粉
(4)无人机上使用了锂电池。金属锂比铁活泼,请写出金属锂(Li)与稀盐酸反应的方程式
您最近一年使用:0次
名校
解题方法
5 . 高端芯片将引领中国“新质生产力”,高端芯片的基材主要是高纯硅,在生产硅的过程会发生反应:2Mg+SiO2 Si+2MgO,下列有关该反应的说法不正确的是
Si+2MgO,下列有关该反应的说法不正确的是
 Si+2MgO,下列有关该反应的说法不正确的是
Si+2MgO,下列有关该反应的说法不正确的是| A.该反应的基本反应类型为置换反应 |
| B.在反应中SiO2作氧化剂 |
| C.在反应中体现了Mg的还原性 |
| D.在反应中Mg反生了还原反应 |
您最近一年使用:0次
名校
解题方法
6 . 下列实验方案设计合理的是
| 选项 | 实验目的 | 实验方案 |
| A | 除去KCl溶液中的K2CO3 | 加过量的BaCl2溶液,过滤 |
| B | 分离碳酸钙和氯化钙的混合物 | 加适量的稀盐酸,过滤 |
| C | 鉴别二氧化碳与一氧化碳 | 湿润的pH试纸 |
| D | 除去四氧化三铁中混有的铁 | 在空气中点燃 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 下列对传统文化隐含的化学原理的分析错误的是
| 选项 | 出处 | 阐述 | 隐含的化学原理 |
| A | 《山亭夏日》 | “水晶帘动微风起,满架蔷微一院香” | 分子在不断运动 |
| B | 《天工开物》 | “凡石灰,经火焚炼为用。成质之后,入水永劫不坏” | “经火焚炼”涉及高温煅烧石灰石 |
| C | 《肘后备急方》 | “青蒿一握,以水二升渍,绞取汁 | “绞取汁”的原理与“过滤”的原理相似 |
| D | 《梦溪笔谈》 | “熬胆矾铁釜,久之亦化为铜” | 2Fe+3CuSO4═3Cu+Fe2(SO4)3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 板蓝根中某有效成分的化学式为C9H7NO2。下列对该成分描述正确的是
| A.分子中含有18个原子 |
| B.该成分属于有机化合物 |
| C.完全燃烧只生成二氧化碳和水 |
| D.构成该成分的分子由碳、氢、氮、氧四种元素组成 |
您最近一年使用:0次
名校
解题方法
9 . 第十九届亚洲运动会在杭州成功举办,亚运会充满了“化学元素”。下列属于有机高分子材料的是
| A.“大莲花”场馆的主体结构材料——钢 |
| B.场馆顶部的覆盖膜——聚四氟乙烯 |
| C.场地的防滑涂层——石墨烯 |
| D.主火炬使用的可再生燃料——甲醇 |
您最近一年使用:0次
10 . 已知甲、乙、Na2CO3三种物质的物质类别不同,“—”表示相连的两种物质能发生化学反应,“→”表示两端的物质通过一步反应可以转化,下列说法不正确的是
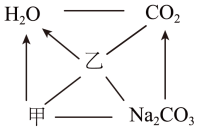
| A.甲可能是稀盐酸 | B.乙一定是碱 |
| C.乙与CO2的反应属于复分解反应 | D.甲→H2O可能产生气泡 |
您最近一年使用:0次



