解题方法
1 . 绿茶中含有茶氨酸(化学式为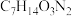 ),有提高记忆力的功能。请计算:
),有提高记忆力的功能。请计算:
(1)茶氨酸的相对分子质量为______ 。
(2)茶氨酸分子中碳、氢、氧、氮的原子个数比是______ 。
(3)______ g茶氨酸中含1.4g氮元素。
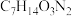 ),有提高记忆力的功能。请计算:
),有提高记忆力的功能。请计算:(1)茶氨酸的相对分子质量为
(2)茶氨酸分子中碳、氢、氧、氮的原子个数比是
(3)
您最近一年使用:0次
解题方法
2 . 推理是一种重要的研究和学习方法。下列推理正确的是
| A.酸、碱、盐的溶液能导电,所以酸、碱、盐的溶液中一定含有自由移动的离子 |
| B.复分解反应会生成沉淀、气体或水,所以有沉淀、气体或水生成的反应一定是复分解反应 |
C.常温下,酸雨的 ,所以 ,所以 的雨水一定是酸雨 的雨水一定是酸雨 |
| D.酸性溶液能使紫色石蕊溶液变红,所以能使紫色石蕊溶液变红的溶液一定是酸溶液 |
您最近一年使用:0次
解题方法
3 . 下列实验现象记录正确的是( )
| A.蜡烛在空气中燃烧,生成二氧化碳和水 |
| B.将硝酸铵固体放到水中,温度升高 |
| C.将铝丝插入硫酸铜溶液中,铝丝表面覆盖一层红色固体 |
| D.向氢氧化钠溶液中滴加硫酸铁溶液生成红棕色沉淀 |
您最近一年使用:0次
解题方法
4 . 下列实验方案设计正确的是
| 选项 | 实验目的 | 实验方案 |
| A | 检验氢氧化钠是否变质 | 加入足量稀盐酸,观察是否产生气泡 |
| B | 分离木炭粉和铁粉的混合物 | 加入足量稀硫酸,过滤、洗涤、干燥 |
| C | 除去O2中混有的CO | 通过灼热的氧化铜 |
| D | 除去CuCl2溶液中混有的NaCl | 加入足量的NaOH溶液,过滤,向滤渣中加入适量稀盐酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 物质在溶解时速率会受到哪些因素的影响?以硫酸铜为例进行如下探究。
【提出假设】
(1)假设一:温度因素;温度越高,硫酸铜晶体溶解速率越快。
假设二:搅拌因素;搅拌能加快硫酸铜晶体溶解速率。
假设三:颗粒大小因素;______ 。
【进行实验】
(2)设计实验验证假设二。
【反思评价】
(3)在上述因素中,能改变物质溶解度的因素是______ 。
(4)用分子观点解释温度的影响______ 。
(5)在本实验中搅拌能加快晶体溶解速率的原因______ 。
(6)要使试管里的固体加速溶解,常采用的方法是______ 。
【提出假设】
(1)假设一:温度因素;温度越高,硫酸铜晶体溶解速率越快。
假设二:搅拌因素;搅拌能加快硫酸铜晶体溶解速率。
假设三:颗粒大小因素;
【进行实验】
(2)设计实验验证假设二。
| 实验操作 | 实验现象 | 实验结论 |
| 在2个大小相同的烧杯中,分别注入温度相同的100mL水,再同时向烧杯中各加入一药匙颗粒大小相同的硫酸铜晶体,用玻璃棒搅拌其中一个烧杯 | 在搅拌的情况下,硫酸铜晶体溶解得 | 假设二正确 |
【反思评价】
(3)在上述因素中,能改变物质溶解度的因素是
(4)用分子观点解释温度的影响
(5)在本实验中搅拌能加快晶体溶解速率的原因
(6)要使试管里的固体加速溶解,常采用的方法是
您最近一年使用:0次
解题方法
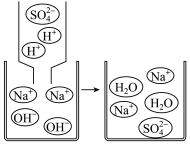
6 . 如图是小明用来描述某两种溶液反应的微观实质。请按要求填空。______ 。
(2)该反应的化学方程式为______ 。
(3)该反应的微观实质可表示为 。以此类推,当氯化钡溶液和稀硫酸反应时,其微观实质可表示为
。以此类推,当氯化钡溶液和稀硫酸反应时,其微观实质可表示为______ 。
(4)从微观角度看,氢氧化钠溶液和澄清石灰水具有相似化学性质的原因是______ 。
(2)该反应的化学方程式为
(3)该反应的微观实质可表示为
 。以此类推,当氯化钡溶液和稀硫酸反应时,其微观实质可表示为
。以此类推,当氯化钡溶液和稀硫酸反应时,其微观实质可表示为(4)从微观角度看,氢氧化钠溶液和澄清石灰水具有相似化学性质的原因是
您最近一年使用:0次
7 . 下列除杂设计(括号内为杂质)正确的是
| 序号 | 物质 | 除杂试剂 | 操作 |
| A | 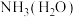 | 浓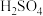 | 将混合气体通过盛有浓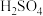 的洗气瓶 的洗气瓶 |
| B | 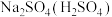 | NaOH | 加入适量NaOH溶液至 |
| C | Cu(Zn) | 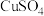 | 滴加过量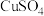 溶液,反应后过滤、洗涤、烘干 溶液,反应后过滤、洗涤、烘干 |
| D | 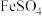 溶液( 溶液(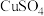 ) ) | Zn | 加入适量的锌粉,充分反应后过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
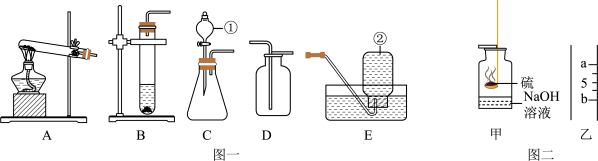
8 . 根据如图所示实验装置图,回答有关问题。______ 。仪器②的用途为______ 。
(2)实验室用高锰酸钾制取氧气的发生装置是______ (填字母)。实验室制取二氧化碳的化学方程式为______ ,选用的收集装置是______ (填字母)。
(3)实验室可用氧化钙固体与浓氨水在常温下混合制取少量氨气,为了得到平稳的氨气流,选用的发生装置是______ (填字母)。
(4)用如图二中的甲所示装置做硫在氧气中燃烧的实验,燃烧结束后取出燃烧匙,立即用玻璃片盖住瓶口并振荡。若将集气瓶倒转,发现玻璃片被“吸住”而不掉下来,其原因是______ 。为完成上述实验,用10mL量筒量取6.0mL氢氧化钠溶液,读数时量筒内的液体凹液面最低处应与图乙中______ (填“a”或“b”)处刻度线保持水平。
(2)实验室用高锰酸钾制取氧气的发生装置是
(3)实验室可用氧化钙固体与浓氨水在常温下混合制取少量氨气,为了得到平稳的氨气流,选用的发生装置是
(4)用如图二中的甲所示装置做硫在氧气中燃烧的实验,燃烧结束后取出燃烧匙,立即用玻璃片盖住瓶口并振荡。若将集气瓶倒转,发现玻璃片被“吸住”而不掉下来,其原因是
您最近一年使用:0次
9 . 某同学配制50g9%的氯化钠溶液,整个操作过程如图所示。请回答下列问题。______ (填序号,下同),其中操作错误的是______ 。
(2)需量取水______ mL,量取水时选用的量筒量程最合适的是______ (填字母)。
A.10mL B.25mL C.50mL D.100mL
(3)若用上述操作配制溶液,则所配溶液中氯化钠的质量分数会______ (填“偏大”“偏小”或“无影响”)。

(2)需量取水
A.10mL B.25mL C.50mL D.100mL
(3)若用上述操作配制溶液,则所配溶液中氯化钠的质量分数会
您最近一年使用:0次
解题方法
10 . Ⅰ.利用工业或实验产生的废液回收金属,具有环保和节约的双重意义。某同学对含 、
、 、
、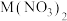 的实验室废弃混合溶液进行探究,流程如下(
的实验室废弃混合溶液进行探究,流程如下( 表示一种金属元素)。
表示一种金属元素)。
(1)滤液 中可能含有的溶质
中可能含有的溶质______ 。
(2)固体甲中含有的金属是______ 。
Ⅱ.如图 、
、 、
、 、
、 、
、 、
、 为初中化学常见的六种物质。其中
为初中化学常见的六种物质。其中 、
、 、
、 是酸、碱、盐,固体
是酸、碱、盐,固体 和
和 的浓溶液都可作干燥剂,
的浓溶液都可作干燥剂, 是赤铁矿的主要成分(图中“-”表示两种物质间能发生反应,“
是赤铁矿的主要成分(图中“-”表示两种物质间能发生反应,“ ”表示某一种物质经一步反应可转化为另一种物质,部分反应物和生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质)。请回答下列问题。
”表示某一种物质经一步反应可转化为另一种物质,部分反应物和生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质)。请回答下列问题。 的化学式:
的化学式:______ 。
(4) 和
和 反应的化学方程式为
反应的化学方程式为______ 。
 、
、 、
、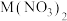 的实验室废弃混合溶液进行探究,流程如下(
的实验室废弃混合溶液进行探究,流程如下( 表示一种金属元素)。
表示一种金属元素)。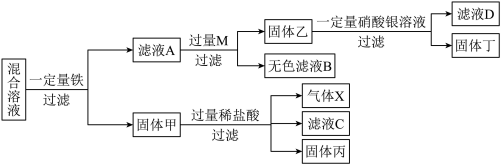
(1)滤液
 中可能含有的溶质
中可能含有的溶质(2)固体甲中含有的金属是
Ⅱ.如图
 、
、 、
、 、
、 、
、 、
、 为初中化学常见的六种物质。其中
为初中化学常见的六种物质。其中 、
、 、
、 是酸、碱、盐,固体
是酸、碱、盐,固体 和
和 的浓溶液都可作干燥剂,
的浓溶液都可作干燥剂, 是赤铁矿的主要成分(图中“-”表示两种物质间能发生反应,“
是赤铁矿的主要成分(图中“-”表示两种物质间能发生反应,“ ”表示某一种物质经一步反应可转化为另一种物质,部分反应物和生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质)。请回答下列问题。
”表示某一种物质经一步反应可转化为另一种物质,部分反应物和生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质)。请回答下列问题。
 的化学式:
的化学式:(4)
 和
和 反应的化学方程式为
反应的化学方程式为
您最近一年使用:0次



