| A.氧化物含有氧元素,所以含有氧元素的化合物一定是氧化物 |
| B.离子是显电性的微粒,所以显电性的微粒一定是离子 |
| C.化学变化伴随着能量变化,所以有能量变化的一定是化学变化 |
| D.某物质在氧气中充分燃烧生成H2O和CO2,所以该物质一定含有C、H元素 |
| A.碱溶液能使无色酚酞溶液变红,那么能使无色酚酞变红的溶液一定呈碱性 |
| B.离子是带电的微粒,因此带电荷的微粒一定是离子 |
| C.中和反应生成盐和水,因此有盐和水生成的一定是中和反应 |
| D.溶液是均一、稳定的,因此均一、稳定的液体一定是溶液 |
3 . 科学探究和证据推理是化学学科的核心素养。化学兴趣小组对“测定空气中氧气的含量”实验进行探究,并基于证据进行推理分析。
(一)氧气是参与“氧循环”的重要物质。
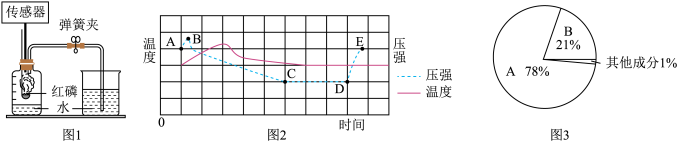
(1)图3为空气成分示意图,物质A是
(2)若测出空气中氧气体积分数小于1/5,可能的原因是
(3)利用图1装置测定空气中氧气含量并结合传感器技术,测得实验过程中容器内气体压强、温度的变化趋势如图2所示。请结合实验原理,解释BC段气体压强变化的原因:
(二)Ι用红磷测定空气中氧气的含量
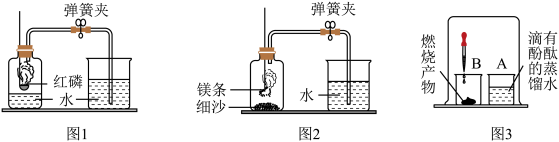
(4)写出红磷在空气中燃烧的文字表达式:
(5)某同学利用图1所示装置进行实验,步骤如下:
①用弹簧夹夹紧胶皮管;
②点燃燃烧匙内的红磷,立即伸入瓶中并塞紧瓶塞;
③
④观察并记录水面的变化情况。多次实验发现,集气瓶内水平面上升始终小于1/5。
同学们查阅资料得知,当空气中氧气的体积分数降至约为7%以下时,红磷不再燃烧。由此可知,燃烧红磷法测定结果不够准确的原因的是
Ⅱ用镁条测定空气中氧气的含量
(6)某同学进行图2所示实验时发现,产物中有少许黄色固体。
【提出问题】黄色固体是什么呢?
【查阅资料】
①氧化镁为白色固体;
②镁能与空气中的氮气反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水反应生成氨气
【做出猜想】黄色固体为Mg3N2
【实验过程】进行图3所示实验:取燃烧产物于烧杯B中,加入适量水,然后用大烧杯罩住小烧杯A和B。
【实验结论】观察到的现象
【反思交流】进行图2所示实验时,在确保规范操作的前提下,该同学所测得的空气中氧气的体积分数
| A.化合反应生成物质只有一种,所以有一种物质生成的反应是化合反应 |
| B.制取氧气必须检查装置气密性,所以制取气体都要检查装置的气密性 |
| C.二氧化锰是过氧化氢分解的催化剂,所以任何反应都可用二氧化锰做催化剂 |
| D.化学变化常常伴随发光放热的现象,所以有发光放热的变化一定属于化学变化 |
| A.催化剂在化学反应前后质量不变,但是在化学反应前后质量不变的不一定是催化剂 |
| B.中和反应一定有盐和水生成,所以有盐和水生成的反应一定是中和反应 |
| C.酸溶液都能使紫色石蕊溶液变红,所以使紫色石蕊溶液变红的一定是酸溶液 |
| D.溶液具有均一性和稳定性,则具有均一性和稳定性的液体一定是溶液 |
| A.单质是由同种元素组成的,所以由同种元素组成的物质一定是单质 |
| B.在同一化合物中,若金属元素显正价,则非金属元素一定显负价 |
| C.燃烧伴有发光、放热现象,所以有发光、放热的现象就一定是燃烧 |
| D.元素是质子数相同的一类原子的总称,因此质子数相同的原子一定属于同种元素 |
| A.单质中只有一种元素,含有一种元素的物质一定是单质 |
| B.置换反应能生成单质,则生成单质的反应一定是置换反应 |
| C.酸能使石蕊溶液变红,则能使石蕊溶液变红的一定是酸 |
| D.点燃可燃性气体前要验纯,则点燃氢气前要验纯 |
| A.单质是由同种元素组成的,由同种元素组成的物质一定是单质 |
| B.同种元素的微粒中质子数相同,质子数相同的微粒一定属于同种元素 |
| C.分子由原子构成,分子的体积和质量一定比原子大 |
| D.化学反应遵守质量守恒定律,铁丝在氧气中燃烧后质量虽然增加但仍然符合质量守恒定律 |
| A.离子是带电的粒子,则带电的粒子一定是离子 |
| B.溶液是均一、稳定的,则均一、稳定的液体一定是溶液 |
| C.氧化物都含氧元素,则含氧元素的物质一定是氧化物 |
| D.化合物是由不同种元素组成的纯净物,则由不同种元素组成的纯净物一定是化合物 |
| A.置换反应有单质和化合物生成,所以有单质和化合物生成的反应一定是置换反应 |
| B.物质燃烧的反应都能放出热量,所以能放出热量的反应一定是物质燃烧的反应 |
| C.催化剂在化学反应前后质量不变,所以化学反应前后质量不变的物质一定是催化剂 |
| D.化合物中含有不同种元素,所以由不同种元素组成的纯净物一定是化合物 |



