解题方法
1 . 如图是元素周期表中的一格。铝的相对原子质量为_____ ;铝的原子结构示意图为____ ;铝元素在元素周期表中位于第______ 周期。


您最近一年使用:0次
解题方法
2 . 在宏观、微观和符号之间建立联系是化学学科的重要思维方式。

(1)A微粒属于___________ (填“原子”、“阳离子”或“阴离子”)。
(2)B、C属于同种元素的原因是___________ 。
(3)原子序数为12的元素与D元素组成的化合物的化学式是___________ 。
(4)乙图为硒的原子结构示意图与元素周期表中的信息,其相对原子质量为___________ ,它与丙图中___________ (填元素名称)的化学性质相似。

(1)A微粒属于
(2)B、C属于同种元素的原因是
(3)原子序数为12的元素与D元素组成的化合物的化学式是
(4)乙图为硒的原子结构示意图与元素周期表中的信息,其相对原子质量为
您最近一年使用:0次
3 . 好茶看茶叶。茶叶中含有多种成分。
(1)茶叶含氟较高,对预防龋齿有一定效果。这里的“氟”指的是___________ (填“元素”或“单质”)。
(2)茶叶中的硒有防癌作用。硒原子结构示意图如图所示,x=___________ ,硒元素在化学反应中易___________ (填“得到”或“失去”)电子。

(3)茶叶中的茶多酚具有强血管降血脂的作用。某种茶多酚的化学式为C6H6O2,其氢、氧元素的质量比为___________ 。
(1)茶叶含氟较高,对预防龋齿有一定效果。这里的“氟”指的是
(2)茶叶中的硒有防癌作用。硒原子结构示意图如图所示,x=

(3)茶叶中的茶多酚具有强血管降血脂的作用。某种茶多酚的化学式为C6H6O2,其氢、氧元素的质量比为
您最近一年使用:0次
解题方法
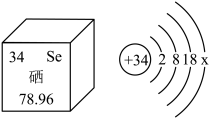
4 . 富硒水稻具有抗癌、提高人体免疫力等多种特殊保健功能。如图是硒元素在元素周期表中的信息及其原子结构示意图,则硒原子的原子序数是______ , 的值
的值______ 。
 的值
的值
您最近一年使用:0次
解题方法
5 . 探秘原子结构
人类探索原子结构的奥秘,经历了漫长的过程。
(1)1897年,汤姆森发现了__________ 提出原子是可分的,并提出原子模型如图所示。

(2)1911年,物理学家卢瑟福用一束带正电的、质量比电子大得多的高速 粒子轰击金箔,预期这些
粒子轰击金箔,预期这些 粒子会毫不费力地击穿金原子,到达对面的探测板上,结果发现:绝大多数
粒子会毫不费力地击穿金原子,到达对面的探测板上,结果发现:绝大多数 粒子穿过金箔后仍保持原来的运动方向,少数
粒子穿过金箔后仍保持原来的运动方向,少数 粒子发生了较大角度的偏转,极少数
粒子发生了较大角度的偏转,极少数 粒子被反弹回来。
粒子被反弹回来。
①当 粒子轰击金箔时,下图四条运动轨迹中不可能出现的是(填序号)
粒子轰击金箔时,下图四条运动轨迹中不可能出现的是(填序号)__________ 。

②卢瑟福根据实验现象推测:原子中心有一个结构(原子核),它具有如下特点____________________ 。
(3)用高能粒子轰击原子核是研究微观粒子的一种常用方法。
1938年,德国科学家哈恩用中子轰击铀235原子(质子数为92,相对原子质量是235,元素符号为U),得到了质子数为56的钡原子,并用下图模型定义该变化。

①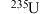 原子中,中子数是
原子中,中子数是__________ 。
②上述变化是不是化学变化__________ ,理由是______________________________ 。
(4)随着研究的不断深入,科学家逐渐揭开构成物质的粒子及其规律。请用物质组成和构成的化学术语填空。其中②、⑤、⑥、⑧为带电的粒子。

①__________ ;②__________ ;③__________ ;④__________ ;⑤__________ ;⑥__________ ;⑦__________ ;⑧__________ 。
(5)分析原子结构及原子的发现历程,以下观点正确的是__________。
人类探索原子结构的奥秘,经历了漫长的过程。
(1)1897年,汤姆森发现了

(2)1911年,物理学家卢瑟福用一束带正电的、质量比电子大得多的高速
 粒子轰击金箔,预期这些
粒子轰击金箔,预期这些 粒子会毫不费力地击穿金原子,到达对面的探测板上,结果发现:绝大多数
粒子会毫不费力地击穿金原子,到达对面的探测板上,结果发现:绝大多数 粒子穿过金箔后仍保持原来的运动方向,少数
粒子穿过金箔后仍保持原来的运动方向,少数 粒子发生了较大角度的偏转,极少数
粒子发生了较大角度的偏转,极少数 粒子被反弹回来。
粒子被反弹回来。①当
 粒子轰击金箔时,下图四条运动轨迹中不可能出现的是(填序号)
粒子轰击金箔时,下图四条运动轨迹中不可能出现的是(填序号)
②卢瑟福根据实验现象推测:原子中心有一个结构(原子核),它具有如下特点
(3)用高能粒子轰击原子核是研究微观粒子的一种常用方法。
1938年,德国科学家哈恩用中子轰击铀235原子(质子数为92,相对原子质量是235,元素符号为U),得到了质子数为56的钡原子,并用下图模型定义该变化。

①
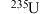 原子中,中子数是
原子中,中子数是②上述变化是不是化学变化
(4)随着研究的不断深入,科学家逐渐揭开构成物质的粒子及其规律。请用物质组成和构成的化学术语填空。其中②、⑤、⑥、⑧为带电的粒子。

①
(5)分析原子结构及原子的发现历程,以下观点正确的是__________。
| A.科学模型的建立是一个不断完善、修正的过程 |
| B.模型是一种重要的方法,人类借助模型构建,对原子的认识逐渐接近本质 |
| C.科学结论的得出要依据客观事实,面对前人的观点要敢于质疑 |
| D.科学理论的发展过程是发现并改正前人错误认识的过程 |
您最近一年使用:0次
名校
解题方法
6 . 某元素是人体中的常量元素,它在人体内99%存在于骨骼和牙齿中。该元素的原子结构示意图为:
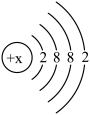
则该元素的原子序数为____________ ,该原子核外有______________ 个电子,该粒子易______ 电子,该粒子在化合物中显____________ 价。

则该元素的原子序数为
您最近一年使用:0次
2024-02-06更新
|
21次组卷
|
2卷引用:海南省文昌市文昌中2023-2024学年九年级上学期期末化学试题(重点班)
解题方法
7 . 元素周期表是我们学习和研究化学的重要工具,请根据图示回答下列问题。

(1)原子序数为18的元素名称是______ 。
(2)氧元素与硫元素具有相似化学性质的原因是_____________________________ 。
(3)写出由原子序数为8和12的两种元素组成的化合物的化学式______ 。
(4)由图1可知,同一周期的元素,它们原子的最外层电子从左至右排布的规律是_______________ 。
(5)镓常应用于电子行业,图2为镓原子的电子排布图,从中能获取的一条信息是______ 。

(1)原子序数为18的元素名称是
(2)氧元素与硫元素具有相似化学性质的原因是
(3)写出由原子序数为8和12的两种元素组成的化合物的化学式
(4)由图1可知,同一周期的元素,它们原子的最外层电子从左至右排布的规律是
(5)镓常应用于电子行业,图2为镓原子的电子排布图,从中能获取的一条信息是
您最近一年使用:0次
解题方法
8 . 如图是A、B、C微粒的结构示意图,请结合图示回答下列问题:

(1)图中A结构示意图中X=________ ;C结构示意图中y=_________ ;
(2)图中B结构示意图表示的粒子的化学符号为_____________ 。
(3)图中A与C结合形成的物质的化学式为_____________________ ;

(1)图中A结构示意图中X=
(2)图中B结构示意图表示的粒子的化学符号为
(3)图中A与C结合形成的物质的化学式为
您最近一年使用:0次
解题方法
9 . 碘元素对青少年智力发育影响很大,市售加碘盐是在食盐中加入适量碘酸钾(KIO3)。左图是超市销售的一种加碘盐标签上的部分文字说明,右图是碘离子(I-)的结构示意图。


回答下列问题:
(1)上图中x=______ 。
(2)氯化钠是由______ (填“分子”、“原子”或“离子”)构成的。
(3)碘酸钾受热易分解,反应的化学方程式为:2KIO3 3O2↑+2口。方框中填入的化学式是
3O2↑+2口。方框中填入的化学式是______ 。
(4)每袋食盐中碘酸钾的质量是______ mg(计算结果精确到0.1mg)。


回答下列问题:
(1)上图中x=
(2)氯化钠是由
(3)碘酸钾受热易分解,反应的化学方程式为:2KIO3
 3O2↑+2口。方框中填入的化学式是
3O2↑+2口。方框中填入的化学式是(4)每袋食盐中碘酸钾的质量是
您最近一年使用:0次
解题方法
10 . 模型可以反映客观现象,简单明了地表示事物及变化。
(1)人类对原子结构的探究经历了漫长的过程。1910年英国科学家卢瑟福进行了著名的 粒子袭击金箔实验,下图1是卢瑟福用
粒子袭击金箔实验,下图1是卢瑟福用  粒子袭击金箔的实验现象,请结合现象分析:
粒子袭击金箔的实验现象,请结合现象分析:

①若原子质量、正电荷在原子内均匀分布,则极少数 子就
子就_______ (填“会”或“不会”)发生大角度偏转。卢瑟福所说的除非原子的大部分质量集中到了一个“很小的结构”中,“很小的结构”指的是_______ 。
②你认为原子结构为如图2中的_______ (填字母序号)。
③图3为某原子结构模型的示意图。下列说法中不正确的是_______ (填字母序号)。
A.原子中a和 的数目一定相等
的数目一定相等
B.原子中 与
与 的数目一定相等
的数目一定相等
C.原子的质量主要集中在b和c
D.决定原子核电荷数的微粒是c的数目
(2)化学式建立了宏观与微观之间的桥梁。
①化学物质中有一种形似足球的笼状分子,称为“足球烯”(如图),化学式为 由
由_______ (填“分子”或“原子”)构成,其中碳元素化合价为_______ 。
②如图是二氧化碳的化学式“ ”所表达信息的模型,请写出其所表达的信息:
”所表达信息的模型,请写出其所表达的信息:
宏观信息:_____________ (写一条,下同);
微观信息:_____________ 。
(1)人类对原子结构的探究经历了漫长的过程。1910年英国科学家卢瑟福进行了著名的
 粒子袭击金箔实验,下图1是卢瑟福用
粒子袭击金箔实验,下图1是卢瑟福用  粒子袭击金箔的实验现象,请结合现象分析:
粒子袭击金箔的实验现象,请结合现象分析:
①若原子质量、正电荷在原子内均匀分布,则极少数
 子就
子就②你认为原子结构为如图2中的
③图3为某原子结构模型的示意图。下列说法中不正确的是
A.原子中a和
 的数目一定相等
的数目一定相等 B.原子中
 与
与 的数目一定相等
的数目一定相等C.原子的质量主要集中在b和c
D.决定原子核电荷数的微粒是c的数目
(2)化学式建立了宏观与微观之间的桥梁。
①化学物质中有一种形似足球的笼状分子,称为“足球烯”(如图),化学式为
 由
由②如图是二氧化碳的化学式“
 ”所表达信息的模型,请写出其所表达的信息:
”所表达信息的模型,请写出其所表达的信息:宏观信息:
微观信息:
您最近一年使用:0次



