名校
解题方法
1 . 尿素是一种有机氮肥,其化学式为CO(NH2)2.下列关于尿素的说法正确的是


| A.CO(NH2)2不能与碱性物质混合施用 |
| B.C、O、N、H四种原子的个数比为1∶1∶1∶4 |
C.氮元素的质量分数为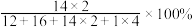 |
| D.CO(NH2)2难溶于水 |
您最近一年使用:0次
解题方法
2 . 物质甲、乙两种化合物均可灭杀新型冠状病毒,灭杀过程中有如图转化:

下列说法正确的是

下列说法正确的是
| A.乙是氧化物 |
| B.丙的水溶液能够除铁锈 |
| C.甲、乙、丙中氯元素的化合价相同 |
| D.甲、乙、丙中氯元素的质量分数依次降低 |
您最近一年使用:0次
真题
解题方法
3 . 国家对化肥的销售有明确的质量标准。为检测铵态氮肥质量的优劣,可采用铵盐与氢氧化钠反应的方法。某同学称取15g硫酸铵样品(杂质不含氮元素),与足量的NaOH混合后,放入试管中加热,发生如下反应: 。充分反应后共收集到3.4gNH3。
。充分反应后共收集到3.4gNH3。
(1)(NH4)2SO4中氮元素的质量分数______ (精确到0.1%)。
(2)样品中硫酸铵的质量(写出计算过程)。
(3)合格硫酸铵化肥中硫酸铵的质量分数需达到94.3%~99%,通过计算判断上述样品是否合格?
 。充分反应后共收集到3.4gNH3。
。充分反应后共收集到3.4gNH3。(1)(NH4)2SO4中氮元素的质量分数
(2)样品中硫酸铵的质量(写出计算过程)。
(3)合格硫酸铵化肥中硫酸铵的质量分数需达到94.3%~99%,通过计算判断上述样品是否合格?
您最近一年使用:0次
2022-07-14更新
|
1043次组卷
|
9卷引用:2023年中考风向标-江苏-综合应用与计算
(已下线)2023年中考风向标-江苏-综合应用与计算(已下线)2024年中考风向标-江苏-综合应用与计算(已下线)专题14? 化学计算(七大题型)-2024年中考化学二轮热点题型归纳与变式演练(江苏通用)2022年江苏省宿迁市中考化学真题2023中考一轮复习考点微专题-专题24 化学计算-考点专练(已下线)专项12 化学计算题20题-2024年中考化学常考点必杀300题(全国通用)2023口袋书系列-专题07 化学计算公式-知识手册 提高练习湖北省黄石市阳新县国和中学2022-2023学年九年级上学期期中化学试题(已下线)第五单元 化学方程式【考题猜想】(23大题型)-2023-2024学年九年级化学上学期期末考点大串讲(人教版)
真题
解题方法
4 . 含有铵根离子( )的盐属于铵盐,兴趣小组对铵盐及相关问题进行探究。
)的盐属于铵盐,兴趣小组对铵盐及相关问题进行探究。
【了解组成】
(1)一种常见铵盐的微观模型示意图为 ,则它表示的物质是
,则它表示的物质是___________ (填化学式)。
(2)碳酸氢铵的化学式为NH4HCO3,某种碳酸氢铵样品中氮元素的质量分数是21.8%,则该碳酸氢铵样品属于___________ (填“纯净物”或“混合物”)。
【比较性质】
(3)已知硝酸铵溶液显酸性,则该溶液中含有的阳离子有 和
和___________ (填离子符号)。
(4)常见的铵盐中,仅有碳酸氢铵在常温下就能分解,放出氨气,则常温下鉴别碳酸氢铵与硫酸铵的最简便方法是___________ 。
(5)铵盐与碱混合通常会放出氨气,因此,施肥时要避免铵态氮肥与碱性物质混用。写出加热条件下硫酸铵与烧碱反应的化学方程式:___________ 。
【提出问题】氨气与氯化氢反应可以得到一种铵盐,该反应常用于探究微粒的运动性。那么,微粒运动速率与气体的相对分子质量有什么关系呢?
【查阅资料】浓盐酸靠近浓氨水时,会出现大量的白烟。
【进行实验】
将一根玻璃管放在水平桌面上,在左右两端同时塞入分别滴有浓盐酸、浓氨水的脱脂棉,再塞紧橡皮塞。稍后,在靠近浓盐酸的一端最先出现白烟,如图甲。
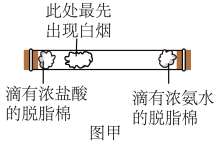
(6)浓盐酸与浓氨水未直接接触就产生白烟,是因为浓盐酸和浓氨水都具有___________ 。
(7)由图甲实验可知,相同条件下相对分子质量越小的气体,其微粒运动速率越___________ 。
【拓展延伸】
再取一根V型玻璃管,开口向上竖直放置,在左右两端同时塞入分别滴有浓盐酸、浓氨水的脱脂棉,再塞紧橡皮塞。稍后,在靠近浓氨水的一端最先出现白烟,如图乙。
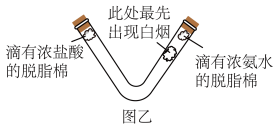
(8)图乙实验中,最先出现白烟的位置与图甲实验相反,说明相同条件下___________ 。
(9)实验中发现V型玻璃管发热,其原因是___________ 。
 )的盐属于铵盐,兴趣小组对铵盐及相关问题进行探究。
)的盐属于铵盐,兴趣小组对铵盐及相关问题进行探究。【了解组成】
(1)一种常见铵盐的微观模型示意图为
 ,则它表示的物质是
,则它表示的物质是(2)碳酸氢铵的化学式为NH4HCO3,某种碳酸氢铵样品中氮元素的质量分数是21.8%,则该碳酸氢铵样品属于
【比较性质】
(3)已知硝酸铵溶液显酸性,则该溶液中含有的阳离子有
 和
和(4)常见的铵盐中,仅有碳酸氢铵在常温下就能分解,放出氨气,则常温下鉴别碳酸氢铵与硫酸铵的最简便方法是
(5)铵盐与碱混合通常会放出氨气,因此,施肥时要避免铵态氮肥与碱性物质混用。写出加热条件下硫酸铵与烧碱反应的化学方程式:
【提出问题】氨气与氯化氢反应可以得到一种铵盐,该反应常用于探究微粒的运动性。那么,微粒运动速率与气体的相对分子质量有什么关系呢?
【查阅资料】浓盐酸靠近浓氨水时,会出现大量的白烟。
【进行实验】
将一根玻璃管放在水平桌面上,在左右两端同时塞入分别滴有浓盐酸、浓氨水的脱脂棉,再塞紧橡皮塞。稍后,在靠近浓盐酸的一端最先出现白烟,如图甲。

(6)浓盐酸与浓氨水未直接接触就产生白烟,是因为浓盐酸和浓氨水都具有
(7)由图甲实验可知,相同条件下相对分子质量越小的气体,其微粒运动速率越
【拓展延伸】
再取一根V型玻璃管,开口向上竖直放置,在左右两端同时塞入分别滴有浓盐酸、浓氨水的脱脂棉,再塞紧橡皮塞。稍后,在靠近浓氨水的一端最先出现白烟,如图乙。

(8)图乙实验中,最先出现白烟的位置与图甲实验相反,说明相同条件下
(9)实验中发现V型玻璃管发热,其原因是
您最近一年使用:0次
2022-07-05更新
|
1030次组卷
|
6卷引用:2023年中考风向标-江苏-科学探究
(已下线)2023年中考风向标-江苏-科学探究(已下线)2024年中考风向标-江苏-科学探究2022年江苏省徐州市中考化学真题(已下线)重难点10 盐和化肥-2023年中考化学【热点·重点·难点】专练(全国通用)(已下线)课题2 化学肥料(共2课时)(好题精练)-2022-2023学年九年级化学下册精品课堂课件精讲及好题精练(人教版)2023-2024九化课后作业与单元测试 人教版 第十一单元 课题2 化学肥料 课后作业
解题方法
5 . 珍爱生命,远离毒品。LSD(化学式为C20H25N3O)是一种俗称为“邮票”的新型毒品,毒性极强。下列关于C20H25N3O的说法正确的是
| A.属于有机高分子化合物 | B.由碳、氢、氮、氧四种元素组成 |
| C.氢元素质量分数最大 | D.碳、氢元素质量比为20:25 |
您最近一年使用:0次
2022-06-13更新
|
232次组卷
|
8卷引用:专题03 化学用语、化学式、物质分类、反应方程式-5年(2018-2022)中考1年模拟化学分项汇编(江苏苏州专用)
(已下线)专题03 化学用语、化学式、物质分类、反应方程式-5年(2018-2022)中考1年模拟化学分项汇编(江苏苏州专用)(已下线)2024年中考风向标-江苏-化学式分析与计算2022年江苏省苏州园区星汇学校中考三模化学试题2021年江苏省苏州市姑苏区第五初级中学校中考考前练习化学试题2023年江苏省苏州市中考一模模拟化学试题(四)2023年江苏省淮安市淮阴区中考二模化学试题2024年江苏省苏州市工业园区东沙湖学中考化学模拟试卷(一)2024年河北省中考化学仿真卷9
名校
解题方法
6 . 中国酸菜的历史颇为悠久,制作酸菜的初衷是为了延长蔬菜保存时间。酸菜的制作过程中会产生大量乳酸。下列有关乳酸(化学式为C3H6O3)的说法正确的是
| A.乳酸是一种氧化物 |
| B.乳酸中氧元素的质量分数最大 |
| C.乳酸的相对分子质量为90g |
| D.乳酸中C、H、O三种元素的质量比为1:2:1 |
您最近一年使用:0次
2022-06-08更新
|
90次组卷
|
4卷引用:专题03 化学用语、化学式、物质分类、反应方程式-5年(2018-2022)中考1年模拟化学分项汇编(江苏苏州专用)
(已下线)专题03 化学用语、化学式、物质分类、反应方程式-5年(2018-2022)中考1年模拟化学分项汇编(江苏苏州专用)2022年江苏省苏州市平江、草桥中学中考二模化学试题2022年江苏省苏州市草桥中学中考考前化学练习试题(1)(已下线)《化学式与化合价》第3课时(分层作业)-【上好课】2022-2023学年九年级化学上册同步备课系列(人教版)
解题方法
7 . NiSO4•6H2O是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电池等,可由电镀废渣(除含Ni外,还含有Cu、Zn、Fe等杂质)为原料获得。有关工艺流程如图:
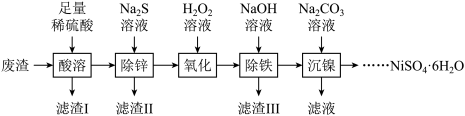
【资料】①Ni能与稀硫酸反应生成NiSO4和H2;
②H2O2溶液能将FeSO4氧化成Fe2(SO4)3;
③NiCO3是一种不溶于水、易溶于强酸的浅绿色沉淀;
④碱性条件下NiSO4转化为Ni(OH)2沉淀。
(1)“酸溶”时向废渣中加入足量稀硫酸的目的是_______ 。
(2)“除锌”时发生复分解反应,滤渣Ⅱ的成分是_______ (填化学式)。
(3)“氧化”时发生的反应为H2O2+2FeSO4+H2SO4=Fe2(SO4)3+aH2O,则a=_______ 。加入H2O2溶液时,温度不能太高的原因是_______ 。
(4)“除铁”时,控制不同的条件可以得到不同的滤渣Ⅲ.已知滤渣Ⅲ的成分与温度、pH的关系如图所示,图中阴影部分是黄铁矾钠沉淀【化学式为:Na2Fe6(SO4)4(OH)12】。下列说法正确的是 (填字母)。

(5)“沉镍”时生成NiCO3沉淀的化学方程式为_______ 。在“沉镍”时,若将NiSO4溶液滴入Na2CO3溶液中,会生成_______ (填化学式),不能得到NiCO3。
(6)由NiCO3沉淀制得NiSO4•6H2O晶体的实验步骤为:向沉淀中加入_______ 溶液,直至恰好完全溶解,转化为NiSO4溶液;蒸发浓缩、降温结晶、_______ 、洗涤并晾干。
(7)现有含Ni20%的电镀废渣100kg,经过上述工业制得NiSO4•6H2O78.9kg,则Ni的利用率为___ 。(写计算过程,结果保留一位小数。)
已知:①NiSO4•6H2O的相对分子质量为263;②利用率= ×100%
×100%

【资料】①Ni能与稀硫酸反应生成NiSO4和H2;
②H2O2溶液能将FeSO4氧化成Fe2(SO4)3;
③NiCO3是一种不溶于水、易溶于强酸的浅绿色沉淀;
④碱性条件下NiSO4转化为Ni(OH)2沉淀。
(1)“酸溶”时向废渣中加入足量稀硫酸的目的是
(2)“除锌”时发生复分解反应,滤渣Ⅱ的成分是
(3)“氧化”时发生的反应为H2O2+2FeSO4+H2SO4=Fe2(SO4)3+aH2O,则a=
(4)“除铁”时,控制不同的条件可以得到不同的滤渣Ⅲ.已知滤渣Ⅲ的成分与温度、pH的关系如图所示,图中阴影部分是黄铁矾钠沉淀【化学式为:Na2Fe6(SO4)4(OH)12】。下列说法正确的是 (填字母)。

| A.FeOOH中铁元素为+2价 |
| B.Fe2O3固体为红棕色 |
| C.若在20°C时,用H2O2氧化Fe2+,再在pH=4时除去铁,此时溶液中出现的沉淀是FeOOH和Fe(OH)3 |
| D.工业生产中若保持溶液的pH为1.8左右、温度为85~95°C时得到沉淀为黄铁矾钠 |
(6)由NiCO3沉淀制得NiSO4•6H2O晶体的实验步骤为:向沉淀中加入
(7)现有含Ni20%的电镀废渣100kg,经过上述工业制得NiSO4•6H2O78.9kg,则Ni的利用率为
已知:①NiSO4•6H2O的相对分子质量为263;②利用率=
 ×100%
×100%
您最近一年使用:0次
2022-06-01更新
|
220次组卷
|
3卷引用:非选择专练12 工业流程(25题)-2023年中考化学总复习高频考点必刷题(苏州专用)
(已下线)非选择专练12 工业流程(25题)-2023年中考化学总复习高频考点必刷题(苏州专用)2022年江苏省扬州市江都区第三中学中考二模化学试题2022年江苏省扬州市邗江实验学校蒋王分校中考三模化学试题
解题方法
8 . 中国科学家以CO2和H2为原料,经催化可转化为有机物,其微观反应原理如下图所示。下列说法正确的是
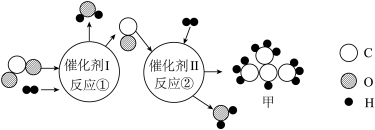
A.反应①的化学方程式为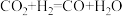 |
B.反应②中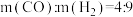 |
| C.CO是总反应的催化剂 |
| D.在甲物质中,氢元素的质量分数为17.24% |
您最近一年使用:0次
2022-05-21更新
|
297次组卷
|
8卷引用:专题02 构成物质的微粒 微粒结构与微观反应示意图-5年(2018-2022)中考1年模拟化学分项汇编(江苏苏州专用)
(已下线)专题02 构成物质的微粒 微粒结构与微观反应示意图-5年(2018-2022)中考1年模拟化学分项汇编(江苏苏州专用)2022年江苏省苏州市昆山、太仓、常熟、张家港市联考中考模拟化学试题2022年江苏省昆山、太仓、常熟、张家港市中考适应性考试化学试题2022年江苏省常州市中考适应性练习(三模)化学试题江苏省高邮市高邮镇2022-2023学年九年级下学期4月月考化学试题2024年江苏省苏州市工业园区东沙湖实验中学中考化学模拟试卷(二)(已下线)【临考满分卷】2024年中考化学临考满分卷(苏州专用)2022年新疆乌鲁木齐市第四十四中学中考一模化学试题
解题方法
9 . 一种生产学校操场跑道塑胶的新型环保材料的化学式为C15H10N2O2,下列对该物质的说法中正确的是
| A.该物质中共含有29个原子 | B.该物质碳、氧元素的质量比为15:2 |
| C.该物质中氢元素的质量分数最低 | D.该物质中含有氮分子和氧分子 |
您最近一年使用:0次
2022-05-05更新
|
108次组卷
|
7卷引用:2022江苏中考风向标-化学计算
解题方法
10 . 尿素是一种重要的化肥,它的化学式为【CO(NH2)2】。下列关于尿素的说法正确的是
| A.尿素的相对分子质量是60g |
| B.尿素属于铵态氮肥 |
| C.尿素的含氮量比碳酸氢铵高 |
| D.尿素由一氧化碳分子、氮原子和氢原子构成 |
您最近一年使用:0次



