1 . 2024年5月3日,嫦娥六号探测器成功发射,开启月球背面采样之旅。
(1)月球背面的水有固态和气态两种存在方式。
①气态水的分子间隔比固态水更___________ (填“大”或“小”)。
②水由固态变为气态的过程中,没有发生变化的是___________ (填“物理”或“化学”)性质。
(2)科研人员曾用嫦娥五号带回的月壤证实:在一定条件下,月壤中的FeO(铁橄榄石的主要成分)分解生成Fe3O4(磁铁矿的主要成分)以及单质铁。
①写出该反应的化学方程式___________ 。
②下列关于含铁物质的说法中,正确的是___________ (填序号)。
A.磁铁矿是工业炼铁的重要原料
B.铁锈的主要成分是
C.铁合金比纯铁应用更为广泛
(1)月球背面的水有固态和气态两种存在方式。
①气态水的分子间隔比固态水更
②水由固态变为气态的过程中,没有发生变化的是
(2)科研人员曾用嫦娥五号带回的月壤证实:在一定条件下,月壤中的FeO(铁橄榄石的主要成分)分解生成Fe3O4(磁铁矿的主要成分)以及单质铁。
①写出该反应的化学方程式
②下列关于含铁物质的说法中,正确的是
A.磁铁矿是工业炼铁的重要原料
B.铁锈的主要成分是

C.铁合金比纯铁应用更为广泛
您最近一年使用:0次
2 . 下列图像与实验过程对应关系正确的个数为
②锌和稀硫酸反应生成氢气
③将足量汞放在充满空气的密闭容器中持续加热
④向氢氧化钠和氯化钡的混合溶液中滴加稀硫酸

②锌和稀硫酸反应生成氢气
③将足量汞放在充满空气的密闭容器中持续加热
④向氢氧化钠和氯化钡的混合溶液中滴加稀硫酸
| A.0个 | B.1个 | C.2个 | D.3个 |
您最近一年使用:0次
真题
解题方法
3 . 锂(Li)离子电池应用广泛,有利于电动汽车的不断发展。
(1)Li___________ (填“得到”或“失去”)电子变成Li+。
(2)锂离子电池中含有铝箔,通常由铝锭打造而成,说明铝具有良好的___________ 性。
(3)锂离子电池中还含有铜箔,为验证铝和铜的金属活动性顺序,设计了如下实验:
【方案一】将铝片和铜片相互刻划,金属片上出现划痕者更活泼。
【方案二】将铝丝和铜丝表面打磨后,同时放入5mL相同的稀盐酸中,金属丝表面产生气泡者更活泼。
【方案三】将铝丝和铜丝表面打磨后,同时放入5mL相同的硝酸银溶液中,金属丝表面有银白色物质析出者更活泼。
以上方案中,你认为能达到实验目的的是___________ (填方案序号),该方案中发生反应的化学方程式为___________ 。
(1)Li
(2)锂离子电池中含有铝箔,通常由铝锭打造而成,说明铝具有良好的
(3)锂离子电池中还含有铜箔,为验证铝和铜的金属活动性顺序,设计了如下实验:
【方案一】将铝片和铜片相互刻划,金属片上出现划痕者更活泼。
【方案二】将铝丝和铜丝表面打磨后,同时放入5mL相同的稀盐酸中,金属丝表面产生气泡者更活泼。
【方案三】将铝丝和铜丝表面打磨后,同时放入5mL相同的硝酸银溶液中,金属丝表面有银白色物质析出者更活泼。
以上方案中,你认为能达到实验目的的是
您最近一年使用:0次
真题
解题方法
4 . 下列实验不能达到实验目的的是
A.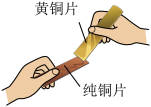 相互刻画比较硬度 相互刻画比较硬度 |
B. 验证质量守恒定律 验证质量守恒定律 |
C. 除去食盐水中的泥沙 除去食盐水中的泥沙 |
D. 检验氢气的纯度 检验氢气的纯度 |
您最近一年使用:0次
真题
5 . 已知 为初中化学的常见物质,B、C、
为初中化学的常见物质,B、C、 为单质,
为单质, 均为黑色固体,C常用于作导线,D常用作气体肥料,它们之间的转化关系如图所示(反应条件、部分产物已略去)。
均为黑色固体,C常用于作导线,D常用作气体肥料,它们之间的转化关系如图所示(反应条件、部分产物已略去)。
(1)C的化学式为_________ ,D的名称是_________ 。
(2)反应①中B的元素化合价_________ (填“升高”或“降低”)。
(3)反应②的化学方程式为_________ 。
(4) 的用途是
的用途是_________ (填一条)。
 为初中化学的常见物质,B、C、
为初中化学的常见物质,B、C、 为单质,
为单质, 均为黑色固体,C常用于作导线,D常用作气体肥料,它们之间的转化关系如图所示(反应条件、部分产物已略去)。
均为黑色固体,C常用于作导线,D常用作气体肥料,它们之间的转化关系如图所示(反应条件、部分产物已略去)。
(1)C的化学式为
(2)反应①中B的元素化合价
(3)反应②的化学方程式为
(4)
 的用途是
的用途是
您最近一年使用:0次
真题
解题方法
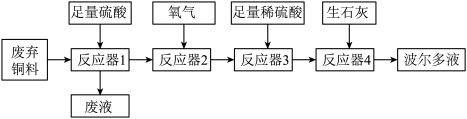
6 . “波尔多液”是使用历史最长的一种杀菌剂。如图是利用废弃铜料(只含有铜一定量的铁)制备“波尔多液”的流程。
(1)反应器1产生的废液中含有的溶质有_________ (写一种即可)。
(2)反应器2中的铜将会从紫红色变为_________ 色。
(3)反应器3中反应的化学方程式是_________ 。
(4)反应器4中生石灰先与水反应生成熟石灰,熟石灰的化学式为_________ 。
(5)_________ (填“能”或“不能”)用铁制品盛装“波尔多液”,理由是_________ 。
(1)反应器1产生的废液中含有的溶质有
(2)反应器2中的铜将会从紫红色变为
(3)反应器3中反应的化学方程式是
(4)反应器4中生石灰先与水反应生成熟石灰,熟石灰的化学式为
(5)
您最近一年使用:0次
真题
解题方法
7 . 文物是传承文化最好的物质载体。制作下列文物的材料不属于金属材料的是
| A.曾乙侯青铜编钟 | B.明宣德青花瓷器 | C.三星堆黄金权杖 | D.舞马衔杯纹银壶 |
您最近一年使用:0次
真题
解题方法
8 . 下表列出了除去物质中所含少量杂质的方法,其中正确的是
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | CO2气体 | CO | 将气体缓缓通过足量的灼热铜网 |
| B | KOH溶液 | Ca(OH)2 | 滴加碳酸钠溶液至恰好完全反应,过滤 |
| C | CaCO3固体 | CaO | 将固体混合物高温充分煅烧,直至固体质量不再减少为止 |
| D | Na2SO4溶液 | MgSO4 | 加入过量的氢氧化钠溶液,过滤,滤液中加稀硫酸至中性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
真题
解题方法
9 . 金属材料在生产生活中应用广泛。
(1)高铁电传输系统的材料主要含铜,是利用了铜良好的_______ 性。
(2)高铁轨道、车厢、附属设施使用了大量的铁合金和铝合金。小组同学探究合金中金属的化学性质。
【实验一】在分别装有质量相等和外形相同的Cu、Fe、A1和Mg的四个烧杯中,加入相同质量的溶质质量分数为7.3%的盐酸,如图1所示。_______ ,反应的化学方程式为_______ 。
②在烧杯丙、丁中,使用温度传感器,测得反应过程中温度的变化曲线如图2所示,据图分析可知,金属活动性Mg>Al,其理由是_______ 。
③分析实验一和实验二,下列说法正确的是_______ (填序号)。
A.由实验一、二可知,金属活动性Mg>Al>Fe>Cu
B.实验二反应后所得溶液中一定有AlCl3
C.实验二充分反应后,所得溶液的质量一定减小
D.实验一,若丁中固体有剩余,则丙、丁中参加反应的盐酸的质量相等
(3)某铝合金可能含有Al、Mg、Cu中的两种或三种。现提供ng铝合金样品和足量的稀盐酸,请设计实验确定该铝合金的成分,写出依据实验获取的证据和合金可能的成分:_______ 。
(4)目前,铁是使用量最大的金属。写出工业上用赤铁矿(主要成分是Fe2O3)和CO反应生成Fe的化学方程式:_______ 。
(1)高铁电传输系统的材料主要含铜,是利用了铜良好的
(2)高铁轨道、车厢、附属设施使用了大量的铁合金和铝合金。小组同学探究合金中金属的化学性质。
【实验一】在分别装有质量相等和外形相同的Cu、Fe、A1和Mg的四个烧杯中,加入相同质量的溶质质量分数为7.3%的盐酸,如图1所示。

②在烧杯丙、丁中,使用温度传感器,测得反应过程中温度的变化曲线如图2所示,据图分析可知,金属活动性Mg>Al,其理由是

③分析实验一和实验二,下列说法正确的是
A.由实验一、二可知,金属活动性Mg>Al>Fe>Cu
B.实验二反应后所得溶液中一定有AlCl3
C.实验二充分反应后,所得溶液的质量一定减小
D.实验一,若丁中固体有剩余,则丙、丁中参加反应的盐酸的质量相等
(3)某铝合金可能含有Al、Mg、Cu中的两种或三种。现提供ng铝合金样品和足量的稀盐酸,请设计实验确定该铝合金的成分,写出依据实验获取的证据和合金可能的成分:
(4)目前,铁是使用量最大的金属。写出工业上用赤铁矿(主要成分是Fe2O3)和CO反应生成Fe的化学方程式:
您最近一年使用:0次
2024-04-24更新
|
400次组卷
|
4卷引用:2023年贵州省中考理科综合真题-初中化学
2023年贵州省中考理科综合真题-初中化学2024口袋书系列-题型专练-专题4重要规律-提高练习2024中考一轮复习考点微专题-专题05金属的化学性质-考点专练(已下线)化学(扬州卷)-学易金卷:2024年中考第二次模拟考试
真题
解题方法
10 . 金属的冶炼和利用,促进了人类的发展。
(1)明代的《菽园杂记》总记载:“用矿二百五十萝...入大旋风炉,连烹三日三夜,方见成铜。”文中的矿指硫化矿,其主要成分是Cu2S。Cu2S和氧气在高温下反应生成铜与二氧化硫,写出该反应的化学方程式:____________________ 。
(2)将一根用砂纸打磨过的铝丝浸入硫酸铜溶液中,过一会儿取出,观察到的现象是___________________ ,写出该反应的化学方程式:___________________ 。
(3)常见含铁矿石有赤铁矿、磁铁矿、菱铁矿(主要成分FeCO3)等,FeCO3中铁元素的化合价为__ 。
(4)一些活泼金属可以将相对不活泼的金属从其化合物中置换出来,例如:2Al+Fe2O3 2Fe+ Al2O3,该反应中体现出还原性的物质是
2Fe+ Al2O3,该反应中体现出还原性的物质是__ 。试计算270g铝发生上述反应时,理论上最多生成铁的质量是多少(写出计算过程)?_
(5)等质量的Cu2S和Fe2O3中所含铜元素与铁元素的质量比为____ (填最简整数比)。
(1)明代的《菽园杂记》总记载:“用矿二百五十萝...入大旋风炉,连烹三日三夜,方见成铜。”文中的矿指硫化矿,其主要成分是Cu2S。Cu2S和氧气在高温下反应生成铜与二氧化硫,写出该反应的化学方程式:
(2)将一根用砂纸打磨过的铝丝浸入硫酸铜溶液中,过一会儿取出,观察到的现象是
(3)常见含铁矿石有赤铁矿、磁铁矿、菱铁矿(主要成分FeCO3)等,FeCO3中铁元素的化合价为
(4)一些活泼金属可以将相对不活泼的金属从其化合物中置换出来,例如:2Al+Fe2O3
 2Fe+ Al2O3,该反应中体现出还原性的物质是
2Fe+ Al2O3,该反应中体现出还原性的物质是(5)等质量的Cu2S和Fe2O3中所含铜元素与铁元素的质量比为
您最近一年使用:0次



