解题方法
1 . 科学家经历了曲折的历程,揭秘了水的组成。请写出相关反应的化学方程式。
(1)18世纪末,英国科学家普利斯特里把“易燃空气”(即 )和空气混合后在干燥、洁净的玻璃瓶中用电火花点火,发出震耳的爆鸣声,且玻璃内壁上出现了液滴。
)和空气混合后在干燥、洁净的玻璃瓶中用电火花点火,发出震耳的爆鸣声,且玻璃内壁上出现了液滴。
(2)法国科学家拉瓦锡做了另一个实验:让水蒸气通过一根烧红的铁质枪管,枪管表面有黑色固体(四氧化三铁)生成,同时得到“易燃空气”。由此他得出结论。
(1)18世纪末,英国科学家普利斯特里把“易燃空气”(即
 )和空气混合后在干燥、洁净的玻璃瓶中用电火花点火,发出震耳的爆鸣声,且玻璃内壁上出现了液滴。
)和空气混合后在干燥、洁净的玻璃瓶中用电火花点火,发出震耳的爆鸣声,且玻璃内壁上出现了液滴。(2)法国科学家拉瓦锡做了另一个实验:让水蒸气通过一根烧红的铁质枪管,枪管表面有黑色固体(四氧化三铁)生成,同时得到“易燃空气”。由此他得出结论。
您最近一年使用:0次
解题方法
2 . 纯净的氢气在空气中燃烧火焰呈淡蓝色,而实际操作中却常为黄色。某兴趣小组展开如下实验探究。
【任务一】探究氢气燃烧火焰呈黄色的主要原因
【查阅资料】含某些金属元素的物质在灼烧时使火焰呈现特殊颜色,如含钠元素物质灼烧时火焰呈黄色。
【作出假设】
猜想1:黄色火焰是由玻璃导管中钠元素引起的。
猜想2:黄色火焰的产生与气体流速有关
假设3:黄色火焰的产生与温度有关
【实验探究】实验1、2用的是普通玻璃导管,实验3用的是普通试管。
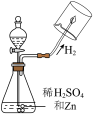
(1)写出图1中锥形瓶内反应的化学方程式________ 。
(2)由实验________ (填序号),猜想1不成立。
(3)氢气燃烧产生黄色火焰主要干扰因素是________ 。
【任务二】实验改进一设计出适合课堂演示的实验方案
【继续探究】
(4)实验进行简单改进,如图4所示,能获得稳定、流速适中的氢气,且点燃氢气时看到了淡蓝色火焰。实验步骤如下:________ (填“a”或“b”)导管的一端通过乳胶管与自来水龙头连接。
②打开自来水,将氢气排出,并在导管口处点燃氢气,可以看到氢气持续、稳定地燃烧,火焰呈淡蓝色(在暗处淡蓝色非常明显)。如果出现少量黄色火焰,立即调________ (填“大”或“小”)自来水的流速。
③在火焰上方罩一个干冷烧杯,可以看到烧杯内壁出现无色液滴,说明氢气燃烧生成了水。
④实验结束时,用湿抹布捂住导管口使火焰熄灭,再关闭自来水龙头。这样先后操作的理由是________ 。
【实验反思】
(5)【继续探究】中将玻璃管换成铁管,黄色火焰的成分更少,实验效果更好。推测是因为________ 。
(6)通过调节氢气的流速来降低________ ,可以看到明显的淡蓝色火焰。
【任务一】探究氢气燃烧火焰呈黄色的主要原因
【查阅资料】含某些金属元素的物质在灼烧时使火焰呈现特殊颜色,如含钠元素物质灼烧时火焰呈黄色。
【作出假设】
猜想1:黄色火焰是由玻璃导管中钠元素引起的。
猜想2:黄色火焰的产生与气体流速有关
假设3:黄色火焰的产生与温度有关
【实验探究】实验1、2用的是普通玻璃导管,实验3用的是普通试管。
| 实验序号 | 实验装置 | 实验现象 |
| 1.氢气燃烧 |
| 氢气燃烧时火焰主要为黄色,气体流速越大,火焰尖端黄色越明显 |
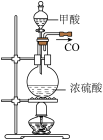
| 2.一氧化碳燃烧 |
| 一氧化碳燃烧时火焰呈蓝色。增大体流速,始终看不到黄色火焰 |
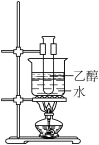
| 3.乙醇蒸气燃烧 |
| 乙醇蒸气的流速较小时,火焰为淡蓝色。流速越大,火焰尖端黄色越明显 |
(1)写出图1中锥形瓶内反应的化学方程式
(2)由实验
(3)氢气燃烧产生黄色火焰主要干扰因素是
【任务二】实验改进一设计出适合课堂演示的实验方案
【继续探究】
(4)实验进行简单改进,如图4所示,能获得稳定、流速适中的氢气,且点燃氢气时看到了淡蓝色火焰。实验步骤如下:
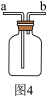
②打开自来水,将氢气排出,并在导管口处点燃氢气,可以看到氢气持续、稳定地燃烧,火焰呈淡蓝色(在暗处淡蓝色非常明显)。如果出现少量黄色火焰,立即调
③在火焰上方罩一个干冷烧杯,可以看到烧杯内壁出现无色液滴,说明氢气燃烧生成了水。
④实验结束时,用湿抹布捂住导管口使火焰熄灭,再关闭自来水龙头。这样先后操作的理由是
【实验反思】
(5)【继续探究】中将玻璃管换成铁管,黄色火焰的成分更少,实验效果更好。推测是因为
(6)通过调节氢气的流速来降低
您最近一年使用:0次
解题方法
3 . 如图是电解水及其相关实验,下列说法正确的是
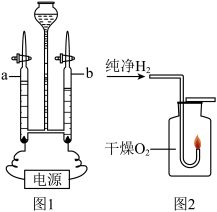
| A.与b管相连的是电源正极 |
| B.a管中产生的气体可做燃料 |
| C.如图两个实验均可证明水是由氢分子和氧分子构成的 |
| D.图2中“干燥氧气”的目的是除去水蒸气,防止对生成物的检验产生干扰 |
您最近一年使用:0次
解题方法
4 . 科技缔造生活,创新筑梦未来。中国空间站的建成标志着中国从航天大国迈向了航天强国。火箭燃料是发射梦天实验舱的长征五号B遥四运载火箭采用低温液氢液氧环保型推进剂作为动力来源。氢气与氧气反应的化学方程式为___________ ,液氢液氧推进剂被称为“环保型推进剂”的原因是___________ ,氢气没有被广泛应用的原因___________ 。
您最近一年使用:0次
解题方法
5 . 阅读下列科普短文,回答有关问题
化学电池
现代生活离不开化学电池。
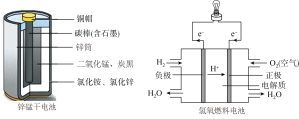
材料一:生活中常见的化学电池——锌锰干电池。 锌锰电池的原理可以用化学方程式:Zn+2MnO2+2NH4Cl=ZnCl2+Mn2O3+2NH3↑+H2O表示。锌锰电池是一种一次性电池,锌锰电池对环境污染很严重,一节 5 号废电池可以污染数十立方米的水,使一平方米土地荒废。
(1)氢氧燃料电池中H2在电源负极_____ (填“得到”或“失去”)了电子。
(2)锌锰干电池中碳棒具有_____ 性,故在实验中可以作电池的电极。
(3)在锌锰干电池的反应材料中,属于氧化物的是_____ (写化学式)。
(4)氢氧燃料电池是通过燃料的燃烧反应设计的,它的反应方程式为_____ 。
(5)氢氧燃料电池优于锌锰干电池的理由:______ (写出一条即可)。
化学电池
现代生活离不开化学电池。
材料一:生活中常见的化学电池——锌锰干电池。 锌锰电池的原理可以用化学方程式:Zn+2MnO2+2NH4Cl=ZnCl2+Mn2O3+2NH3↑+H2O表示。锌锰电池是一种一次性电池,锌锰电池对环境污染很严重,一节 5 号废电池可以污染数十立方米的水,使一平方米土地荒废。
(1)氢氧燃料电池中H2在电源负极
(2)锌锰干电池中碳棒具有
(3)在锌锰干电池的反应材料中,属于氧化物的是
(4)氢氧燃料电池是通过燃料的燃烧反应设计的,它的反应方程式为
(5)氢氧燃料电池优于锌锰干电池的理由:
您最近一年使用:0次
解题方法
6 . 物质的用途是由性质决定。下列物质的性质与用途相对应的是
| A.氢气具有还原性,可以制氢气球 | B.氢氧化铝能与酸反应,可以中和胃酸 |
| C.浓盐酸具有挥发性,可用于金属除锈 | D.石墨具有导电性,可用于制作铅笔芯 |
您最近一年使用:0次
7 . 无处安放的“核污染水”
2024年4月19日,日本开始第五轮将含有大量放射性氚(质子数为1、中子数为2的一种氢原子)的核污染水排入大海。核污染水来自日本福岛第一核电站。2011年由于地震造成核反应堆堆芯熔毁,随后发生氢气爆炸,放射性物质大量释放。为降低反应堆温度,注入了大量冷却水。放射性物质溶于冷却水得到核污染水,十多年来核污染水越来越多,已无处存放,日本政府决定将其排入大海。
我国有11座核电站,为何不愁有核污染水产生?因为我国有先进的超高温气冷堆核电技术。高温气冷堆的核燃料是用石墨材料包裹的燃料球,它能承受1620℃的高温。为防止堆芯熔毁,还采用高温下也不会反应的氦气作为冷却剂,在风机驱动下,利用氦气的高导热性,将堆芯释放的热量带出核反应堆。反应堆出口蒸气温度高达750℃,可以满足大多数行业的热源需求。反应堆还有自动停堆系统,堆芯只要稍微过热便会自动停堆,终止核反应,彻底避免了堆芯熔毁以及核泄漏的可能性。
(1)放射性氚属于________ (填写元素名称)元素。
(2)福岛核电站爆炸的原因是________ (用化学方程式解释)。
(3)石墨材料具有的性质是________ 。
(4)氦气在高温下也不会反应,是因为________ 。
(5)反应堆出口的高温蒸气可用于________ 。
(6)超高温气冷堆核电技术的最大特点是________ 。
2024年4月19日,日本开始第五轮将含有大量放射性氚(质子数为1、中子数为2的一种氢原子)的核污染水排入大海。核污染水来自日本福岛第一核电站。2011年由于地震造成核反应堆堆芯熔毁,随后发生氢气爆炸,放射性物质大量释放。为降低反应堆温度,注入了大量冷却水。放射性物质溶于冷却水得到核污染水,十多年来核污染水越来越多,已无处存放,日本政府决定将其排入大海。
我国有11座核电站,为何不愁有核污染水产生?因为我国有先进的超高温气冷堆核电技术。高温气冷堆的核燃料是用石墨材料包裹的燃料球,它能承受1620℃的高温。为防止堆芯熔毁,还采用高温下也不会反应的氦气作为冷却剂,在风机驱动下,利用氦气的高导热性,将堆芯释放的热量带出核反应堆。反应堆出口蒸气温度高达750℃,可以满足大多数行业的热源需求。反应堆还有自动停堆系统,堆芯只要稍微过热便会自动停堆,终止核反应,彻底避免了堆芯熔毁以及核泄漏的可能性。

(1)放射性氚属于
(2)福岛核电站爆炸的原因是
(3)石墨材料具有的性质是
(4)氦气在高温下也不会反应,是因为
(5)反应堆出口的高温蒸气可用于
(6)超高温气冷堆核电技术的最大特点是
您最近一年使用:0次
8 . 纳米零价铁在环保领域应用广泛。学习小组对其制备及应用其进行如下探究。
高温条件下,以菱铁矿和H2为原料制备纳米零价铁,其他产物为水和二氧化碳。
已知:菱铁矿主要含 ,所含杂质高温下不与
,所含杂质高温下不与 反应。
反应。
(1)请用化学方程式表示该制备原理:_______ 。
Ⅱ 探究剩余固体的成分
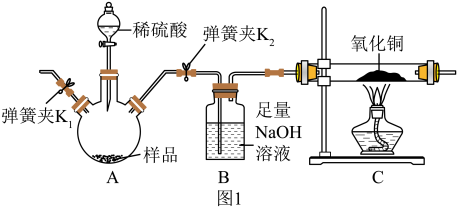
利用图1所示装置,对制备纳米零价铁一段时间后剩余固体的成分进行探究。
部分实验步骤如下:
步骤1:称取15.0g剩余固体的样品置于装置A中;
步骤2:打开 、
、 ,通一段时间N2后关闭K2,称量装置B、C及其所含药品的质量,分别为160.0g、146.0g;
,通一段时间N2后关闭K2,称量装置B、C及其所含药品的质量,分别为160.0g、146.0g;
步骤3:关闭 、打开
、打开 ,先向A中缓慢注入稀硫酸,再点燃酒精灯;
,先向A中缓慢注入稀硫酸,再点燃酒精灯;
步骤4:待装置A中不再产生气泡时,停止注入稀硫酸,熄灭酒精灯;
步骤5:打开 ,缓缓通入
,缓缓通入 ,至装置C中玻璃管冷却至室温后,称量装置B、C及其所含药品的质量,分别为161.1g、142.8g;
,至装置C中玻璃管冷却至室温后,称量装置B、C及其所含药品的质量,分别为161.1g、142.8g;
步骤6:将装置A中物质取出过滤,将滤渣洗涤、干燥后称量质量,为1.5g。
(2)步骤2中通N2的主要目的是_______ 。
(3)步骤3中,观察到有大量气泡产生,溶液由无色变浅绿色,能否说明样品中一定含有单质铁?请作出判断并说明理由:_______ 。
(4)根据实验现象及数据,均能确定样品中含有单质铁。
已知:加热条件下氢气具有还原性;菱铁矿中所含杂质不溶于水和酸。
①装置C中_______ (填实验现象)能证明样品中存在单质铁。
②样品中单质铁的质量分数为_______ (精确到0.1%)。
Ⅲ 用纳米零价铁处理废水
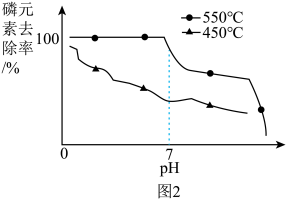
(5)去除废水中的磷元素。将制得的纳米零价铁在450℃及550℃下进行热处理,再分别对不同酸碱度的水体进行处理,磷元素的去除率如图2所示。据图可知,温度为_______ 时、_______ (填“酸性”或“碱性”)条件下处理效果更好。
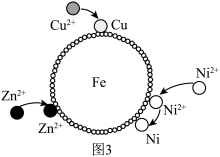
(6)去除废水中的金属离子。根据金属活动性顺序,去除途径可分三种(如图3):第一类是吸附捕捉,第二类是直接反应,第三类是吸附捕捉再慢慢反应。 的去除途径属于第
的去除途径属于第_______ 类。
②若 的去除途径属于第一类,则Cd的金属活动性比Ag的
的去除途径属于第一类,则Cd的金属活动性比Ag的_______ (填“强”或“弱”)。
高温条件下,以菱铁矿和H2为原料制备纳米零价铁,其他产物为水和二氧化碳。
已知:菱铁矿主要含
 ,所含杂质高温下不与
,所含杂质高温下不与 反应。
反应。(1)请用化学方程式表示该制备原理:
Ⅱ 探究剩余固体的成分
利用图1所示装置,对制备纳米零价铁一段时间后剩余固体的成分进行探究。
部分实验步骤如下:
步骤1:称取15.0g剩余固体的样品置于装置A中;
步骤2:打开
 、
、 ,通一段时间N2后关闭K2,称量装置B、C及其所含药品的质量,分别为160.0g、146.0g;
,通一段时间N2后关闭K2,称量装置B、C及其所含药品的质量,分别为160.0g、146.0g;步骤3:关闭
 、打开
、打开 ,先向A中缓慢注入稀硫酸,再点燃酒精灯;
,先向A中缓慢注入稀硫酸,再点燃酒精灯;步骤4:待装置A中不再产生气泡时,停止注入稀硫酸,熄灭酒精灯;
步骤5:打开
 ,缓缓通入
,缓缓通入 ,至装置C中玻璃管冷却至室温后,称量装置B、C及其所含药品的质量,分别为161.1g、142.8g;
,至装置C中玻璃管冷却至室温后,称量装置B、C及其所含药品的质量,分别为161.1g、142.8g;步骤6:将装置A中物质取出过滤,将滤渣洗涤、干燥后称量质量,为1.5g。
(2)步骤2中通N2的主要目的是
(3)步骤3中,观察到有大量气泡产生,溶液由无色变浅绿色,能否说明样品中一定含有单质铁?请作出判断并说明理由:
(4)根据实验现象及数据,均能确定样品中含有单质铁。
已知:加热条件下氢气具有还原性;菱铁矿中所含杂质不溶于水和酸。
①装置C中
②样品中单质铁的质量分数为
Ⅲ 用纳米零价铁处理废水
(5)去除废水中的磷元素。将制得的纳米零价铁在450℃及550℃下进行热处理,再分别对不同酸碱度的水体进行处理,磷元素的去除率如图2所示。据图可知,温度为
(6)去除废水中的金属离子。根据金属活动性顺序,去除途径可分三种(如图3):第一类是吸附捕捉,第二类是直接反应,第三类是吸附捕捉再慢慢反应。
 的去除途径属于第
的去除途径属于第②若
 的去除途径属于第一类,则Cd的金属活动性比Ag的
的去除途径属于第一类,则Cd的金属活动性比Ag的
您最近一年使用:0次
解题方法
9 . 下列物质间转化不能通过一步反应实现的是
| A.CaO→CaCl2→CaCO3 | B.Fe2O3→Fe→FeCl2 |
| C.NaCl→Na2CO3→NaNO3 | D.HCl→H2→Cu |
您最近一年使用:0次
7日内更新
|
56次组卷
|
2卷引用:2024年5月山东省曲阜市第二次中考模拟化学试题
10 . 有关物质的鉴别,下列方案正确的是
| A.鉴别硫酸钠和氯化钠溶液,分别滴加硝酸银溶液和稀硝酸 |
| B.鉴别溶液的酸碱度滴加石蕊溶液 |
| C.鉴别一氧化碳和氢气两种气体,分别通过灼热的氧化铜,观察现象 |
| D.鉴别硝酸铵和碳酸氢铵固体,闻气味 |
您最近一年使用:0次